硅因为具有半导体的性质被认为是一种比较特殊的非金属元素,它的单质是硬度较大的非金属单质。铬单质为钢灰色金属,是自然界硬度最大的金属。
(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布_______ 。
(2)与硅同周期的金属第一电离能由大到小排列:_______ 。与硅同周期的非金属电负性由小到大排列:_______ 。
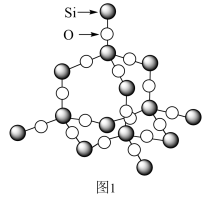
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是_______ (选填“原子晶体”、“分子晶体”或“离子晶体”,下同)。与硅同主族的元素碳的氧化物干冰是_______ 。1mol二氧化硅晶体所含有的σ键个数为_______ 。1mol的乙炔含有π键的个数为_______ 。
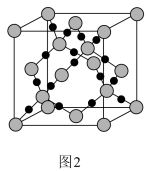
(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度_______ g/cm3。(列出计算式)

(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布
(2)与硅同周期的金属第一电离能由大到小排列:
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是

(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度
更新时间:2021-12-21 11:57:02
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi),在性质上表现出从典型的非金属元素到典型的金属元素的过渡。回答下列问题:
(1)①基态N原子含有___________ 种不同能量的电子。
② 、
、 、
、 、
、 中,中心原子与
中,中心原子与 中N原子杂化类型相同的为
中N原子杂化类型相同的为___________ (填化学式,下同),微粒的空间结构相同的为___________ 和___________ ;键角:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
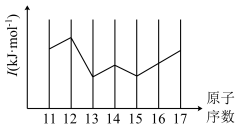
(2)第三周期主族元素某一级电离能如图所示,该电离能是第___________ (填“一”“二”或“三”)电离能,其中P的该级电离能比Si小的原因为___________ 。
(3) 和
和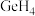 的沸点如下表:
的沸点如下表:
 的沸点比
的沸点比 的沸点高的主要原因为
的沸点高的主要原因为___________ 。
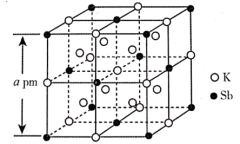
(4)锑钾(Sb-K)合金的立方晶胞结构如图所示,晶胞中锑原子与钾原子的数量比为___________ 。若该合金的密度为 ,该合金的摩尔质量为
,该合金的摩尔质量为___________  (
( 表示阿伏加德罗常数的值,用含
表示阿伏加德罗常数的值,用含 、a、
、a、 的式子表示)。
的式子表示)。
(1)①基态N原子含有
②
 、
、 、
、 、
、 中,中心原子与
中,中心原子与 中N原子杂化类型相同的为
中N原子杂化类型相同的为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)第三周期主族元素某一级电离能如图所示,该电离能是第

(3)
 和
和 的沸点如下表:
的沸点如下表:| 物质 |  |  |
| 沸点 | -62℃ | -90℃ |
 的沸点比
的沸点比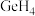 的沸点高的主要原因为
的沸点高的主要原因为(4)锑钾(Sb-K)合金的立方晶胞结构如图所示,晶胞中锑原子与钾原子的数量比为
 ,该合金的摩尔质量为
,该合金的摩尔质量为 (
( 表示阿伏加德罗常数的值,用含
表示阿伏加德罗常数的值,用含 、a、
、a、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素.回答下列问题;
(1)钪(Sc)元素的原子核外电子排布式为_____________ 。钬(Ho)的基态原子电子排布式为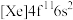 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为_________ 。
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是_____________ 。
几种稀土元素的电离能(单位:kJ/mol)
(3)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+ CH2=CH2;ICH2CH2I中碳原子杂化轨道类型为________ 。
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有___________ 。
(5)1molCH2=CH2中含有的 键数目为:
键数目为:____________ 。
(1)钪(Sc)元素的原子核外电子排布式为
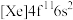 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是
几种稀土元素的电离能(单位:kJ/mol)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有
(5)1molCH2=CH2中含有的
 键数目为:
键数目为:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】砷化镓(GaAs)是当前最重要、技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs___________ GaN(填“>”或“<”,下同),第一电离能Ga___________ As。
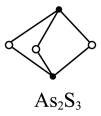
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为___________ 。
(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为______ 。
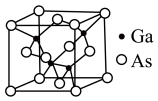
(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为___________ cm。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为

(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为

(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为
您最近一年使用:0次
【推荐1】W、X、Y、Z、N是原子序数依次增大的5种短周期元素,其元素性质或原子结构如下:
请完成下列空白:
(1)写出各元素的元素符号:W:___________ 、X:___________ 、Y:___________ 、Z:___________ 、N:___________ 。
(2)X、Y和Z三种元素的原子半径由大到小的顺序:___________ (请填元素符号)。
(3)X、Z和N三种元素的电负性由大到小的顺序:___________ (请填元素符号)。
(4)Y、Z和N三种元素的第一电离能由大到小的顺序:___________ (请填元素符号)。
| 元素 | 元素性质或原子结构 |
| W | 电子只有一种自旋取向 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| Y | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都高于同周期相邻元素 |
| Z | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| N | 只有一个不成对电子 |
(1)写出各元素的元素符号:W:
(2)X、Y和Z三种元素的原子半径由大到小的顺序:
(3)X、Z和N三种元素的电负性由大到小的顺序:
(4)Y、Z和N三种元素的第一电离能由大到小的顺序:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: ;二锗酸钠:
;二锗酸钠: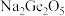 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。
① 中锗原子的杂化方式是
中锗原子的杂化方式是_______ 。
②推测1mol 中含有的σ键的数目是
中含有的σ键的数目是_______ (用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(2)利用离子液体 可电沉积还原金属Ge,其熔点只有7℃,其中
可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。

①该物质的晶体类型是_______ 。
② 中组成元素的电负性由小到大的顺序是
中组成元素的电负性由小到大的顺序是_______ 。
(3)独立的 分子中H−N−H的键角约为
分子中H−N−H的键角约为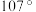 ,
, 中H−N−H的键角
中H−N−H的键角_______ 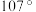 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
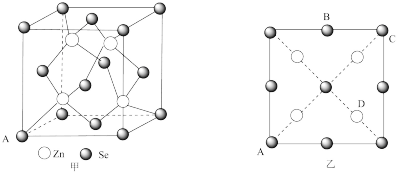
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是_______ ;已知晶胞边长为apm,乙图为甲图的俯视图,A点坐标为(0,0,0),B点坐标为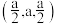 ,则D点坐标为
,则D点坐标为_______ ;若该晶胞密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为_______ (只列出计算式)。
(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
 ;二锗酸钠:
;二锗酸钠: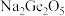 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。①
 中锗原子的杂化方式是
中锗原子的杂化方式是②推测1mol
 中含有的σ键的数目是
中含有的σ键的数目是 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(2)利用离子液体
 可电沉积还原金属Ge,其熔点只有7℃,其中
可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
①该物质的晶体类型是
②
 中组成元素的电负性由小到大的顺序是
中组成元素的电负性由小到大的顺序是(3)独立的
 分子中H−N−H的键角约为
分子中H−N−H的键角约为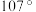 ,
, 中H−N−H的键角
中H−N−H的键角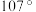 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
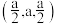 ,则D点坐标为
,则D点坐标为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】铜是应用最广泛的金属之一,其抗氧化防腐技术一直是化学研究的热点课题。
(1)基态铜原子的价电子排布图为_____ ,铜元素位于元素周期表中_____ 区。
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为_____ 。
②HCOO-中碳原子的杂化方式为_____ ,其空间构型为____ 。
③HCOOH能与水任意比互溶的原因为_____ 。
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于_____ 晶体。
(1)基态铜原子的价电子排布图为
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为
②HCOO-中碳原子的杂化方式为
③HCOOH能与水任意比互溶的原因为
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】LiFePO4、LiPF6、LiAsF6、LiCl等常用于锂离子聚合物电池。请回答:
(1) 的立体构型是
的立体构型是___________ 。
(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为___________ 。
(3)抗坏血酸(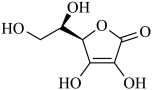 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是___________ 。
(4)电池工作时,Li⁺沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出),电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
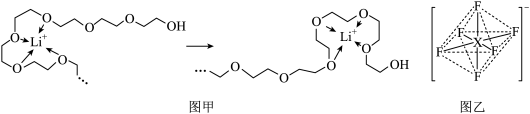
①从化学键角度看,Li⁺迁移过程发生___________ (填“物理”或“化学”)变化。
②已知相同条件下,锂离子的迁移速率与离子键的强弱有关,则Li⁺在___________ (选填“LiPF6”或“LiAsF6”)中迁移较快。
③图乙中X的杂化方式最可能是___________ (填字母编号)。
a.sp3 b.sp3d c.sp3d2 d.sp3d3
(5)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有___________ 个“Cu2O”;Cu2O晶胞中Cu的配位数是___________ ;若①处Cu原子坐标为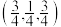 ,②处Cu原子坐标为
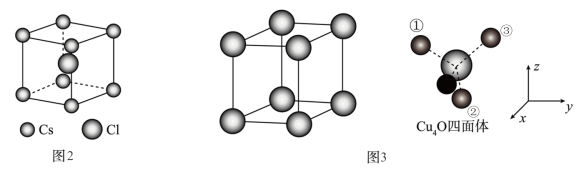
,②处Cu原子坐标为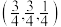 ,则③处Cu原子坐标为(___________,
,则③处Cu原子坐标为(___________,___________ ,)。
(1)
 的立体构型是
的立体构型是(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(3)抗坏血酸(
 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是(4)电池工作时,Li⁺沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出),电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①从化学键角度看,Li⁺迁移过程发生
②已知相同条件下,锂离子的迁移速率与离子键的强弱有关,则Li⁺在
③图乙中X的杂化方式最可能是
a.sp3 b.sp3d c.sp3d2 d.sp3d3
(5)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有
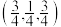 ,②处Cu原子坐标为
,②处Cu原子坐标为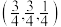 ,则③处Cu原子坐标为(___________,
,则③处Cu原子坐标为(___________,
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】磷及其化合物在电池、催化等领域有重要应用。回答下列问题:
(1)LiPF6、LiAsF6等可作为聚乙二醇锂离子电池的电极材料。电池放电时,Li+沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子未画出)。

①Li+迁移过程发生________ (填“物理”或“化学”)变化。
②相同条件下,使用________ (填“LiPF6”或“LiAsF6”)作电极材料时,Li+迁移速率较快,原因是________ 。
(2)PCl5是一种白色晶体,其晶胞如图所示。该晶体熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。
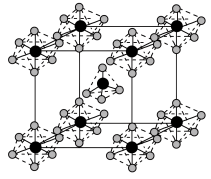
①写出PCl5熔融时的电离方程式________ 。
②若晶胞参数为anm,则晶体的密度为________  (列出计算式)。
(列出计算式)。
(3)最简单的硼烷是B2H6,其分子结构如图(Ⅰ)所示,B原子的杂化方式为________ 。NaBH4是一种重要的储氢载体,NaBH4中的阴离子空间构型是________ 。

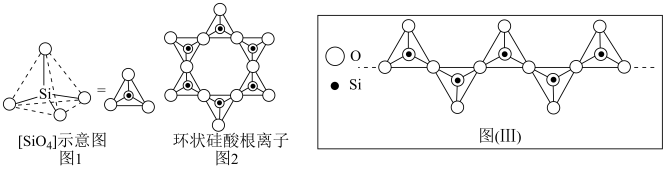
(4)硅酸盐中的硅酸根离子通常以[SiO4]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:________ 。图Ⅲ中钠盐的化学式为________ 。
(5)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态Ni原子,其价电子的自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态Ni原子,其价电子的自旋磁量子数的代数和为________ 。
(1)LiPF6、LiAsF6等可作为聚乙二醇锂离子电池的电极材料。电池放电时,Li+沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子未画出)。

①Li+迁移过程发生
②相同条件下,使用
(2)PCl5是一种白色晶体,其晶胞如图所示。该晶体熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。

①写出PCl5熔融时的电离方程式
②若晶胞参数为anm,则晶体的密度为
 (列出计算式)。
(列出计算式)。(3)最简单的硼烷是B2H6,其分子结构如图(Ⅰ)所示,B原子的杂化方式为

(4)硅酸盐中的硅酸根离子通常以[SiO4]四面体(如图1所示)的方式形成链状、环状或网络状复杂阴离子,图2所示为一种环状硅酸根离子,写出其化学式:

(5)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态Ni原子,其价电子的自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态Ni原子,其价电子的自旋磁量子数的代数和为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】元素A、B、C、D、E、F、G在元素周期表中的位置如图所示,回答下列问题:
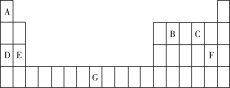
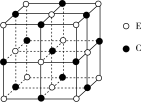
(1)G的基态原子价层电子排布式为_______ 。原子的第一电离能:D_____ E(填“>”或“<”)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l—l>l—b>b—b(l为孤对电子对,b为键合电子对),则关于A2C中的A—C—A键角可得出的结论是________。
(3)化合物G(BC)5的熔点为-20℃,沸点为103℃,其固体属于_______ 晶体,该物质中存在的化学键类型有_________ 。
(4)化合物BCF2的立体构型为________ ,其中B原子的杂化轨道类型是________ 。
(5)化合物EC的晶胞结构如图所示,晶胞参数a=0.424nm。则EC晶体的密度(g·cm-3)_______ 。(写出表达式)


(1)G的基态原子价层电子排布式为
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l—l>l—b>b—b(l为孤对电子对,b为键合电子对),则关于A2C中的A—C—A键角可得出的结论是________。
| A.180° | B.接近120°,但小于120° |
| C.接近120°,但大于120° | D.接近109°28’,但小于109°28’ |
(4)化合物BCF2的立体构型为
(5)化合物EC的晶胞结构如图所示,晶胞参数a=0.424nm。则EC晶体的密度(g·cm-3)
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】下面是一些晶体的结构示意图。
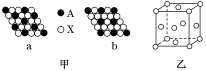
(1)下列关于晶体的说法正确的是___________(填字母)。
(2)图甲表示的是晶体的二维平面示意图,a、b中可表示化学式为AX3的化合物的是___________ (填“a”或“b”)。
(3)图乙表示的是金属铜的晶胞。
①该晶胞“实际”拥有的铜原子数是___________ ,铜原子的配位数为___________ 。
②该晶胞称为___________ (填字母)。
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
(4)NiO、FeO的晶体结构相同,且r(Fe2+)>r(Ni2+),NiO的熔点为1 960 ℃,则FeO的熔点___________ (填“>”或“<”)1 960 ℃,判断的依据是___________ 。

(1)下列关于晶体的说法正确的是___________(填字母)。
| A.晶体的形成与晶体的自范性有关 |
| B.可以用X射线衍射仪区分晶体和非晶体 |
| C.石蜡是非晶体,但有固定的熔点 |
| D.晶胞就是晶体 |
(3)图乙表示的是金属铜的晶胞。
①该晶胞“实际”拥有的铜原子数是
②该晶胞称为
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
(4)NiO、FeO的晶体结构相同,且r(Fe2+)>r(Ni2+),NiO的熔点为1 960 ℃,则FeO的熔点
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】某加碘盐的包装袋上有如下说明,回答下列问题:
(1)加碘盐中的“碘”是指碘酸钾,其化学式为___________ ,碘元素在周期表中的位置为___________ 。
(2)①比较离子半径:Na+___________ Cl-(填“大于”或“小于”),其原因是___________ 。
②NaCl晶胞如图,若NaCl晶体的密度为dg·cm-3,则晶体中Na+与Na+之间的最短距离是___________ cm。(已知阿伏加德罗常数的值为NA)
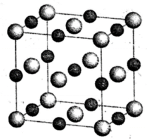
(3)食盐中的抗结剂常见的是亚铁氰化钾,其化学式为K4[Fe(CN)6]。CN-的电子式是___________ ,1molCN-中含有π键的数目为___________ 。在该配合物中所含化学键的类型有___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(4)二茂铁(结构简式为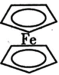 )是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为
)是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为___________ 。
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 18~33mg/kg |
(1)加碘盐中的“碘”是指碘酸钾,其化学式为
(2)①比较离子半径:Na+
②NaCl晶胞如图,若NaCl晶体的密度为dg·cm-3,则晶体中Na+与Na+之间的最短距离是

(3)食盐中的抗结剂常见的是亚铁氰化钾,其化学式为K4[Fe(CN)6]。CN-的电子式是
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(4)二茂铁(结构简式为
 )是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为
)是重要的有机金属化合物,常温下为橙黄色粉末,熔点172~174℃,沸点249℃,100℃以上能升华,不溶于水,易溶于苯、乙醚等有机溶剂。根据以上性质,判断二茂铁的晶体类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。回答下列问题:
(1)镍元素在周期表中的位置为___________ ,基态镍原子未成对电子数为___________ 。
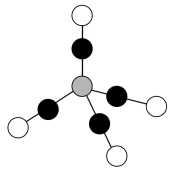
(2)区分晶体和非晶体最可靠的科学方法为___________ ;配合物Ni(CO)4熔点−19.3℃,沸点42.1℃,难溶于水,易溶于有机溶剂,结构见下图,则固态Ni(CO)4属于___________ 晶体,1mol Ni(CO)4含有___________ mol配位键。
(3)NiO的晶体结构类型与NaCl相似,离子半径如下表所示:NiO晶胞中Ni2+的配位数为____ ,NiO的熔点比NaCl高的原因是______ 。
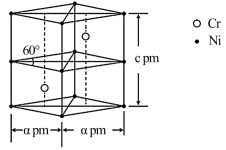
(4)某铬镍合金晶胞如图所示,Cr、Ni原子个数比为__ ,该晶胞中Cr、Ni原子最近距离为__ pm(用含a、c的代数式表示)。
(1)镍元素在周期表中的位置为
(2)区分晶体和非晶体最可靠的科学方法为

(3)NiO的晶体结构类型与NaCl相似,离子半径如下表所示:NiO晶胞中Ni2+的配位数为
| Na+ | 102pm | Cl- | 181pm |
| Ni2+ | 69pm | O2− | 140pm |

您最近一年使用:0次



