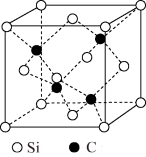LiFePO4、LiPF6、LiAsF6、LiCl等常用于锂离子聚合物电池。请回答:
(1) 的立体构型是
的立体构型是___________ 。
(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为___________ 。
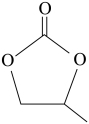
(3)抗坏血酸(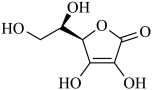 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是___________ 。
(4)电池工作时,Li⁺沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出),电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
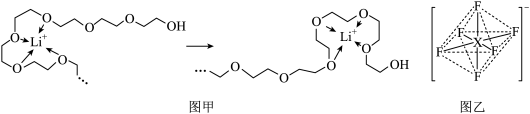
①从化学键角度看,Li⁺迁移过程发生___________ (填“物理”或“化学”)变化。
②已知相同条件下,锂离子的迁移速率与离子键的强弱有关,则Li⁺在___________ (选填“LiPF6”或“LiAsF6”)中迁移较快。
③图乙中X的杂化方式最可能是___________ (填字母编号)。
a.sp3 b.sp3d c.sp3d2 d.sp3d3
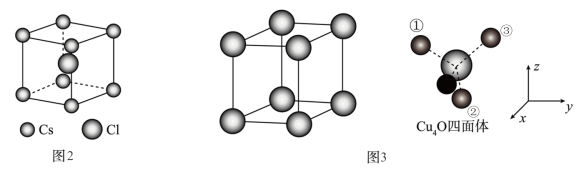
(5)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有___________ 个“Cu2O”;Cu2O晶胞中Cu的配位数是___________ ;若①处Cu原子坐标为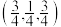 ,②处Cu原子坐标为
,②处Cu原子坐标为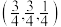 ,则③处Cu原子坐标为(___________,
,则③处Cu原子坐标为(___________,___________ ,)。
(1)
 的立体构型是
的立体构型是(2)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(3)抗坏血酸(
 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是(4)电池工作时,Li⁺沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出),电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①从化学键角度看,Li⁺迁移过程发生
②已知相同条件下,锂离子的迁移速率与离子键的强弱有关,则Li⁺在
③图乙中X的杂化方式最可能是
a.sp3 b.sp3d c.sp3d2 d.sp3d3
(5)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有
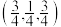 ,②处Cu原子坐标为
,②处Cu原子坐标为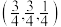 ,则③处Cu原子坐标为(___________,
,则③处Cu原子坐标为(___________,
更新时间:2023-05-22 13:42:49
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】I.乙烯是重要有机化工原料,以乙烯为原料合成部分化工产品的流程如下(部分反应条件略去)。
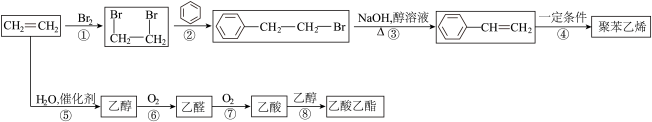
回答下列问题:
(1)乙酸的官能团的名称是___________ 。
(2)反应②的反应类型是___________ 。
(3)聚苯乙烯的结构简式为___________ 。
(4)反应⑧的化学方程式为___________ 。
Ⅱ.回答以下问题。
(5)基态Cu原子的核外电子排布式为___________ 。
(6)NH3的空间结构是___________ 。
(7)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为apm,则该晶体的密度是___________ g·cm-3。

回答下列问题:
(1)乙酸的官能团的名称是
(2)反应②的反应类型是
(3)聚苯乙烯的结构简式为
(4)反应⑧的化学方程式为
Ⅱ.回答以下问题。
(5)基态Cu原子的核外电子排布式为
(6)NH3的空间结构是
(7)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为apm,则该晶体的密度是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】异氰酸苯酯( )是重要的农药中间体,广泛用于合成杀菌剂、除草剂、植物生长调节剂等制备异氰酸苯酯最常用、最经济的原料是苯胺与光气反应,其反应过程如图:
)是重要的农药中间体,广泛用于合成杀菌剂、除草剂、植物生长调节剂等制备异氰酸苯酯最常用、最经济的原料是苯胺与光气反应,其反应过程如图:
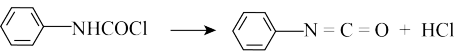
(1)
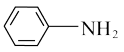 中的官能团是
中的官能团是(2)①光气(COCl2)的结构式为
②氯元素基态原子的电子排布式为
(3)氯吡苯脲是经国家批准使用的植物生长膨大剂之一、其结构简式为
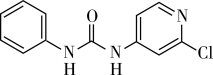 。
。资料:异氛酸苯酯与2-氯-4-氨基吡啶反应,可生成氯吡苯脲,其反应方程式如下:
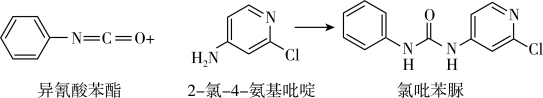 。
。
①该反应的反应类型为
②反应过程中,每生成1个氯吡苯脲,断裂
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有NH3、CO2、H2O等。
①CO2、NH3的空间结构分别是
②请用共价键知识解释H2O分子比NH3分子稳定的原因
您最近一年使用:0次
【推荐3】法国一家公司研发出一种比锂电池成本更低、寿命更长、充电速度更快的钠离子电池,该电池的负极材料为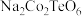 (制备原料为
(制备原料为 、
、 和
和 ),电解液为
),电解液为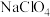 的碳酸丙烯酯溶液。回答下列问题:
的碳酸丙烯酯溶液。回答下列问题:
(1)基态Na原子中,核外电子占据的原子轨道总数为_______ ,Te属于元素周期表中_______ 区元素,其基态原子的价电子排布式为_______ 。
(2) 的空间结构为
的空间结构为_______ ,碳酸丙烯酯的结构简式如图所示,其中碳原子的杂化轨道类型为_______ ,1mol碳酸丙烯酯中 键的数目为
键的数目为_______ 。
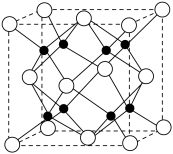
(3)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为_______ ,该晶胞的密度为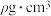 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为_______ cm(用含有 、
、 的代数式表示)。
的代数式表示)。
 (制备原料为
(制备原料为 、
、 和
和 ),电解液为
),电解液为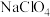 的碳酸丙烯酯溶液。回答下列问题:
的碳酸丙烯酯溶液。回答下列问题:(1)基态Na原子中,核外电子占据的原子轨道总数为
(2)
 的空间结构为
的空间结构为 键的数目为
键的数目为
(3)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为
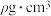 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
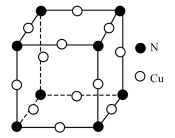
【推荐1】铁、钴、镍都属于第Ⅷ族元素,它们的单质、合金及其化合物在催化剂和能源领域用途非常广泛。
⑴基态Fe2+的核外电子排布式为____ 。结合电子排布式分析Fe3+比Co3+氧化性弱的原因:_____ 。
⑵BNCP可用于激光起爆器等,BNCP可由N2H4、HClO4、CTCN、NaNT共反应制备。
①ClO4-的空间构型为________ 。
②CTCN的化学式为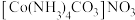 ,与Co3+形成配位键的原子是
,与Co3+形成配位键的原子是________ 。(已知CO32−的结构式为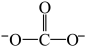 )
)
③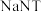 可以
可以 (双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为
(双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为________ ,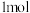
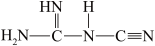 中含有σ键的物质的量为
中含有σ键的物质的量为________ 。
④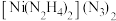 是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为
是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为_____ 。
⑶一种新型的功能材料的晶胞结构如图所示,Mn在面心和顶点,它的化学式可表示为________ 。
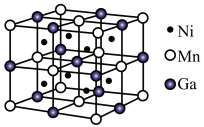
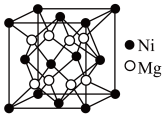
⑷镍镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间的距离为anm。则镍镁晶体未储氢时的密度为________ (列出计算表达式,NA表示阿伏加 德罗常数的数值) g∙cm-3。
⑴基态Fe2+的核外电子排布式为
⑵BNCP可用于激光起爆器等,BNCP可由N2H4、HClO4、CTCN、NaNT共反应制备。
①ClO4-的空间构型为
②CTCN的化学式为
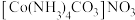 ,与Co3+形成配位键的原子是
,与Co3+形成配位键的原子是 )
)③
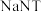 可以
可以 (双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为
(双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为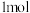
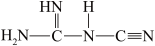 中含有σ键的物质的量为
中含有σ键的物质的量为④
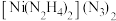 是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为
是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为⑶一种新型的功能材料的晶胞结构如图所示,Mn在面心和顶点,它的化学式可表示为

⑷镍镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间的距离为anm。则镍镁晶体未储氢时的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】青蒿素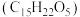 是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
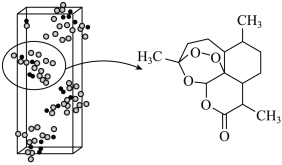
(1)提取青蒿素:在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚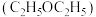 提取,效果更好。
提取,效果更好。
①乙醚沸点低于乙醇,原因是___________ 。
②用乙醚提取效果更好,原因是___________ 。
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:___________ 。
②图中晶胞的棱长分别为 ,晶体的密度为
,晶体的密度为___________  。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)
③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是___________ 。
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效:一定条件下,用 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
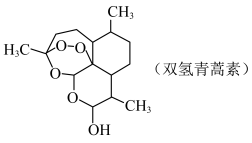
①双氢青蒿素分子中碳原子的杂化方式为___________ 。
② 的空间结构为
的空间结构为___________ , 中有
中有___________  配位键。
配位键。
③比较水溶性:双氢青蒿素___________ (填“ ”)青蒿素。
”)青蒿素。
 是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
(1)提取青蒿素:在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚
 提取,效果更好。
提取,效果更好。①乙醚沸点低于乙醇,原因是
②用乙醚提取效果更好,原因是
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中
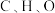 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:②图中晶胞的棱长分别为
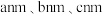 ,晶体的密度为
,晶体的密度为 。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效:一定条件下,用
 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
①双氢青蒿素分子中碳原子的杂化方式为
②
 的空间结构为
的空间结构为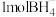 中有
中有 配位键。
配位键。③比较水溶性:双氢青蒿素
 ”)青蒿素。
”)青蒿素。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】硅及其化合物在生活、生产和科技等方面应用广泛。工业制备高纯硅的主要过程如下:
石英砂(主要成分 )
) 粗硅
粗硅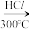

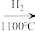 高纯硅
高纯硅
(1) 位于元素周期表第
位于元素周期表第_____ 周期,第_____ 族。
(2)由硅原子核形成的三种微粒,电子排布式分别为:a.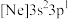 、b.
、b.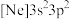 、c.
、c.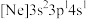 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。
(3)石英砂与焦炭反应制备粗硅的化学方程式为_____ 。粗硅与 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为_____ 。 的键角
的键角_____ (填“大于”、“小于”或“等于”) 的键角。
的键角。
(4) 以空间结构为
以空间结构为_____ 。 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式_____ (已知:电负性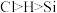 )。
)。
石英砂(主要成分
 )
) 粗硅
粗硅

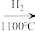 高纯硅
高纯硅(1)
 位于元素周期表第
位于元素周期表第(2)由硅原子核形成的三种微粒,电子排布式分别为:a.
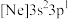 、b.
、b.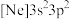 、c.
、c.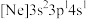 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。A.微粒半径: |
| B.电子排布属于基态原子(或离子)的是:a、b |
C.电离一个电子所需最低能量: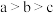 |
D.得电子能力: |
 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为 的键角
的键角 的键角。
的键角。(4)
 以空间结构为
以空间结构为 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式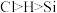 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有________ 。
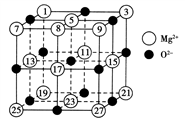
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:__________________ 。
(3)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因:_____________________________________ 。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:

(3)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1 266 | 1 534 | 183 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】Fe3+与SCN-形成的配离子颜色极似血液,常被用于电影特技和魔术表演。回答下列问题:
(1)写出Fe3+的电子排布式:___________ ;SCN-的结构式为________
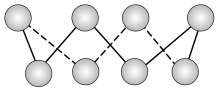
(2)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为_________ 。硫的一种同素异形体分子式为S8,其结构如图所示,其中S原子的杂化轨道类型为______ 。S8易溶于二硫化碳的原因是__________________________________________________ 。
(3)已知立方氮化硼晶体内存在配位键,则其晶体中配位键与普通共价键数目之比为______ 。原子坐标参数可表示晶胞内部各原子的相对位置,图中a处B的原子坐标参数为(0, 0, 0),则距离该B原子最近的N原子坐标参数为_________ 。
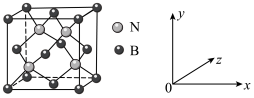
(4)单质铁的晶体结构如图所示,该堆积方式名称为________ 。已知该晶胞的密度为ρ g/cm3,则铁原子半径的计算式为______________ pm。

(1)写出Fe3+的电子排布式:
(2)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为

(3)已知立方氮化硼晶体内存在配位键,则其晶体中配位键与普通共价键数目之比为

(4)单质铁的晶体结构如图所示,该堆积方式名称为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】a、b、c、d、e均为周期表前四周期元素,原子序数依次增大,相关信息如下表所示。
请回答:
(1)画出d元素的原子结构示意图___________ 。
(2)b与其同周期相邻元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)c的氢化物水溶液中存在的氢键有___________ 种。
(4)a与其相邻同主族元素的最高价氧化物的熔点相差较大的原因是___________ 。
(5)若将a元素最高价氧化物水化物对应的正盐酸根离子表示为A,与A互为等电子体的一种分子为___________ (填化学式)。
(6)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为___________ ,若该晶体的相对分子质量为M,密度为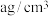 ,则晶胞的体积为
,则晶胞的体积为___________ ( 用表示阿伏伽德罗常数的值)。
用表示阿伏伽德罗常数的值)。
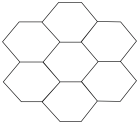
(7)a形成的某种单质的层状结构如图,其中a原子数、a-a键数之比为___________ 。
| a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
| b | 基态原子的p轨道电子数比s轨道电子数少1 |
| c | 在周期表所列元素中电负性最大 |
| d | 位于周期表中第8纵行 |
| e | 基态原子M层全充满,N层只有一个电子 |
(1)画出d元素的原子结构示意图
(2)b与其同周期相邻元素第一电离能由大到小的顺序为
(3)c的氢化物水溶液中存在的氢键有
(4)a与其相邻同主族元素的最高价氧化物的熔点相差较大的原因是
(5)若将a元素最高价氧化物水化物对应的正盐酸根离子表示为A,与A互为等电子体的一种分子为
(6)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为
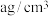 ,则晶胞的体积为
,则晶胞的体积为 用表示阿伏伽德罗常数的值)。
用表示阿伏伽德罗常数的值)。(7)a形成的某种单质的层状结构如图,其中a原子数、a-a键数之比为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】镓(Ga)是一种重要的金属,镓的化合物广泛应用于半导体、太阳能、液态合金、医疗化工等诸多领域,被称为电子工业的“脊梁”。
(1)基态Ga原子的价层电子的轨道表示式是___________________ 。
(2) 在270°C左右以二聚体
在270°C左右以二聚体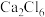 存在,结构式如图。
存在,结构式如图。
① 可以形成二聚体的原因是
可以形成二聚体的原因是__________________________ 。
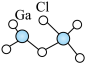
② 和
和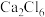 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是_________________ 。
③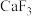 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,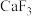 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因_____ 。
(3) 可与
可与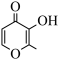 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是______________ ,甲基麦芽酚中,与 形成配位键的原子是
形成配位键的原子是________ 。
(1)基态Ga原子的价层电子的轨道表示式是
(2)
 在270°C左右以二聚体
在270°C左右以二聚体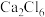 存在,结构式如图。
存在,结构式如图。
①
 可以形成二聚体的原因是
可以形成二聚体的原因是②
 和
和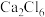 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是③
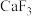 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,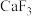 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因(3)
 可与
可与 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是 形成配位键的原子是
形成配位键的原子是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】实验室用氨法浸出氧化锌烟尘制备活性ZnO,其主要实验流程如下:
(1)浸出。用一定浓度的氨水和 配成的混合液浸取氧化锌烟尘,得到锌氨
配成的混合液浸取氧化锌烟尘,得到锌氨 浸出液。
浸出液。
①烟尘中的主要成分ZnO发生反应的化学方程式为___________ 。
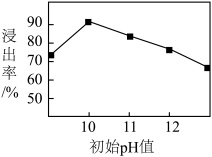
②锌元素的浸出率随浸出液初始pH的变化关系如图所示,当浸出液初始pH大于10时,浸出率随pH增大而减小的原因是___________ 。
(2)除杂。 、
、 等杂质也与氨水形成配合物存在于浸出后的滤液中,加入Zn粉可将它们置换除去。写出Zn粉和铜氨配合物反应的离子方程式
等杂质也与氨水形成配合物存在于浸出后的滤液中,加入Zn粉可将它们置换除去。写出Zn粉和铜氨配合物反应的离子方程式___________ 。
(3)蒸氨。加热时溶液中过量的氨和铵被蒸出,锌氨配合物最终以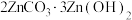 沉淀形式从溶液中析出。该过程需保持恒温80℃,可采取的加热方式为
沉淀形式从溶液中析出。该过程需保持恒温80℃,可采取的加热方式为___________ 。
(4)焙解。已知 和
和 的分解温度分别为125℃、300℃。实验室加热碱式碳酸锌
的分解温度分别为125℃、300℃。实验室加热碱式碳酸锌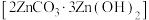 时测得的固体残留率随温度的变化关系如图所示。
时测得的固体残留率随温度的变化关系如图所示。
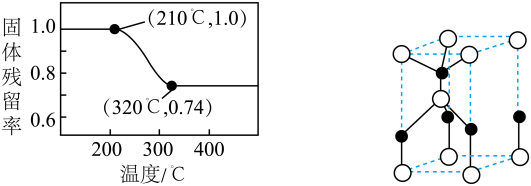
①275℃时,碱式碳酸锌分解产生的气态物质为___________ (填化学式)。
②经焙解得到的活性ZnO晶胞结构如图所示。该晶胞中Zn原子的配位数为___________ 。
(1)浸出。用一定浓度的氨水和
 配成的混合液浸取氧化锌烟尘,得到锌氨
配成的混合液浸取氧化锌烟尘,得到锌氨 浸出液。
浸出液。①烟尘中的主要成分ZnO发生反应的化学方程式为
②锌元素的浸出率随浸出液初始pH的变化关系如图所示,当浸出液初始pH大于10时,浸出率随pH增大而减小的原因是

(2)除杂。
 、
、 等杂质也与氨水形成配合物存在于浸出后的滤液中,加入Zn粉可将它们置换除去。写出Zn粉和铜氨配合物反应的离子方程式
等杂质也与氨水形成配合物存在于浸出后的滤液中,加入Zn粉可将它们置换除去。写出Zn粉和铜氨配合物反应的离子方程式(3)蒸氨。加热时溶液中过量的氨和铵被蒸出,锌氨配合物最终以
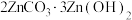 沉淀形式从溶液中析出。该过程需保持恒温80℃,可采取的加热方式为
沉淀形式从溶液中析出。该过程需保持恒温80℃,可采取的加热方式为(4)焙解。已知
 和
和 的分解温度分别为125℃、300℃。实验室加热碱式碳酸锌
的分解温度分别为125℃、300℃。实验室加热碱式碳酸锌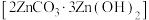 时测得的固体残留率随温度的变化关系如图所示。
时测得的固体残留率随温度的变化关系如图所示。
①275℃时,碱式碳酸锌分解产生的气态物质为
②经焙解得到的活性ZnO晶胞结构如图所示。该晶胞中Zn原子的配位数为
您最近一年使用:0次

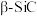 的晶胞结构如图所示,若碳和硅的原子半径分别为apm和bpm,密度为
的晶胞结构如图所示,若碳和硅的原子半径分别为apm和bpm,密度为 ,其原子的空间利用率(即晶胞中原子体积占空间体积的百分率)为
,其原子的空间利用率(即晶胞中原子体积占空间体积的百分率)为 ,
,