法国一家公司研发出一种比锂电池成本更低、寿命更长、充电速度更快的钠离子电池,该电池的负极材料为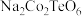 (制备原料为
(制备原料为 、
、 和
和 ),电解液为
),电解液为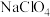 的碳酸丙烯酯溶液。回答下列问题:
的碳酸丙烯酯溶液。回答下列问题:
(1)基态Na原子中,核外电子占据的原子轨道总数为_______ ,Te属于元素周期表中_______ 区元素,其基态原子的价电子排布式为_______ 。
(2) 的空间结构为
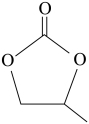
的空间结构为_______ ,碳酸丙烯酯的结构简式如图所示,其中碳原子的杂化轨道类型为_______ ,1mol碳酸丙烯酯中 键的数目为
键的数目为_______ 。
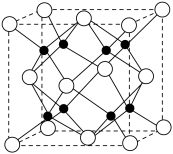
(3)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为_______ ,该晶胞的密度为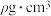 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为_______ cm(用含有 、
、 的代数式表示)。
的代数式表示)。
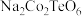 (制备原料为
(制备原料为 、
、 和
和 ),电解液为
),电解液为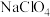 的碳酸丙烯酯溶液。回答下列问题:
的碳酸丙烯酯溶液。回答下列问题:(1)基态Na原子中,核外电子占据的原子轨道总数为
(2)
 的空间结构为
的空间结构为 键的数目为
键的数目为
(3)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为
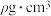 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为 、
、 的代数式表示)。
的代数式表示)。
更新时间:2022-06-29 08:33:45
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】原子序数依次增大的四种元素A、B、C、D分别处于第1~4周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是____ (填元素符号,下同),第一电离能最小的是____ 。
(2)C所在的主族元素气态氢化物中,沸点最低的是____ (填化学式)。
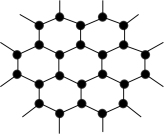
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为____ 。
(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是____ (填选项序号)。

①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
D单质 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:____ 。
(1)这四种元素中电负性最大的是
(2)C所在的主族元素气态氢化物中,沸点最低的是
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为

(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是

①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
D单质
 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀请书写第⑤步反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】ⅤA族元素及其化合物在材料等方面有重要用途。根据所学知识回答下列问题:
(1)基态砷原子处于最高能级的电子云轮廓图为_______ 形。
(2) 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是_______ 。
(3)叠氮化钠( )用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(
)用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸( ),叠氮酸中3个氮原子的杂化类型分别为
),叠氮酸中3个氮原子的杂化类型分别为_______ (不分先后)。
(4)N原子之间可以形成π键,而 原子之间较难形成π键。从原子结构角度分析,其原因为
原子之间较难形成π键。从原子结构角度分析,其原因为_______ 。
(5)往硫酸铜溶液中加入过量氨水,可生成配离子 。已知
。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是_______ 。
(6)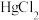 和不同浓度
和不同浓度 反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个
反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个 原子均处于小立方体的面心)
原子均处于小立方体的面心)
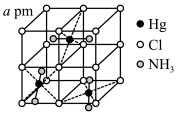
写出该含汞化合物的化学式:_______ 。则该晶体的密度
_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
(1)基态砷原子处于最高能级的电子云轮廓图为
(2)
 、
、 、
、 是同主族元素的氢化物,其中键角最小的是
是同主族元素的氢化物,其中键角最小的是(3)叠氮化钠(
 )用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(
)用于汽车的安全气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸( ),叠氮酸中3个氮原子的杂化类型分别为
),叠氮酸中3个氮原子的杂化类型分别为(4)N原子之间可以形成π键,而
 原子之间较难形成π键。从原子结构角度分析,其原因为
原子之间较难形成π键。从原子结构角度分析,其原因为(5)往硫酸铜溶液中加入过量氨水,可生成配离子
 。已知
。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子,其原因是
形成配离子,其原因是(6)
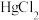 和不同浓度
和不同浓度 反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个
反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个 原子均处于小立方体的面心)
原子均处于小立方体的面心)
写出该含汞化合物的化学式:

 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Z在元素周期表中的位置 _______________________ ,Z的氢化物空间构型是________
(2)在H—Y、H—Z两种共价键中,键的极性较强的是____________ (用相应的元素符号表示该共价键)。
(3)XZ2分子中X以________ 方式杂化。
(4)写出W元素的原子核外电子排布式___________________________________ 。
(5)Y元素和Na形成晶体的部分结构可用下图中的_________ 来表示(填序号)。
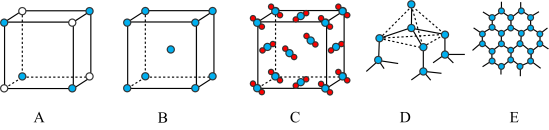
| 元素 | 相关信息 |
| X | X的价电子排布式为nsnnpn |
| Y | Y的负一价离子的电子层结构都与氩相同 |
| Z | 常温常压下,Z单质是淡黄色固体,常在火山口附近沉积 |
| W | W原子共有6个价电子,其中五个价电子位于第三能层d轨道 |
(2)在H—Y、H—Z两种共价键中,键的极性较强的是
(3)XZ2分子中X以
(4)写出W元素的原子核外电子排布式
(5)Y元素和Na形成晶体的部分结构可用下图中的

您最近一年使用:0次
【推荐1】五种短周期元素A、B、C、D、E原子序数逐渐增大。A和B在同一周期,A是同周期元素中半径最大的(不包含稀有气体);B原子的次外层电子数是最外层电子数的4倍;C是同周期简单离子中半径最小的元素;D元素原子的p轨道有3个未成对电子;E原子的K、L层电子数之和比K、M层电子数之和多1个。
(1)写出E元素基态原子的外围电子排布式____________
(2)比较第一电离能的大小:B_______ C(填大于、小于或等于)
(3)分别写出D、E的最高价氧化物对应水化物的化学式_______ 、________ ,并比较二者酸性(或碱性)的强弱_______ (填大于、小于或等于)
(4)写出B的最高价氧化物对应水化物与E的最高价氧化物对应水化物反应的离子方程式_______________________________
(5)写出C的最高价氧化物对应水化物与A的最高价氧化物对应水化物反应的化学方程式_____________
(1)写出E元素基态原子的外围电子排布式
(2)比较第一电离能的大小:B
(3)分别写出D、E的最高价氧化物对应水化物的化学式
(4)写出B的最高价氧化物对应水化物与E的最高价氧化物对应水化物反应的离子方程式
(5)写出C的最高价氧化物对应水化物与A的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式_______ ,C、O、Si三种元素的电负性由大到小的顺序为_______ 。C、N、O三种元素的第一电离能由大到小的顺序为_______ 。
(2)基态铬原子和基态锰原子中第一电离能较大的是_______ (填元素符号),原因为_______ 。
(3)SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为_______ 。
(4)氧化物XO的电子总数与SiC的相等,则X为_______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是_______ 。
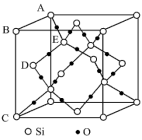
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含_______ 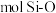 键。
键。
(1)写出Si的基态原子核外最外层电子排布式
(2)基态铬原子和基态锰原子中第一电离能较大的是
(3)SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为
(4)氧化物XO的电子总数与SiC的相等,则X为

(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含
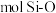 键。
键。
您最近一年使用:0次
【推荐3】前四周期元素 、
、 、
、 、
、 、
、 原子序数依次增大,其相关性质如下表所示:
原子序数依次增大,其相关性质如下表所示:
请根据以上信息,回答问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为______ ,其基态原子的最高能级的电子云轮廓图的形状为______ 。
(2) 和
和 的第一电离能
的第一电离能
______  (填“>”或“<”),其原因是
(填“>”或“<”),其原因是______ 。
(3) 、
、 、
、 、
、 四种元素的简单离子的半径由大到小的顺序为
四种元素的简单离子的半径由大到小的顺序为______ (用具体离子符号表示)。
(4) 和
和 可形成一种同时含有共价键和离子键的化合物,写出此化合物与水反应的化学方程式
可形成一种同时含有共价键和离子键的化合物,写出此化合物与水反应的化学方程式______ 。
(5) 元素位于元素周期表的
元素位于元素周期表的______ 区,其基态原子核外有______ 种运动状态不同的电子,该元素基态原子的价电子排布图为______ 。
 、
、 、
、 、
、 、
、 原子序数依次增大,其相关性质如下表所示:
原子序数依次增大,其相关性质如下表所示:
| 基态原子 能级电子半充满 能级电子半充满 |
| 与 同周期,且原子核外有2个未成对电子 同周期,且原子核外有2个未成对电子 |
| 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子 |
| 其基态原子外围电子排布式为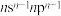 |
| 前四周期元素中, 元素基态原子未成对电子数最多 元素基态原子未成对电子数最多 |
(1)
 元素在周期表中的位置为
元素在周期表中的位置为(2)
 和
和 的第一电离能
的第一电离能
 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是(3)
 、
、 、
、 、
、 四种元素的简单离子的半径由大到小的顺序为
四种元素的简单离子的半径由大到小的顺序为(4)
 和
和 可形成一种同时含有共价键和离子键的化合物,写出此化合物与水反应的化学方程式
可形成一种同时含有共价键和离子键的化合物,写出此化合物与水反应的化学方程式(5)
 元素位于元素周期表的
元素位于元素周期表的
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】治疗疟疾的有效药物青蒿素是白色针状晶体,受热不稳定,易溶于乙醇和乙醚;乙醚( )的沸点小于乙醇的。按要求回答下列问题。
)的沸点小于乙醇的。按要求回答下列问题。
(1)青蒿素的提取:
①萃取剂选用乙醚( )而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是
)而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是_____ 。
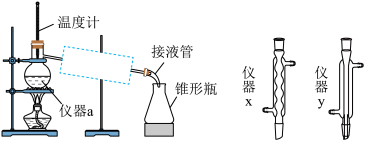
②将粗品蒸馏所用装置如图所示,虚线框内应选用右侧的仪器_____ (填“x”或“y”)。
(2)青蒿素的分子式的确定
①经元素分析,得知其分子中含有C、H、O三种元素,其中电负性最最大的是_________ 。
②经测定得知其相对分子质量为282,所用物理方法名称是_________ 。
(3)青蒿素的分子结构的确定
①用红外光线照射青蒿素分子,是为获得其__________________ 信息。
②通过晶体X射线衍射实验,获得其晶胞的类型和大小、原子的种类和数目等信息,可计算出原子间的距离,判断出晶体中哪些原子间存在化学键,进而确定键参数如_________ 、_________ ,得出该分子的空间结构及其晶胞(长方体,棱长分别为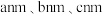 ,含4个青蒿素分子),如图甲所示。
,含4个青蒿素分子),如图甲所示。
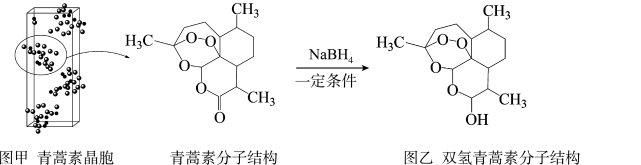
③晶体的密度为_________  (阿伏伽德罗常数的值设为
(阿伏伽德罗常数的值设为 ;列出表达式)。
;列出表达式)。
(4)青蒿素结构的修饰:一定条件下,用 将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
①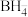 的中心原子的VSEPR模型名称为
的中心原子的VSEPR模型名称为_________ 。
②青蒿素结构修饰过程中,杂化轨道发生变化的碳原子的杂化方式变为_________ ,对应的官能团转变为_________ 。
 )的沸点小于乙醇的。按要求回答下列问题。
)的沸点小于乙醇的。按要求回答下列问题。(1)青蒿素的提取:
①萃取剂选用乙醚(
 )而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是
)而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是②将粗品蒸馏所用装置如图所示,虚线框内应选用右侧的仪器

(2)青蒿素的分子式的确定
①经元素分析,得知其分子中含有C、H、O三种元素,其中电负性最最大的是
②经测定得知其相对分子质量为282,所用物理方法名称是
(3)青蒿素的分子结构的确定
①用红外光线照射青蒿素分子,是为获得其
②通过晶体X射线衍射实验,获得其晶胞的类型和大小、原子的种类和数目等信息,可计算出原子间的距离,判断出晶体中哪些原子间存在化学键,进而确定键参数如
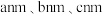 ,含4个青蒿素分子),如图甲所示。
,含4个青蒿素分子),如图甲所示。
③晶体的密度为
 (阿伏伽德罗常数的值设为
(阿伏伽德罗常数的值设为 ;列出表达式)。
;列出表达式)。(4)青蒿素结构的修饰:一定条件下,用
 将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。①
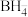 的中心原子的VSEPR模型名称为
的中心原子的VSEPR模型名称为②青蒿素结构修饰过程中,杂化轨道发生变化的碳原子的杂化方式变为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】催化剂的研究一直是一个重要的领域。根据所学知识,回答下列问题:
Ⅰ.铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有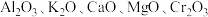 等氧化物中的几种。
等氧化物中的几种。
(1)基态氧原子中,核外电子有___________ 种空间运动状态,能量最高的电子的电子云在空间有___________ 个伸展方向。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,
”表示, 即即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为
即即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为___________ 。
Ⅱ.我国科研人员研制出了 (M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度、压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度、压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。
(3)Mn在元素周期表中位于___________ 区。
(4)第三电离能:
___________ (填“>”或“<”)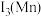 ,原因是
,原因是___________ 。
(5) 可作为氨选择性催化还原法脱除
可作为氨选择性催化还原法脱除 的催化剂。
的催化剂。 可由
可由 与
与 反应制得。
反应制得。 的结构如图。
的结构如图。
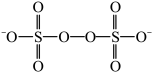
① 中
中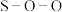
___________ (填“是”或“不是”)在一条直线上。
② 中的
中的 比
比 中的更
中的更___________ (填“难”或“易”)断裂。
Ⅲ.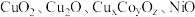 是常见的无机非贵金属光催化剂等。
是常见的无机非贵金属光催化剂等。
(6)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则其中绿色对应的辐射波长为___________ (填标号)。
A.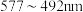 B.
B.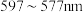 C.
C.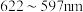
Ⅰ.铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
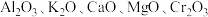 等氧化物中的几种。
等氧化物中的几种。(1)基态氧原子中,核外电子有
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,
”表示, 即即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为
即即称为电子的自旋磁量子数。对于基态的铁原子,其价层电子自旋磁量子数的代数和为Ⅱ.我国科研人员研制出了
 (M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度、压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度、压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。(3)Mn在元素周期表中位于
(4)第三电离能:

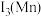 ,原因是
,原因是(5)
 可作为氨选择性催化还原法脱除
可作为氨选择性催化还原法脱除 的催化剂。
的催化剂。 可由
可由 与
与 反应制得。
反应制得。 的结构如图。
的结构如图。
①
 中
中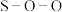
②
 中的
中的 比
比 中的更
中的更Ⅲ.
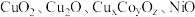 是常见的无机非贵金属光催化剂等。
是常见的无机非贵金属光催化剂等。(6)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则其中绿色对应的辐射波长为
A.
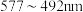 B.
B.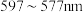 C.
C.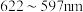
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】已知A、B、C、D、E、M是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是nsnnp2n;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。M是第四周期元素中未成对电子数最多的元素。
(1)请用元素符号完成下列空白。
①B、C、D、E四种元素中,简单离子半径最小的离子符号是___________ 。
②D、E两种元素的第一电离能___________ >___________ 。
(2)BC 的中心原子的价层电子对数为
的中心原子的价层电子对数为___________ ,VSEPR模型名称为___________ 。
(3)下表是A~M元素中某种元素的部分电离能,由此可判断该元素是___________ 。根据对角线规则,在短周期元素中,该元素的一些化学性质与元素___________ 的相似。
(4)某含M、Ca(钙)、O(氧)的化合物的立方晶胞如图所示。
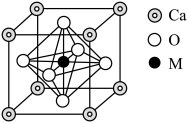
①M位于元素周期表的___________ 区,其基态原子的价层电子排布式为___________ 。
②该化合物的化学式是___________ 。
③Ca和M的最近距离为acm,晶体密度为ρg·cm-3.则阿伏加德罗常数(NA)为_______ mol-1(用代数式表示)。
(1)请用元素符号完成下列空白。
①B、C、D、E四种元素中,简单离子半径最小的离子符号是
②D、E两种元素的第一电离能
(2)BC
 的中心原子的价层电子对数为
的中心原子的价层电子对数为(3)下表是A~M元素中某种元素的部分电离能,由此可判断该元素是
| 某种元素 | 电离能I(kJ·mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 578 | 1817 | 2745 | 11575 | 14830 | |
(4)某含M、Ca(钙)、O(氧)的化合物的立方晶胞如图所示。

①M位于元素周期表的
②该化合物的化学式是
③Ca和M的最近距离为acm,晶体密度为ρg·cm-3.则阿伏加德罗常数(NA)为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
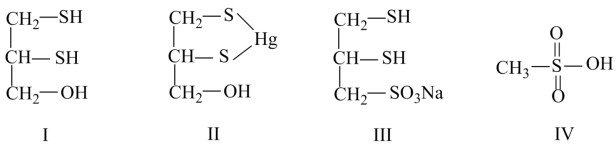
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等

A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】砷的一些化合物常用作半导体、除草剂、杀鼠药等。回答下列问题:
(1)基态As原子的核外电子排布式为[Ar]__________ ,有___________ 个未成对电子。
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是_____________ 。
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为____________ ,1mol 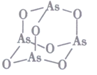 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为________ mol。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0, );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为_____________ 。
②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为____________ g·cm-3(列出计算式即可)。
(1)基态As原子的核外电子排布式为[Ar]
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为
 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0,
 );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】(1)2019年诺贝尔化学奖颁给了三位在锂电池领域做出突出贡献的科学家。
①基态锂原子核外有________ 种不同空间运动状态的电子。
②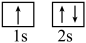 状态的锂到
状态的锂到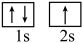 状态的锂所得的原子光谱是
状态的锂所得的原子光谱是________ 光谱。
③锂和铍相比,锂的第Ⅱ电离能________ (填“>”“<”或“=”)铍的第Ⅱ电离能。
(2)某锂离子电池的正极材料为 。
。
①基态 原子价层电子的电子排布图(轨道表达式)是
原子价层电子的电子排布图(轨道表达式)是________ 。
②磷元素是生物体不可缺少的元素之一,把一种填有 的苏打石灰玻璃移植到体内,钙离子和磷酸根离子在玻璃和骨头的间隙中溶出,有助于诱导新的骨骼生成。
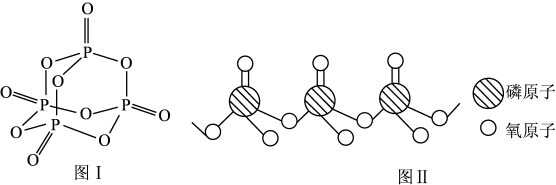
的苏打石灰玻璃移植到体内,钙离子和磷酸根离子在玻璃和骨头的间隙中溶出,有助于诱导新的骨骼生成。 的结构如图I所示,其中
的结构如图I所示,其中 原子的杂化方式是
原子的杂化方式是________ , 是
是________ (填“极性”或“非极性”)分子。
③ 原子形成的含氧酸有很多种结构,图Ⅱ是某种多聚磷酸根的结构示意图。这种多聚磷酸的化学式为
原子形成的含氧酸有很多种结构,图Ⅱ是某种多聚磷酸根的结构示意图。这种多聚磷酸的化学式为________ (用 表示磷原子的个数)。
表示磷原子的个数)。
(3)某锂电池负极材料晶体中 嵌入两层石墨层中导致石墨堆积方式发生改变,形成如图Ⅲ所示的晶体结构。
嵌入两层石墨层中导致石墨堆积方式发生改变,形成如图Ⅲ所示的晶体结构。

①石墨是一种导体,但石墨的导电性只能沿石墨平面的方向,原因是________ 。
②已知最近碳一碳原子间的距离是 ,则最近锂一锂离子间的距离是
,则最近锂一锂离子间的距离是________  ;石墨层之间的距离是
;石墨层之间的距离是 (其中
(其中 ),
), 表示阿伏加 德罗常数的值,该晶体的密度是
表示阿伏加 德罗常数的值,该晶体的密度是________  (列出计算式即可)。
(列出计算式即可)。
①基态锂原子核外有
②
 状态的锂到
状态的锂到 状态的锂所得的原子光谱是
状态的锂所得的原子光谱是③锂和铍相比,锂的第Ⅱ电离能
(2)某锂离子电池的正极材料为
 。
。①基态
 原子价层电子的电子排布图(轨道表达式)是
原子价层电子的电子排布图(轨道表达式)是②磷元素是生物体不可缺少的元素之一,把一种填有
 的苏打石灰玻璃移植到体内,钙离子和磷酸根离子在玻璃和骨头的间隙中溶出,有助于诱导新的骨骼生成。
的苏打石灰玻璃移植到体内,钙离子和磷酸根离子在玻璃和骨头的间隙中溶出,有助于诱导新的骨骼生成。 的结构如图I所示,其中
的结构如图I所示,其中 原子的杂化方式是
原子的杂化方式是 是
是③
 原子形成的含氧酸有很多种结构,图Ⅱ是某种多聚磷酸根的结构示意图。这种多聚磷酸的化学式为
原子形成的含氧酸有很多种结构,图Ⅱ是某种多聚磷酸根的结构示意图。这种多聚磷酸的化学式为 表示磷原子的个数)。
表示磷原子的个数)。
(3)某锂电池负极材料晶体中
 嵌入两层石墨层中导致石墨堆积方式发生改变,形成如图Ⅲ所示的晶体结构。
嵌入两层石墨层中导致石墨堆积方式发生改变,形成如图Ⅲ所示的晶体结构。
①石墨是一种导体,但石墨的导电性只能沿石墨平面的方向,原因是
②已知最近碳一碳原子间的距离是
 ,则最近锂一锂离子间的距离是
,则最近锂一锂离子间的距离是 ;石墨层之间的距离是
;石墨层之间的距离是 (其中
(其中 ),
), 表示阿伏加 德罗常数的值,该晶体的密度是
表示阿伏加 德罗常数的值,该晶体的密度是 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次



