下面是一些晶体的结构示意图。
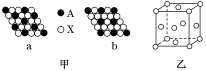
(1)下列关于晶体的说法正确的是___________(填字母)。
(2)图甲表示的是晶体的二维平面示意图,a、b中可表示化学式为AX3的化合物的是___________ (填“a”或“b”)。
(3)图乙表示的是金属铜的晶胞。
①该晶胞“实际”拥有的铜原子数是___________ ,铜原子的配位数为___________ 。
②该晶胞称为___________ (填字母)。
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
(4)NiO、FeO的晶体结构相同,且r(Fe2+)>r(Ni2+),NiO的熔点为1 960 ℃,则FeO的熔点___________ (填“>”或“<”)1 960 ℃,判断的依据是___________ 。

(1)下列关于晶体的说法正确的是___________(填字母)。
| A.晶体的形成与晶体的自范性有关 |
| B.可以用X射线衍射仪区分晶体和非晶体 |
| C.石蜡是非晶体,但有固定的熔点 |
| D.晶胞就是晶体 |
(3)图乙表示的是金属铜的晶胞。
①该晶胞“实际”拥有的铜原子数是
②该晶胞称为
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
(4)NiO、FeO的晶体结构相同,且r(Fe2+)>r(Ni2+),NiO的熔点为1 960 ℃,则FeO的熔点
2021高三·全国·专题练习 查看更多[1]
(已下线)第32讲 晶体结构与性质(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
更新时间:2021-12-06 14:24:46
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】原子序数小于等于36的Q、W、X、Y、Z五种元素,它们的原子序数依次增大,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含未成对电子数均为2,Z的基态原子核外电子有26种运动状态。回答下列问题(涉及元素时用对应的元素符号表示):
(1)Z的基态原子的电子排布式___________ ;从结构角度来看,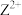 易被氧化成
易被氧化成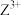 的原因是
的原因是___________ 。
(2)化合物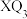 的沸点比化合物
的沸点比化合物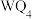 的高,其主要原因是
的高,其主要原因是___________ 。
(3)1molQWX与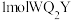 所含
所含 键数目之比为
键数目之比为___________ 。
(4)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为___________ 。
②预测该化合物熔点应___________ (填“高于”或“低于”)金刚石,理由是___________ 。
(5)写出少量Z单质和X的最高价氧化物的水化物的稀溶液反应的离子方程式:___________ 。
(1)Z的基态原子的电子排布式
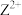 易被氧化成
易被氧化成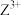 的原因是
的原因是(2)化合物
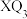 的沸点比化合物
的沸点比化合物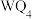 的高,其主要原因是
的高,其主要原因是(3)1molQWX与
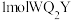 所含
所含 键数目之比为
键数目之比为(4)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为
②预测该化合物熔点应
(5)写出少量Z单质和X的最高价氧化物的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的; F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(注:A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(2)B的氯化物的熔点比MgO的熔点___________ (填“高”或“低”)。
(3)F的外围电子排布式是___________ 。
(4)A、F形成某种化合物的晶胞结构如图所示(其中A显−3价),则其化学式为___________ (每个球均表示1个原子)。
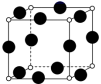
(5)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为___________ 。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点比MgO的熔点
(3)F的外围电子排布式是
(4)A、F形成某种化合物的晶胞结构如图所示(其中A显−3价),则其化学式为

(5)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】X、Y、Z、W、Q是前四周期元素且原子序数依次增大。X的基态原子核外有8种运动状态不同的电子,Y的基态原子的逐级电离能如图1所示,Z的电负性在同周期元素中最大,W是第26号元素,Q是同周期主族元素中未成对电子最多的元素。
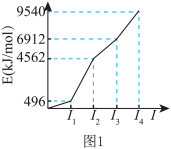
(1)W在周期表中的位置是_____ ,W2+的基态电子排布式为_____ 。
(2)Q的基态电子排布式为_____ 。QZ3的价层电子对互斥(VSEPR)模型名称为_____ 。
(3)与X同周期且第一电离能大于X的元素有_____ (填对应元素的符号,下同)。
(4)如图2是某晶体的晶胞结构(W和Q均位于晶胞内部),该晶体的化学式为_____ 。
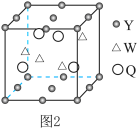

(1)W在周期表中的位置是
(2)Q的基态电子排布式为
(3)与X同周期且第一电离能大于X的元素有
(4)如图2是某晶体的晶胞结构(W和Q均位于晶胞内部),该晶体的化学式为

您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】I.乙烯是重要有机化工原料,以乙烯为原料合成部分化工产品的流程如下(部分反应条件略去)。
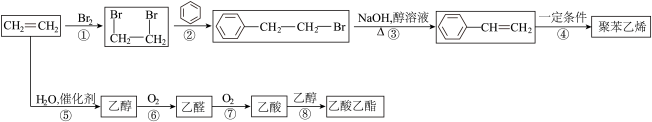
回答下列问题:
(1)乙酸的官能团的名称是___________ 。
(2)反应②的反应类型是___________ 。
(3)聚苯乙烯的结构简式为___________ 。
(4)反应⑧的化学方程式为___________ 。
Ⅱ.回答以下问题。
(5)基态Cu原子的核外电子排布式为___________ 。
(6)NH3的空间结构是___________ 。
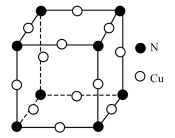
(7)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为apm,则该晶体的密度是___________ g·cm-3。

回答下列问题:
(1)乙酸的官能团的名称是
(2)反应②的反应类型是
(3)聚苯乙烯的结构简式为
(4)反应⑧的化学方程式为
Ⅱ.回答以下问题。
(5)基态Cu原子的核外电子排布式为
(6)NH3的空间结构是
(7)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为apm,则该晶体的密度是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供_______ ,配位原子是_______ ,1 mol [Cu(H2O)4]2+中σ键的数目为_________ 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式_______________ ,再向溶液中加入乙醇,会析出深蓝色晶体____________ (写出化学式)。
(3)“中国蓝”“中国紫”中存在 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为_______ 。
(4)BaO的熔沸点_____ MgO(填“>”“<”“=”),原因是______________ 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为_______ 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为___________ g·cm-3。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式
(3)“中国蓝”“中国紫”中存在
 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为(4)BaO的熔沸点
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)下列说法正确的是___________。
(2)ClO2中心原子为Cl,Cl2O中心原子为O,二者均为V形结构,但ClO2中存在大π键(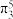 ),ClO2中Cl原子的轨道杂化方式
),ClO2中Cl原子的轨道杂化方式___________ ;O-Cl-O键角___________ Cl-O-Cl键角(填“>”“<”或“=”)。比较ClO2与Cl2O中Cl-O键的键长并说明原因___________ 。
(3)470K时,F2与Cl2反应生成ClF,常温常压下,ClF为无色气体,固态ClF的晶体类型为___________ 。
(4)一定条件下,CuCl2、K和F2反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图所示(晶胞参数 ,
,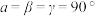 ),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为
),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为___________ 。与Cu原子距离最近的F原子的数目为___________ ,若该化合物的密度为 ,则阿伏加徳罗常数的值NA=
,则阿伏加徳罗常数的值NA=___________ (用含 、a、c的代数式表示。
、a、c的代数式表示。
(1)下列说法正确的是___________。
A.能量最低的激发态F原子的电子排布图为: |
| B.化学键中离子键成分的百分数:CaF2>LiF>NaF |
| C.HF的沸点比H2O低是因为HF氢键的键能小于H2O |
| D.已知N—F键的极性比N—H的极性强,因此NF3分子的极性比NH3的极性弱 |
(2)ClO2中心原子为Cl,Cl2O中心原子为O,二者均为V形结构,但ClO2中存在大π键(
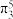 ),ClO2中Cl原子的轨道杂化方式
),ClO2中Cl原子的轨道杂化方式(3)470K时,F2与Cl2反应生成ClF,常温常压下,ClF为无色气体,固态ClF的晶体类型为
(4)一定条件下,CuCl2、K和F2反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图所示(晶胞参数
 ,
,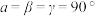 ),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为
),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为 ,则阿伏加徳罗常数的值NA=
,则阿伏加徳罗常数的值NA= 、a、c的代数式表示。
、a、c的代数式表示。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】有 A、B、C三种短周期元素。A-离子的电子层结构和氖原子相同;短周期元素中B的金属性最强;C的原子核内质子数是B的次外层电子数的2倍。试推断:
⑴. A元素的名称是______ 、B在周期表的位置表示为___________________ 、C的原子结构示意图为______________ ;
⑵. B的氢氧化物的电子式是____________ ;其晶体类型是_________ ,晶体中存在的化学键有________
⑶.C元素的最高价氧化物对应水化物与铜反应的化学方程式为:_____________________ 。
⑴. A元素的名称是
⑵. B的氢氧化物的电子式是
⑶.C元素的最高价氧化物对应水化物与铜反应的化学方程式为:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】根据晶体的微观结构,试回答有关问题:
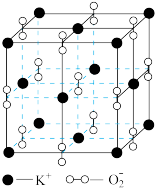
(1)高温下,超氧化钾(KO2)晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。下图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,K+的配位数为_______ ,0价氧原子与-2价氧原子的数目比为_______ 。
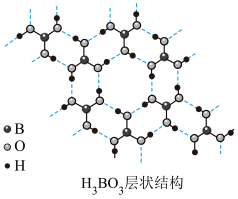
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的有_______ 。
①硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1 mol H3BO3的晶体中有3 mol氢键
⑤含1 mol H3BO3的晶体中有6 mol极性共价键
(3)确定该合金(如图)的化学式为_____ ,与Fe原子等距离且最短的Fe原子个数为____ ,若晶胞的边长为a nm,此合金的密度为_____ g·cm-3。

(1)高温下,超氧化钾(KO2)晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。下图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,K+的配位数为

(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的有

①硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1 mol H3BO3的晶体中有3 mol氢键
⑤含1 mol H3BO3的晶体中有6 mol极性共价键
(3)确定该合金(如图)的化学式为

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
(1)AY2是一种常用的溶剂,为_____________ 分子(填“极性”或“非极性”),分子中存在___________ 个σ键。
(2)X形成的单质与NaOH溶液反应的离子方程式为______________________________ ,超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于____ 晶体。
(3)X、氧、B元素的电负性由大到小的顺序为_______________ (用元素符号作答)。
(4)Z的基态原子核外电子排布式为___________________________ 。
(1)AY2是一种常用的溶剂,为
(2)X形成的单质与NaOH溶液反应的离子方程式为
(3)X、氧、B元素的电负性由大到小的顺序为
(4)Z的基态原子核外电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】回答下列小题:
(1)在四水合铜离子 中,配体是
中,配体是______ ;配位数是______ ;配位原子是______ ;该微粒中存在的化学键有______ 。
(2)有同学书写基态碳原子的核外电子排布图为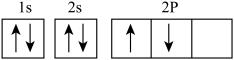 ,这样的书写不正确,违背了
,这样的书写不正确,违背了______ 。
(3) 是一种无色液体,沸点为43℃,熔点为
是一种无色液体,沸点为43℃,熔点为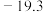 ℃,
℃, 的晶体类型是
的晶体类型是______ 。
(4)氧化物MgO是优良的耐高温材料,其晶体结构与NaCl晶体相似,MgO的熔点比CaO的高,其原因是______ 。
(5)金刚石、石墨、 都是碳的同素异形体
都是碳的同素异形体
①石墨晶体存在作用力有______ 。
② 的熔点比金刚石、石墨熔点低的原因是
的熔点比金刚石、石墨熔点低的原因是______ 。
③石墨中碳原子的杂化轨道类型为______ ;碳原子和碳碳键的个数比是______ 。
(1)在四水合铜离子
 中,配体是
中,配体是(2)有同学书写基态碳原子的核外电子排布图为
 ,这样的书写不正确,违背了
,这样的书写不正确,违背了(3)
 是一种无色液体,沸点为43℃,熔点为
是一种无色液体,沸点为43℃,熔点为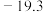 ℃,
℃, 的晶体类型是
的晶体类型是(4)氧化物MgO是优良的耐高温材料,其晶体结构与NaCl晶体相似,MgO的熔点比CaO的高,其原因是
(5)金刚石、石墨、
 都是碳的同素异形体
都是碳的同素异形体①石墨晶体存在作用力有
②
 的熔点比金刚石、石墨熔点低的原因是
的熔点比金刚石、石墨熔点低的原因是③石墨中碳原子的杂化轨道类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题
(1)Na原子核外共有______ 种不同运动状态的电子,有_____ 种不同能量的电子。
(2)相同压强下,部分元素氟化物的熔点见下表:
试解释上表中氟化物熔点差异的原因:_______ 。
(3)SiF4分子的空间构型为_______ 。
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因__________ 。
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数__________ 。
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
(1)Na原子核外共有
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
(3)SiF4分子的空间构型为
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】锰单质及其化合物应用十分广泛。回答下列问题:
(1)基态锰原子的核外电子排布式为_______
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是_______ 。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为_______ (填元素符号)。
②写出一种与BH 互为等电子体的分子
互为等电子体的分子_______ 。
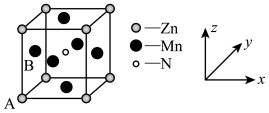
(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为_______ ;其中原子坐标参数A为(0,0,0),B为(0, ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为_______ 。
(5)金属锰有多种晶型,其中δ−Mn的结构为体心立方堆积,晶胞参数为apm,δ−Mn中锰的原子半径为_______ pm。已知阿伏加德罗常数的值为NA,δ−Mn的理论密度ρ=_______ g∙cm−3 (列出计算式)。
(1)基态锰原子的核外电子排布式为
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为
②写出一种与BH
 互为等电子体的分子
互为等电子体的分子(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为
 ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为
(5)金属锰有多种晶型,其中δ−Mn的结构为体心立方堆积,晶胞参数为apm,δ−Mn中锰的原子半径为
您最近一年使用:0次



