稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素.回答下列问题;
(1)钪(Sc)元素的原子核外电子排布式为_____________ 。钬(Ho)的基态原子电子排布式为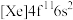 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为_________ 。
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是_____________ 。
几种稀土元素的电离能(单位:kJ/mol)
(3)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+ CH2=CH2;ICH2CH2I中碳原子杂化轨道类型为________ 。
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有___________ 。
(5)1molCH2=CH2中含有的 键数目为:
键数目为:____________ 。
(1)钪(Sc)元素的原子核外电子排布式为
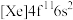 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是
几种稀土元素的电离能(单位:kJ/mol)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有
(5)1molCH2=CH2中含有的
 键数目为:
键数目为:
更新时间:2021-10-29 20:13:03
|
相似题推荐
【推荐1】法国一家公司研发出一种比锂电池成本更低、寿命更长、充电速度更快的钠离子电池,该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。回答下列问题:
(1)C、O、Cl三种元素电负性由大到小的顺序为_______ 。
(2)基态Na原子中,核外不同电子运动状态的数目为_______ ,Co属于元素周期表中_______ 区元素,其基态原子的价电子排布式为_______ 。
(3)碳酸丙烯酯的结构简式如图所示,其中碳原子的杂化轨道类型为_______ ,1mol碳酸丙烯酯中σ键的数目为_______ 。

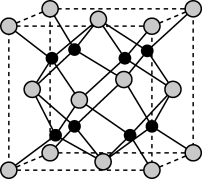
(4)Na和O形成的离子化合物的晶胞结构如图所示,已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则Na与O之间的最短距离为_______ cm(用含有ρ、NA的代数式表示)。
(1)C、O、Cl三种元素电负性由大到小的顺序为
(2)基态Na原子中,核外不同电子运动状态的数目为
(3)碳酸丙烯酯的结构简式如图所示,其中碳原子的杂化轨道类型为

(4)Na和O形成的离子化合物的晶胞结构如图所示,已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则Na与O之间的最短距离为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
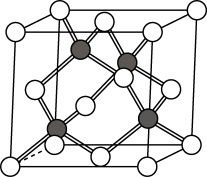
【推荐2】Ⅰ.金刚砂(SIC)是重要的工业制品,可由一以下反应制得: 。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
(1)X的化学式为___________
(2)写出基态Si原子的电子排布式___________ ,SiC中Si的化合价为___________
(3)SiC,金刚石,硅单质的熔点由高到低的顺序为___________
(4)X可与氧气反应生成Y,Y分子中中心原子的杂化类型为___________ ,键角为___________
Ⅱ. 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
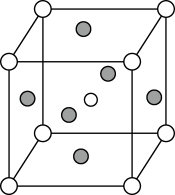
(5)与K原子紧邻的O原子有___________
(6)晶体中K原子与O原子的最短距离为___________ nm(保留三位小数)
 。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
。SiC的晶体结构与金刚石的相似,如图所示,其中C原子和Si原子的位置是交替的。回答下列问题。
(1)X的化学式为
(2)写出基态Si原子的电子排布式
(3)SiC,金刚石,硅单质的熔点由高到低的顺序为
(4)X可与氧气反应生成Y,Y分子中中心原子的杂化类型为
Ⅱ.
 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中K、I、O分别位于顶点、体心、面心位置,如图所示。
(5)与K原子紧邻的O原子有
(6)晶体中K原子与O原子的最短距离为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
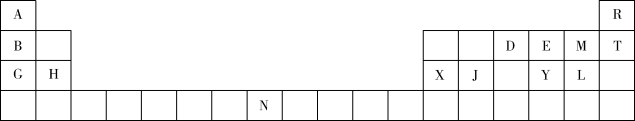
【推荐3】A、B、C、D、E是前四周期的元素。A、B、C同周期,C、D同主族且原子半径C>D,A的原子结构示意图为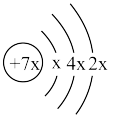 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
(1)写出下列元素的符号:A___________ 。
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是___________ ,碱性最强的是___________ 。
(3)E原子价电子排布式是___________ ;E元素在___________ 区。
(4)D元素的基态原子的电子排布图为___________ 。
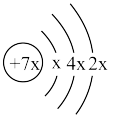 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)E原子价电子排布式是
(4)D元素的基态原子的电子排布图为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
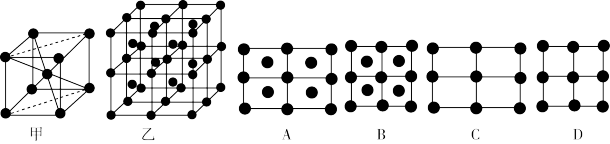
【推荐1】下图中A~D是中学化学教科书中常见的几种晶体结构模型:
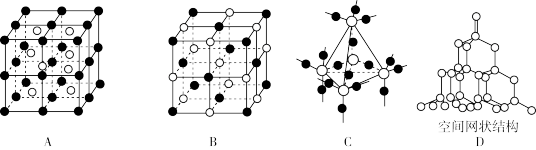
(1)请填写相应物质的名称:A___________ ;B.___________ ;C.___________ ;D.___________ 。
(2)铜元素位于元素周期表___________ 区。单质铜及镍都是由___________ 键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959 kJ∙mol−1,INi=1753 kJ∙mol−1,ICu>INi的原因是___________ 。
(3)单质铁的一种晶体如图甲、乙所示,若按甲虚线方向切乙得到的截面图是___________ (填字母序号)。

(1)请填写相应物质的名称:A
(2)铜元素位于元素周期表
(3)单质铁的一种晶体如图甲、乙所示,若按甲虚线方向切乙得到的截面图是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】亚铁氰化钾( )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。
(1)O元素位于___________ 区,基态O原子核外电子的空间运动状态有___________ 种。
(2)Fe在元素周期表中的位置___________ ,基态Fe原子的价电子轨道表示式为___________ 。
(3)黄血盐( )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是___________ , 该原子能量最高的电子所在能级符号为___________ 。
(4)亚铁氰化钾( )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为___________ 。
(5)普鲁士蓝( )中C的杂化方式为
)中C的杂化方式为___________ 。
 )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。(1)O元素位于
(2)Fe在元素周期表中的位置
(3)黄血盐(
 )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是(4)亚铁氰化钾(
 )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为(5)普鲁士蓝(
 )中C的杂化方式为
)中C的杂化方式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】硫、硒、碲的化合物在农药、石油工业、矿物开采、萃取及有机合成等领域的应用广泛。回答下列问题:
(1)基态Se原子的最高能级组的电子排布式为
(2)下列有关氧族元素单质及其化合物的性质说法正确的是_______。
A.氧族元素气态氢化物的稳定性按 、 、 、 、 、 、 的顺序依次减弱 的顺序依次减弱 |
B.其氢化物中的键长按 、 、 、 、 、 、 的顺序依次减小 的顺序依次减小 |
C.其阴离子的还原性按 、 、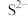 、 、 、 、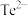 的顺序依次增强 的顺序依次增强 |
D.其最高价氧化物的水化物酸性按 、 、 、 、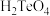 顺序依次增强 顺序依次增强 |
 分子结构式为
分子结构式为 中含有π键的数目为
中含有π键的数目为 结构有两种,已知硫氰酸(
结构有两种,已知硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是(4)
 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为
为 ,
, 为
为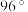 ,则
,则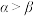 的原因主要是
的原因主要是
(5)二硒键和二硫键是重要的光响应动态共价键(在特定条件下断开并能复原的化学键),其光响应原理可用如图表示,已知光的波长与其能量成反比,则图中实现光响应的波长:

 ,(填“>”或“<”或“=”),其原因是
,(填“>”或“<”或“=”),其原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】氮族元素广泛应用于生产生活中,回答下列问题:
(1)异硫氰酸烯丙酯(CH2=CH−CH2−N=C=S)是芥末油的主要成分,分子中含有的σ键与π键个数比为_______ 。
(2)P与N同族,性质相似。N2很稳定的原因是能形成键能很大的氮氮三键。P不能形成类似单质的原因是_______ 。
(3)PC13和BC13键角前者_______ (填“大于”“小于”或“等于”)后者,原因是_______ 。
(4)如图所示,磷化硼晶体中磷原子作立方最密堆积,硼原子填入间隔的四面体空隙中。晶体中P的配位数是_______ 。已知晶胞中原子1的坐标为(0,0,0),原子2的坐标为(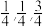 ),则原子3的坐标为
),则原子3的坐标为_______ 。磷化硼的密度为ρg·cm-3,阿伏加德罗常数的值为NA,计算晶体中硼原子和磷原子的核间距d=_______ pm。

(1)异硫氰酸烯丙酯(CH2=CH−CH2−N=C=S)是芥末油的主要成分,分子中含有的σ键与π键个数比为
(2)P与N同族,性质相似。N2很稳定的原因是能形成键能很大的氮氮三键。P不能形成类似单质的原因是
(3)PC13和BC13键角前者
(4)如图所示,磷化硼晶体中磷原子作立方最密堆积,硼原子填入间隔的四面体空隙中。晶体中P的配位数是
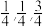 ),则原子3的坐标为
),则原子3的坐标为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】碳是形成单质和化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。
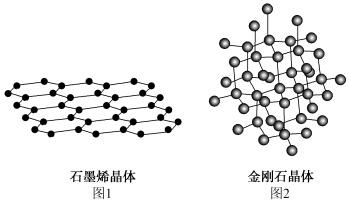
①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性_____ 。
②求出12g金刚石中含σ键数目为_____ 。
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有_____ 。
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目_____ 。
(3)CH 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为______ 。
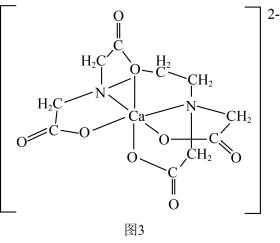
(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有______ 。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图1、图2所示。

①石墨烯是石墨分离出的单独一层,石墨烯非常稳定,属于厚度只有一个直径大小的“二维材料”,写出一个石墨烯所拥有的特性
②求出12g金刚石中含σ键数目为
(2)碳的主要氧化物有CO,能与金属Fe形成一种浅黄色液体Fe(CO)5,Fe(CO)5是配合物其熔点为−20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:
①该化合物的晶体中涉及的作用力有
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②算出1molFe(CO)5配合物中含有σ键数目
(3)CH
 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图3所示。配位体中碳原子的杂化方式有

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
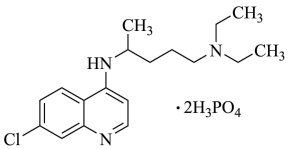
【推荐1】2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(2019-nCoV)的感染。
(1)已知磷酸氯喹的结构如图所示,则一个磷酸氯喹分子中含___________ 个 杂化的碳原子;分子中N原子的杂化方式为
杂化的碳原子;分子中N原子的杂化方式为___________ ;基态磷原子核外电子的空间运动状态有___________ 种。
(2) 与金刚石均为碳的单质,从结构与性质之间的关系解释
与金刚石均为碳的单质,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是___________ 。
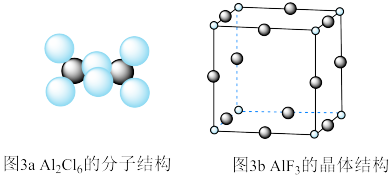
(3)气态 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为
的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为___________ 。 结构属立方晶系,晶胞如图3b所示,
结构属立方晶系,晶胞如图3b所示, 的配位数为
的配位数为___________ 。若晶胞参数为apm,晶体密度ρ=___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(4)吡啶(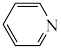 )分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是
)分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是___________ (填代号)。
a.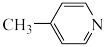 b.
b.  c.
c. 
(1)已知磷酸氯喹的结构如图所示,则一个磷酸氯喹分子中含
 杂化的碳原子;分子中N原子的杂化方式为
杂化的碳原子;分子中N原子的杂化方式为
(2)
 与金刚石均为碳的单质,从结构与性质之间的关系解释
与金刚石均为碳的单质,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是(3)气态
 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为
的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为 结构属立方晶系,晶胞如图3b所示,
结构属立方晶系,晶胞如图3b所示, 的配位数为
的配位数为 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(4)吡啶(
 )分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是
)分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是a.
 b.
b.  c.
c. 
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)1 mol CO2中含有的σ键数目为________ 。
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为________ 。HCN分子内σ键与π键数目之比为________ 。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被NH2(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ΔH=-1 038.7 kJ·mol-1,若该反应中有4 mol N—H键断裂,则形成的π键有________ mol。
(4)CH4、NH3、H2O、HF分子中,共价键的极性由强到弱的顺序是____________ 。
(1)1 mol CO2中含有的σ键数目为
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被NH2(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ΔH=-1 038.7 kJ·mol-1,若该反应中有4 mol N—H键断裂,则形成的π键有
(4)CH4、NH3、H2O、HF分子中,共价键的极性由强到弱的顺序是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等三十多种对人体有益的微量元素。
(1)基态Ge原子的价电子排布图为_______ 。
(2)Ni(CO)4常温下为无色液体,沸点42.1°C,熔点−19.3°C,难溶于水,易溶于有机溶剂。推测Ni(CO)4是_______ 分子(“极性”或“非性极”)。
(3)Co2+可与 形成配离子[Co(NO3)4]2−,该配离子中各元素的第一电离能由小到大的顺序为
形成配离子[Co(NO3)4]2−,该配离子中各元素的第一电离能由小到大的顺序为_______ (用元素符号表示), 中N的杂化方式为
中N的杂化方式为_______ 。
(4)氨气中H−N−H键的键角为107.3°,[Zn(NH3)6]2+离子中H−N−H键的键角_______ 107.3°(填“大于”“小于”或“等于”),原因是:_______ 。
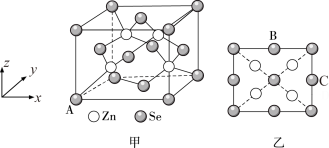
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,A点原子的坐标为(0,0,0),B点原子的坐标为( ,1,
,1, ),则C点原子的坐标为
),则C点原子的坐标为_______ ;已知晶胞边长为apm,阿伏加德罗常数的值为NA,该晶胞密度ρ为_______ g·cm-3(只列出计算式)。
(1)基态Ge原子的价电子排布图为
(2)Ni(CO)4常温下为无色液体,沸点42.1°C,熔点−19.3°C,难溶于水,易溶于有机溶剂。推测Ni(CO)4是
(3)Co2+可与
 形成配离子[Co(NO3)4]2−,该配离子中各元素的第一电离能由小到大的顺序为
形成配离子[Co(NO3)4]2−,该配离子中各元素的第一电离能由小到大的顺序为 中N的杂化方式为
中N的杂化方式为(4)氨气中H−N−H键的键角为107.3°,[Zn(NH3)6]2+离子中H−N−H键的键角
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,A点原子的坐标为(0,0,0),B点原子的坐标为(
 ,1,
,1, ),则C点原子的坐标为
),则C点原子的坐标为
您最近一年使用:0次

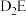 的沸点比
的沸点比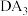 的沸点低,其原因是
的沸点低,其原因是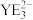 的键角比
的键角比 的键角小的原因是
的键角小的原因是

