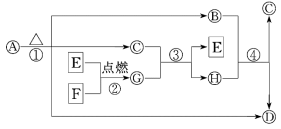
已知B为碱性氧化物,D为淡黄色固体粉末,F为医疗上治疗胃酸过多的一种药剂;物质的转化关系如图所示,请回答下列问题:

(1)请写出下列物质的化学式:A_____ 、F______ 。
(2)请写出下列反应的方程式:
①D→E(写化学方程式):_____ ;
②C→E(写在水溶液中进行的离子方程式):_____ 。
(3)将4.6gA投入47.8g水中,所得溶液中溶质的质量分数为______ (用百分数表示,保留一位小数)。若把A投入盛有CuSO4的溶液中,溶液中出现______ (填沉淀颜色)沉淀。

(1)请写出下列物质的化学式:A
(2)请写出下列反应的方程式:
①D→E(写化学方程式):
②C→E(写在水溶液中进行的离子方程式):
(3)将4.6gA投入47.8g水中,所得溶液中溶质的质量分数为
更新时间:2023-01-17 16:30:15
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】有A、B、C、D四种化合物,分别由K+、Ba2+、 SO 、 CO
、 CO 、OH-中的两种组成,它们具有下列性质
、OH-中的两种组成,它们具有下列性质
①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D的化学式。
A、______ ,B、______ ,C、______ ,D、______ 。
(2)写出下列反应的离子方程式。
B与盐酸反应:_______ ,E(少量)与澄清石灰水反应:______ 。
 、 CO
、 CO 、OH-中的两种组成,它们具有下列性质
、OH-中的两种组成,它们具有下列性质①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D的化学式。
A、
(2)写出下列反应的离子方程式。
B与盐酸反应:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A~L为中学化学常见物质,A为绿色矿石,C为实验室常用溶剂,D为金属氧化物,E为光合作用原料之一,F为二元强酸,K、H分别为固体单质,J为红色金属单质,I的水溶液呈浅绿色,它们之间的转化关系如图所示。
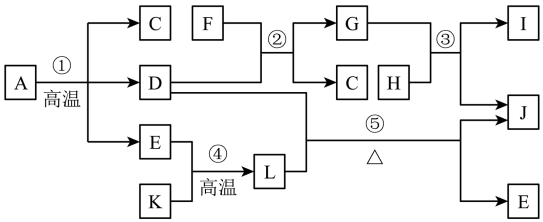
回答下列问题:
(1)A中主要成分的化学式为___ ,D的化学式为___ 。
(2)A—L物质中属于氧化物的有__ (填化学式,下同),属于盐的有___ 。
(3)反应②的离子方程式为__ 。
(4)写出反应⑤化学方程式并用单线桥法标明电子的转移:__ ,该反应现象为__ 。

回答下列问题:
(1)A中主要成分的化学式为
(2)A—L物质中属于氧化物的有
(3)反应②的离子方程式为
(4)写出反应⑤化学方程式并用单线桥法标明电子的转移:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】肼(N2H4) 是一种重要的工业产品,实验室用NH3与Cl2合成肼(N2H4) 并探究肼的性质。实验装置如图所示:
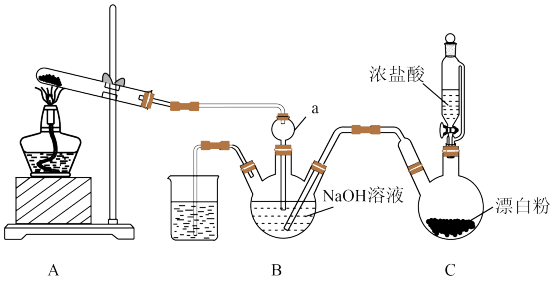
相关物质的性质如下:
回答下列问题:
(1)装置A试管中的试剂为_______ (填化学式)。仪器a的名称是_______ 。
(2)N2H4是_______ 分子(填“极性”或“非极性”)。
(3)装置B中制备肼的离子方程式为_______ ,该装置中通入NH3必须过量的原因是_______ 。
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是_______ 。
(5)①探究N2H4的性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元弱碱,肼与硫酸反应除能生成N2H6SO4外,还可能生成的盐为_______ 。(填化学式)。
②测定肼的质量分数。取装置B中的溶液3.2g,调节溶液pH为6.5左右,加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用c mol·L-1的碘溶液滴定(杂质不参与反应),滴定过程中有无色、无味、无毒气体产生。滴定终点平均消耗标准溶液20.00mL,产品中肼的质量分数为_______ %。

相关物质的性质如下:
| 性状 | 熔点/℃ | 沸点/℃ | 性质 | |
| N2H4 | 无色液体 | 1.4 | 113 | 与水混溶、强还原性 |
| N2H6SO4 | 无色晶体 | 254 | / | 微溶于冷水,易溶于热水 |
(1)装置A试管中的试剂为
(2)N2H4是
(3)装置B中制备肼的离子方程式为
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究N2H4的性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元弱碱,肼与硫酸反应除能生成N2H6SO4外,还可能生成的盐为
②测定肼的质量分数。取装置B中的溶液3.2g,调节溶液pH为6.5左右,加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用c mol·L-1的碘溶液滴定(杂质不参与反应),滴定过程中有无色、无味、无毒气体产生。滴定终点平均消耗标准溶液20.00mL,产品中肼的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、C、D、E分别是铁或铁的化合物。其中D是一种红褐色沉淀,E在空气中极易被氧化。其相互反应关系如图所示:
根据如图所示变化,按要求回答下列问题:
(1)写出A、E的化学式: A_______ ,E_______ ;
(2)写出其中几步反应的化学方程式(能写离子方程式的写离子方程式):
C→B:_______ ;B→C:_______ ;E→D:_______ 。
(3)C中加入NaOH溶液,一段时间内看到的现象是_______ 。

根据如图所示变化,按要求回答下列问题:
(1)写出A、E的化学式: A
(2)写出其中几步反应的化学方程式(能写离子方程式的写离子方程式):
C→B:
(3)C中加入NaOH溶液,一段时间内看到的现象是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
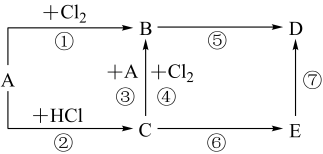
【推荐2】如图,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:
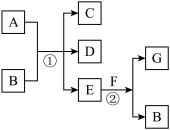
(1)G、A的化学式分别为_______ 、_______ 。
(2)写出反应①的离子方程式:_______ 。
(3)写出反应②的化学方程式:_______
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是_______ 。
②A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是_______ (用化学方程式表示)。

(1)G、A的化学式分别为
(2)写出反应①的离子方程式:
(3)写出反应②的化学方程式:
(4)已知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊溶液中,观察到的现象是
②A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】分类法是研究物质性质的重要方法。现有 、
、 、
、 、
、 、
、 、
、 等物质,根据它们的组成及性质进行如图分类:
等物质,根据它们的组成及性质进行如图分类:
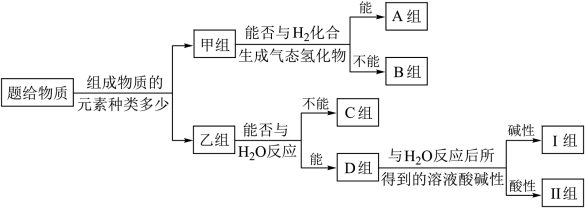
请回答下列问题:
(1)淡黄色固体最终位于其中一组,它的电子式为_______ 。该物质与水反应,若有 个电子转移,则有
个电子转移,则有_______ mol该物质参与反应。
(2)写出实验室制备Ⅰ组中气体的化学方程式_______ 。
(3)B组中的物质能与稀硝酸反应,写出该反应的离子方程式_______ 。
(4)Ⅱ组中的物质滴入水中后与水剧烈反应产生大量酸雾,写出该反应的化学方程式_______ 。
 、
、 、
、 、
、 、
、 、
、 等物质,根据它们的组成及性质进行如图分类:
等物质,根据它们的组成及性质进行如图分类:
请回答下列问题:
(1)淡黄色固体最终位于其中一组,它的电子式为
 个电子转移,则有
个电子转移,则有(2)写出实验室制备Ⅰ组中气体的化学方程式
(3)B组中的物质能与稀硝酸反应,写出该反应的离子方程式
(4)Ⅱ组中的物质滴入水中后与水剧烈反应产生大量酸雾,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。部分元素在周期表中的位置如下:
(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为_______ 。
②经分析,月壤中含有大量的元素d和h,原子半径d_______ h,元素h在周期表中的位置为_______ 。
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为_______ ,f与i形成离子键的过程为_______ 。
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为_______ ,导致该氢化物熔沸点偏高的原因是_______ 。
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为_______ 。
(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请用化学方程式表示你的预测_______ 。(任写一条)
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | g | h | i | |||||||||||||
| j |
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为
②经分析,月壤中含有大量的元素d和h,原子半径d
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为
(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请用化学方程式表示你的预测
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下图是常见物质之间的转化关系,其中金属A是生活中应用最多的金属,其元素在地壳中的含量仅次于铝。甲、乙、丙在常温下是气体,且气体乙为黄绿色。图中有些反应的产物和反应的条件没有全部标出。
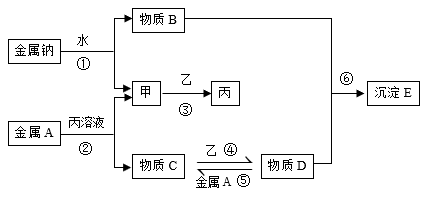
请根据以上信息回答下列问题:
(1)写出反应①和④的化学方程式_______ 、_______ 。
(2)写出反应⑤的离子方程式_______ 。
(3)写出气体乙与水反应的离子方程式_______ 。
(4)写出一个化合反应 生成E_______ 。
(5)“维生素C”也可将物质D转化为物质C,试分析“维生素C”在这一反应过程中的作用是___ 。

请根据以上信息回答下列问题:
(1)写出反应①和④的化学方程式
(2)写出反应⑤的离子方程式
(3)写出气体乙与水反应的离子方程式
(4)写出一个
(5)“维生素C”也可将物质D转化为物质C,试分析“维生素C”在这一反应过程中的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某小组想通过实验探究 Na、Mg、Al 三种金属元素性质的递变规律。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式___________ 。
(2)上述反应中,作还原剂的是___________ 。
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为___________ L。
(4)溶液中,使酚酞试液变红的微粒是___________ 。
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是___________ 。
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是___________ 。
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
(8)综上实验可知,NaOH、Mg(OH)2、Al(OH)3的碱性由强到弱的顺序是___________ 。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式
(2)上述反应中,作还原剂的是
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为
(4)溶液中,使酚酞试液变红的微粒是
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
| 现象 | 结论 | |
| ④ | 出现白色沉淀 | Al(OH)3的碱性比NaOH弱 |
| 沉淀全部溶解 | ||
| ⑤ | 出现白色沉淀 | |
| 沉淀不溶解 | Mg(OH)2无酸性 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知A、B、C、D、E、F、G中均含有同一种元素。A为一种银白色的金属单质,B为A的氧化物,C为一种淡黄色固体,F为食盐的主要成分,G可用于焙制糕点。它们之间的相互转化关系如图所示,回答下列问题:
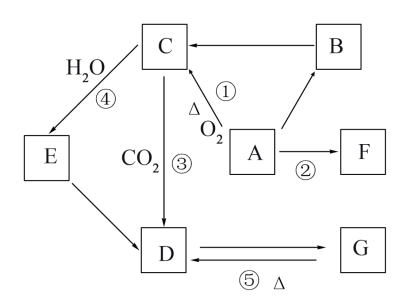
(1)C为___________ (填化学式,下同),G为___________ 。
(2)写出反应③的化学方程式:___________ 。
(3)向G的溶液中滴入E的溶液,发生反应的离子方程式为___________ 。
(4)由F的饱和溶液可制得G和氯化铵,反应的化学方程式为___________ 。

(1)C为
(2)写出反应③的化学方程式:
(3)向G的溶液中滴入E的溶液,发生反应的离子方程式为
(4)由F的饱和溶液可制得G和氯化铵,反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】研究小组探究Na2O2与水反应。向1.56gNa2O2粉末中加入40mL水,充分反应得溶液A(溶液体积变化忽略不计),进行实验。
实验1:向2mL溶液A中滴入1滴酚酞,溶液变红色,20秒后褪色。
(1)Na2O2与H2O反应的化学方程式为___ 。溶液A中NaOH溶液的物质的量浓度为___ 。
(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【提出猜想】
猜想1:Na2O2与H2O反应可能生成了H2O2
猜想2:生成的NaOH浓度太大
【设计并进行实验】
①实验2:向2mL溶液A中加入黑色粉末___ (填化学式),快速产生了能使带火星木条复燃的气体。
②实验3:向2mL物质的量浓度为___ mol/LNaOH溶液中滴入1滴酚酞,溶液变红色,10分钟后溶液褪色。向褪色的溶液中加入___ ,溶液变红色。
【得出结论】
③由以上实验可得出的结论是___ 。
【反思与评价】
(3)分析实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为___ 、___ ,但课本上没有写出中间产物H2O2,可能的原因是___ 。
实验1:向2mL溶液A中滴入1滴酚酞,溶液变红色,20秒后褪色。
(1)Na2O2与H2O反应的化学方程式为
(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【提出猜想】
猜想1:Na2O2与H2O反应可能生成了H2O2
猜想2:生成的NaOH浓度太大
【设计并进行实验】
①实验2:向2mL溶液A中加入黑色粉末
②实验3:向2mL物质的量浓度为
【得出结论】
③由以上实验可得出的结论是
【反思与评价】
(3)分析实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为
您最近一年使用:0次