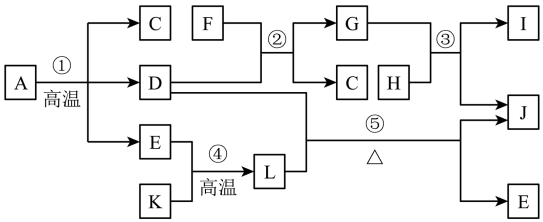
A~L为中学化学常见物质,A为绿色矿石,C为实验室常用溶剂,D为金属氧化物,E为光合作用原料之一,F为二元强酸,K、H分别为固体单质,J为红色金属单质,I的水溶液呈浅绿色,它们之间的转化关系如图所示。
回答下列问题:
(1)A中主要成分的化学式为___ ,D的化学式为___ 。
(2)A—L物质中属于氧化物的有__ (填化学式,下同),属于盐的有___ 。
(3)反应②的离子方程式为__ 。
(4)写出反应⑤化学方程式并用单线桥法标明电子的转移:__ ,该反应现象为__ 。

回答下列问题:
(1)A中主要成分的化学式为
(2)A—L物质中属于氧化物的有
(3)反应②的离子方程式为
(4)写出反应⑤化学方程式并用单线桥法标明电子的转移:
更新时间:2021/12/03 21:04:16
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO;②HCl、H2O、H2SO4、HNO3;③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A___________ ;B___________ ;C___________ 。
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应___________ (填“是”或“不是”)氧化还原反应。写出NaHCO3的电离方程式;___________ 。
(3)写出物质C与足量稀盐酸反应的离子方程式:___________ 。
(4) 与H+在溶液中能共存吗?试用离子方程式说明
与H+在溶液中能共存吗?试用离子方程式说明___________ 。
①MgO、Na2O、CO2、CuO;②HCl、H2O、H2SO4、HNO3;③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应
(3)写出物质C与足量稀盐酸反应的离子方程式:
(4)
 与H+在溶液中能共存吗?试用离子方程式说明
与H+在溶液中能共存吗?试用离子方程式说明
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4•5H2O及CaCO3的步骤如图:
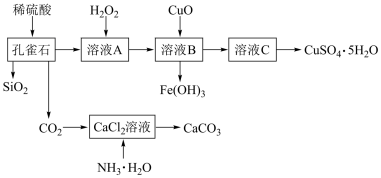
(1)H2O2中O的化合价为______ 。
(2)CaO、CO2、H2O中属于电解质的是______ 。
(3)Cu2(OH)2CO3属于______ (填“酸”“碱”或“盐”)。
(4)制备CaCO3时,发生的反应的化学方程式为______ 。
(5)在一定条件下发生氧化还原反应的是______ 。(填序号)
①孔雀石与稀盐酸 ②溶液A与H2O2③溶液B与CuO ④CO2与NH3•H2O、CaCl2溶液

(1)H2O2中O的化合价为
(2)CaO、CO2、H2O中属于电解质的是
(3)Cu2(OH)2CO3属于
(4)制备CaCO3时,发生的反应的化学方程式为
(5)在一定条件下发生氧化还原反应的是
①孔雀石与稀盐酸 ②溶液A与H2O2③溶液B与CuO ④CO2与NH3•H2O、CaCl2溶液
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】硫及其化合物的“价-类”二维图体现了化学变化之美。
(1)自然界中有斜方硫和单斜硫,它们的关系是______ (填“同位素”或“同素异形体”),二者转化属于化学变化。
(2)如图中属于酸性氧化物的物质是______ (用化学式表示)。
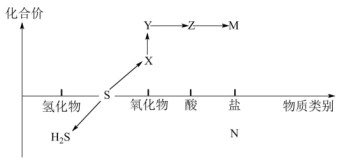
(3)不同价态的硫元素可以相互转化,请写出符合下列转化条件的化学方程式:
反应前后存在3种价态的硫元素的化学方程式______ 。
(4)如果有反应 ,
,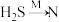 ,M是下列物质中的
,M是下列物质中的______ (填字母序号)
a. b.
b. c.
c. d.
d.
Q可以是______ (用化学式表示,写出至少2类物质)。
(5) 和
和 均为重要的化工产品。已知
均为重要的化工产品。已知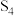 的结构式
的结构式 和有关化学键能如下,则反应
和有关化学键能如下,则反应
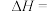
______  。
。
(6) 是一种优良的绝缘气体,分子结构中只存在
是一种优良的绝缘气体,分子结构中只存在 键。已知:
键。已知: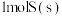 转化为气态硫原子吸收能量
转化为气态硫原子吸收能量 ,断裂
,断裂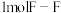 、
、 键需要吸收的能量分别为
键需要吸收的能量分别为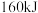 、
、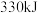 。则
。则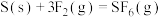 的反应热
的反应热 为
为______ 。
(1)自然界中有斜方硫和单斜硫,它们的关系是
(2)如图中属于酸性氧化物的物质是

(3)不同价态的硫元素可以相互转化,请写出符合下列转化条件的化学方程式:
反应前后存在3种价态的硫元素的化学方程式
(4)如果有反应
 ,
,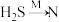 ,M是下列物质中的
,M是下列物质中的a.
 b.
b. c.
c. d.
d.
Q可以是
(5)
 和
和 均为重要的化工产品。已知
均为重要的化工产品。已知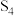 的结构式
的结构式 和有关化学键能如下,则反应
和有关化学键能如下,则反应
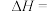
 。
。化学键 |
|
|
|
键能 | 266 | 255 | 243 |
 是一种优良的绝缘气体,分子结构中只存在
是一种优良的绝缘气体,分子结构中只存在 键。已知:
键。已知: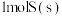 转化为气态硫原子吸收能量
转化为气态硫原子吸收能量 ,断裂
,断裂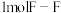 、
、 键需要吸收的能量分别为
键需要吸收的能量分别为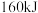 、
、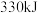 。则
。则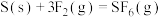 的反应热
的反应热 为
为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态及其含量,设计并进行了如下实验:
【查阅资料】该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸);KSCN中的硫元素为-2价。
实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)将补铁剂碾碎的目的是__________________________________________ 。
(2)试剂1是______________ ,试剂2是______________ 。
(3)加入试剂2后溶液变为浅红色,说明溶液①中含有:___________________ 。
(4)能证明溶液①中含有 的实验现象是
的实验现象是______________ 。
(5)完成在上述条件下 与
与 发生反应的离子方程式
发生反应的离子方程式_________________ 。
(6)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是______________________________ 。
实验Ⅱ.测定该补铁剂中铁元素的含量。
方法一:
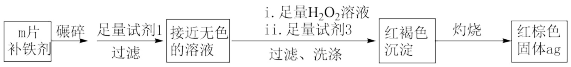
方法二:
①配制0.01、0.008等一系列浓度的 (红色)标准比色液。
(红色)标准比色液。
②样品处理:
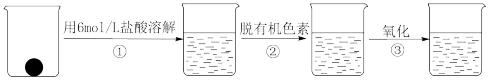
③准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10mL。
④比色,直到与选取的标准颜色一致或相近即可。
(7)方法二中配制100mL 0.01 溶液,需要的玻璃仪器有:烧杯、玻璃棒,还需要:
溶液,需要的玻璃仪器有:烧杯、玻璃棒,还需要:_____ 。
(8)方法二比色法确定待测液的浓度的原理是___________ 。
【查阅资料】该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸);KSCN中的硫元素为-2价。
实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)将补铁剂碾碎的目的是
(2)试剂1是
(3)加入试剂2后溶液变为浅红色,说明溶液①中含有:
(4)能证明溶液①中含有
 的实验现象是
的实验现象是(5)完成在上述条件下
 与
与 发生反应的离子方程式
发生反应的离子方程式(6)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是实验Ⅱ.测定该补铁剂中铁元素的含量。
方法一:
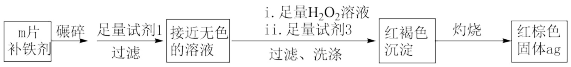
方法二:
①配制0.01、0.008等一系列浓度的
 (红色)标准比色液。
(红色)标准比色液。②样品处理:

③准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10mL。
④比色,直到与选取的标准颜色一致或相近即可。
(7)方法二中配制100mL 0.01
 溶液,需要的玻璃仪器有:烧杯、玻璃棒,还需要:
溶液,需要的玻璃仪器有:烧杯、玻璃棒,还需要:(8)方法二比色法确定待测液的浓度的原理是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】已知海水中的溴含量约为65mg·L-1,从海水中提取溴的工业流程如图:

(1)上述步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将其转化成化合态的溴,目的是__ 。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的___ (填序号)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在方框内填入正确的化学计量数:
________ Br2+________ CO =
=________ BrO +
+________ Br-+________ CO2↑
(4)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为___ 。
(5)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有__ (填字母)。
A.乙醇 B.四氯化碳 C.裂化汽油 D.苯

(1)上述步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将其转化成化合态的溴,目的是
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在方框内填入正确的化学计量数:
 =
= +
+(4)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为
(5)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有
A.乙醇 B.四氯化碳 C.裂化汽油 D.苯
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】铈是一种我国储量较为丰富的稀土元素。回答下列问题:
(1)铈元素有多种核素,如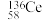 、
、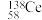 、
、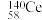 、
、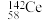 ,它们互为
,它们互为___________ 。
(2)铈常见化合价有 和
和 ,已知氧化性
,已知氧化性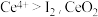 溶于氢碘酸,溶液显黄色,则发生反应的离子方程式为
溶于氢碘酸,溶液显黄色,则发生反应的离子方程式为____ 。
(3)一种以氟碳铈矿(要成分为 )原料制备
)原料制备 的流程如图。
的流程如图。
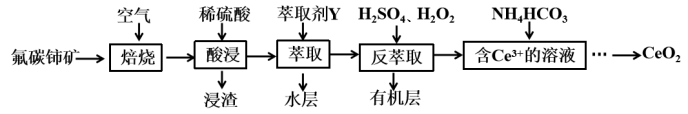
已知 能被萃取剂
能被萃取剂 萃取,
萃取, 不能被萃取剂
不能被萃取剂 萃取。
萃取。
①焙烧过程中,一般要通入足量的空气,目的是___________ 。
②写出反萃取时 参与反应的离子方程式
参与反应的离子方程式___________ 。
(4)上述流程中,若酸浸过程中的稀硫酸改为盐酸、硼酸,则浸渣中易得到沉淀物 ,向该沉淀中加入
,向该沉淀中加入 溶液会发生如下反应:
溶液会发生如下反应: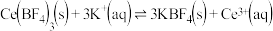 。若某温度下,
。若某温度下, 、
、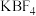 的
的 的值分别为
的值分别为 、
、 ,该平衡体系中
,该平衡体系中 的物质的量浓度为
的物质的量浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为___________  。
。
(1)铈元素有多种核素,如
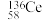 、
、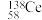 、
、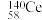 、
、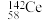 ,它们互为
,它们互为(2)铈常见化合价有
 和
和 ,已知氧化性
,已知氧化性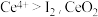 溶于氢碘酸,溶液显黄色,则发生反应的离子方程式为
溶于氢碘酸,溶液显黄色,则发生反应的离子方程式为(3)一种以氟碳铈矿(要成分为
 )原料制备
)原料制备 的流程如图。
的流程如图。
已知
 能被萃取剂
能被萃取剂 萃取,
萃取, 不能被萃取剂
不能被萃取剂 萃取。
萃取。①焙烧过程中,一般要通入足量的空气,目的是
②写出反萃取时
 参与反应的离子方程式
参与反应的离子方程式(4)上述流程中,若酸浸过程中的稀硫酸改为盐酸、硼酸,则浸渣中易得到沉淀物
 ,向该沉淀中加入
,向该沉淀中加入 溶液会发生如下反应:
溶液会发生如下反应: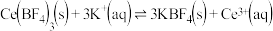 。若某温度下,
。若某温度下, 、
、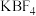 的
的 的值分别为
的值分别为 、
、 ,该平衡体系中
,该平衡体系中 的物质的量浓度为
的物质的量浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】Ⅰ.实验室需要480mL物质的量浓度为0.1mol/L的KMnO4溶液,回答问题:
(1)要配制上述溶液,所需仪器除天平、药匙、烧杯、玻璃棒、胶头滴管外,还需要_______ ;
(2)根据计算,需称量KMnO4固体的质量为______ g;
(3)下列操作会导致所配溶液浓度偏低的是_____ (填选项代号)。
A.定容时加水超过刻度线,用胶头滴管吸出一些
B.定容时仰视刻度线
C.转移溶液后,没有洗涤烧杯内壁
D.配制前容量瓶内壁仍残留有蒸馏水
E.转移溶液时部分溶液溅出
Ⅱ.KMnO4是一种强氧化剂, 加酸酸化能够提高其氧化性,通常用硫酸酸化而不能用盐酸酸化,原因是KMnO4可以和盐酸发生反应。
(4)用双线桥法分析反应:2 +10Cl-+16H+=2Mn2++5Cl2↑+8H2O。
+10Cl-+16H+=2Mn2++5Cl2↑+8H2O。_____ ,该反应中,还原产物是_____ 。判断氧化剂和氧化产物的氧化性强弱_______ 。
(5)若转移的电子数为0.4mol,则产生标况下气体体积为__________ 。
(1)要配制上述溶液,所需仪器除天平、药匙、烧杯、玻璃棒、胶头滴管外,还需要
(2)根据计算,需称量KMnO4固体的质量为
(3)下列操作会导致所配溶液浓度偏低的是
A.定容时加水超过刻度线,用胶头滴管吸出一些
B.定容时仰视刻度线
C.转移溶液后,没有洗涤烧杯内壁
D.配制前容量瓶内壁仍残留有蒸馏水
E.转移溶液时部分溶液溅出
Ⅱ.KMnO4是一种强氧化剂, 加酸酸化能够提高其氧化性,通常用硫酸酸化而不能用盐酸酸化,原因是KMnO4可以和盐酸发生反应。
(4)用双线桥法分析反应:2
 +10Cl-+16H+=2Mn2++5Cl2↑+8H2O。
+10Cl-+16H+=2Mn2++5Cl2↑+8H2O。(5)若转移的电子数为0.4mol,则产生标况下气体体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】氯及其化合物在生产、生活中有着广泛的用途。
Ⅰ.次氯酸钠是最普通的家庭洗涤中的“氯”漂白剂和消毒剂。已知某试剂瓶上贴有如图所示的标签,完成以下问题:

(1)该“84消毒液”的物质的量浓度约为___ mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制100mL含NaClO质量分数为37.25%的消毒液。需要用托盘天平称量NaClO固体的质量为___ g。
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”“偏低”或“无影响”):
①称量时若选择的NaClO固体已在空气中放置时间过久___ ;
②定容时俯视容量瓶刻度线___ 。
Ⅱ.ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
试回答下列问题:
(1)请用双线桥表示反应中电子转移的情况___ 。
2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
(2)试比较KClO3和CO2的氧化性强弱:KClO3___ CO2(填“>”“<”或“=”)。
(3)消毒时,ClO2还可以将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物,此过程说明ClO2具有___ (填“氧化”或“还原”)性。
(4)在标准状况下,当生成11.2LClO2时,转移电子的数目为___ 。
Ⅰ.次氯酸钠是最普通的家庭洗涤中的“氯”漂白剂和消毒剂。已知某试剂瓶上贴有如图所示的标签,完成以下问题:

(1)该“84消毒液”的物质的量浓度约为
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制100mL含NaClO质量分数为37.25%的消毒液。需要用托盘天平称量NaClO固体的质量为
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”“偏低”或“无影响”):
①称量时若选择的NaClO固体已在空气中放置时间过久
②定容时俯视容量瓶刻度线
Ⅱ.ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
试回答下列问题:
(1)请用双线桥表示反应中电子转移的情况
2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
(2)试比较KClO3和CO2的氧化性强弱:KClO3
(3)消毒时,ClO2还可以将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物,此过程说明ClO2具有
(4)在标准状况下,当生成11.2LClO2时,转移电子的数目为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)饮用水中NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。
①配平方程式并用双线桥表示电子转移情况:_____ 。
_____Al+____NO +_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。
+_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。
②上述反应中,还原剂与还原产物的物质的量之比是_____ ,反应中转移电子0.3mol,生成_____ mL(标准状况下)N2。
II.如图是成外化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配制100mL1mol•L-1的稀盐酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;请回答下列问题:
(2)配制稀盐酸时,还缺少的仪器有_____ 。
(3)经计算,配制100mL1mol•L-1的稀盐酸需要用量筒量取上述浓盐酸的体积为_______ mL(保留小数点后一位)。
(4)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L-1,引起误差的原因可能是_____ 。
(1)饮用水中NO
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。①配平方程式并用双线桥表示电子转移情况:
_____Al+____NO
 +_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。
+_____OH-+_____H2O=______[Al(OH)4]-+_____N2↑。②上述反应中,还原剂与还原产物的物质的量之比是
II.如图是成外化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配制100mL1mol•L-1的稀盐酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;请回答下列问题:
(2)配制稀盐酸时,还缺少的仪器有
(3)经计算,配制100mL1mol•L-1的稀盐酸需要用量筒量取上述浓盐酸的体积为
(4)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L-1,引起误差的原因可能是
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶在使用前未干燥,里面有少量蒸馏水 |
| C.转移溶液后,未洗涤烧杯和玻璃棒 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线 |
您最近一年使用:0次