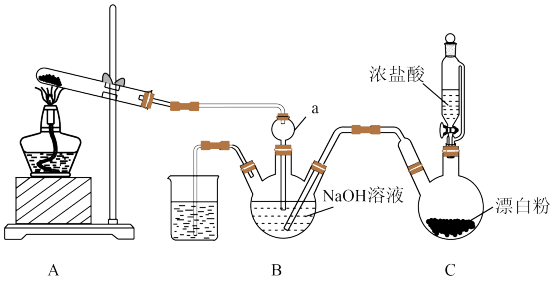
肼(N2H4) 是一种重要的工业产品,实验室用NH3与Cl2合成肼(N2H4) 并探究肼的性质。实验装置如图所示:
相关物质的性质如下:
回答下列问题:
(1)装置A试管中的试剂为_______ (填化学式)。仪器a的名称是_______ 。
(2)N2H4是_______ 分子(填“极性”或“非极性”)。
(3)装置B中制备肼的离子方程式为_______ ,该装置中通入NH3必须过量的原因是_______ 。
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是_______ 。
(5)①探究N2H4的性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元弱碱,肼与硫酸反应除能生成N2H6SO4外,还可能生成的盐为_______ 。(填化学式)。
②测定肼的质量分数。取装置B中的溶液3.2g,调节溶液pH为6.5左右,加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用c mol·L-1的碘溶液滴定(杂质不参与反应),滴定过程中有无色、无味、无毒气体产生。滴定终点平均消耗标准溶液20.00mL,产品中肼的质量分数为_______ %。

相关物质的性质如下:
| 性状 | 熔点/℃ | 沸点/℃ | 性质 | |
| N2H4 | 无色液体 | 1.4 | 113 | 与水混溶、强还原性 |
| N2H6SO4 | 无色晶体 | 254 | / | 微溶于冷水,易溶于热水 |
(1)装置A试管中的试剂为
(2)N2H4是
(3)装置B中制备肼的离子方程式为
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究N2H4的性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元弱碱,肼与硫酸反应除能生成N2H6SO4外,还可能生成的盐为
②测定肼的质量分数。取装置B中的溶液3.2g,调节溶液pH为6.5左右,加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用c mol·L-1的碘溶液滴定(杂质不参与反应),滴定过程中有无色、无味、无毒气体产生。滴定终点平均消耗标准溶液20.00mL,产品中肼的质量分数为
22-23高三上·云南昆明·阶段练习 查看更多[7]
更新时间:2022-09-17 20:08:21
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】碘及其化合物广泛用于医药、染料等方面。回答下列问题:
Ⅰ. 的一种制备方法如下图所示:
的一种制备方法如下图所示:

(1)“富集”步骤中,生成的黄色固体为______ (填化学式)。
(2)“氧化”步骤中的离子方程式为______ 。
Ⅱ.下图是利用海带浸取原液制备 的甲、乙两种实验方案:
的甲、乙两种实验方案:
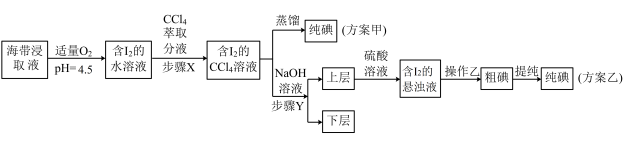
已知:① ;
;
②碘微溶于水,从 左右开始升华;
左右开始升华; 的沸点是
的沸点是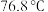 。
。
(3)海带浸取原液在酸性条件下被 氧化的离子方程式是
氧化的离子方程式是______ 。
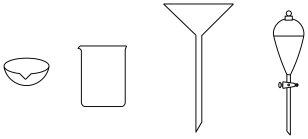
(4)步骤 需要用到的仪器有
需要用到的仪器有______ (从下列图中选择,写出仪器名称)。
(5)“含 的悬浊液”中,水溶液的主要溶质是
的悬浊液”中,水溶液的主要溶质是______ (填化学式)。
(6)操作乙的名称是______ 。
(7)方案甲中采用“蒸馏”不合理,理由是______ 。
Ⅰ.
 的一种制备方法如下图所示:
的一种制备方法如下图所示:
(1)“富集”步骤中,生成的黄色固体为
(2)“氧化”步骤中的离子方程式为
Ⅱ.下图是利用海带浸取原液制备
 的甲、乙两种实验方案:
的甲、乙两种实验方案:
已知:①
 ;
;②碘微溶于水,从
 左右开始升华;
左右开始升华; 的沸点是
的沸点是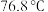 。
。(3)海带浸取原液在酸性条件下被
 氧化的离子方程式是
氧化的离子方程式是(4)步骤
 需要用到的仪器有
需要用到的仪器有
(5)“含
 的悬浊液”中,水溶液的主要溶质是
的悬浊液”中,水溶液的主要溶质是(6)操作乙的名称是
(7)方案甲中采用“蒸馏”不合理,理由是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】电子工业常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。从腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜,并重新获得FeCl3溶液。废液处理流程如下:
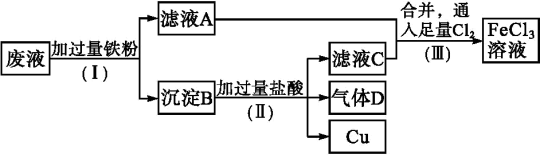
(1)步骤(Ⅰ)中涉及反应的离子方程式:_______ ;_______ 。
(2)沉淀B中主要含有_______ ,气体D是_______ ;
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式_______ ;
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:_______ 。
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为_______ 。
(6)如果向FeCl2溶液中滴加NaOH溶液,现象是_______ ;沉淀变色的原因是_______ (用化学方程式解释)。

(1)步骤(Ⅰ)中涉及反应的离子方程式:
(2)沉淀B中主要含有
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为
(6)如果向FeCl2溶液中滴加NaOH溶液,现象是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】有一包白色粉末,其中可能含有Ba(NO3)2、MgCl2、K2CO3、NaOH,现做以下实验:
①取一定量粉末加入水中,振荡,有白色沉淀生成;②向①的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生;③向①的上层清液中滴入硫酸钠溶液,有白色沉淀产生。根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是___________ ,一定不含有的物质是___________ 。(写化学式)
(2)写出各步变化的离子方程式。
①___________ ; ②___________ ;③___________ 。
①取一定量粉末加入水中,振荡,有白色沉淀生成;②向①的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生;③向①的上层清液中滴入硫酸钠溶液,有白色沉淀产生。根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是
(2)写出各步变化的离子方程式。
①
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题
(1)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。
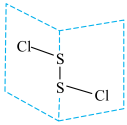
①S2Cl2的结构式为___________ , 的化学键类型为
的化学键类型为___________ (填“极性键”、“非极性键”或“极性键和非极性键”),它是___________ (填“极性”或“非极性”)分子。
②电负性:S___________ Cl (填“>”或“<”), 中硫的化合价为
中硫的化合价为___________ 。
③S2Cl2分子中S原子的杂化轨道类型为___________ ,每个S原子有 ___________ 对孤电子对。
(2)毒奶粉中发现的化工原料三聚氰胺可以由下列反应合成:CaO+3C CaC2+CO↑;CaC2+N2
CaC2+CO↑;CaC2+N2 CaCN2+C;
CaCN2+C; ;
;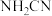 与水反应生成尿素
与水反应生成尿素 ;尿素合成三聚氰胺。
;尿素合成三聚氰胺。
①基态钙原子电子占据的最高能级符号是___________ ,其核外共有___________ 种不同能量的电子。
② 中阴离子为
中阴离子为 ,
, 与CO2分子空间结构相似,由此可以推知
与CO2分子空间结构相似,由此可以推知 的空间结构为
的空间结构为___________ 。
③尿素分子 中所含元素的电负性由大到小的顺序为
中所含元素的电负性由大到小的顺序为___________ 。
④三聚氰胺俗称“蛋白精”,其结构如图,其中氮原子的杂化方式为___________ 。
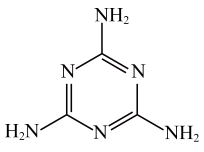
(1)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。

①S2Cl2的结构式为
 的化学键类型为
的化学键类型为②电负性:S
 中硫的化合价为
中硫的化合价为③S2Cl2分子中S原子的杂化轨道类型为
(2)毒奶粉中发现的化工原料三聚氰胺可以由下列反应合成:CaO+3C
 CaC2+CO↑;CaC2+N2
CaC2+CO↑;CaC2+N2 CaCN2+C;
CaCN2+C; ;
;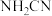 与水反应生成尿素
与水反应生成尿素 ;尿素合成三聚氰胺。
;尿素合成三聚氰胺。①基态钙原子电子占据的最高能级符号是
②
 中阴离子为
中阴离子为 ,
, 与CO2分子空间结构相似,由此可以推知
与CO2分子空间结构相似,由此可以推知 的空间结构为
的空间结构为③尿素分子
 中所含元素的电负性由大到小的顺序为
中所含元素的电负性由大到小的顺序为④三聚氰胺俗称“蛋白精”,其结构如图,其中氮原子的杂化方式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】我国将力争在2030年前实现碳达峰,2060年前实现碳中和的目标,因此二氧化碳的固定以及转化将成为重要的研究课题。
I.在 催化下CO2和H2反应生成甲醇:
催化下CO2和H2反应生成甲醇: 。
。
II.新型 水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
请回答下列问题:
(1)I中涉及的CO2、H2、CH3OH、H2O,属于非极性分子的是___________ ,基态O原子核外有___________ 种不同空间运动状态的电子。
(2)HCOOH分子中σ键和π键数目之比为___________ 。
(3)反应 中,碳原子的杂化方式由
中,碳原子的杂化方式由___________ 转变为___________ 。CH3OH的沸点高于CH3SH,原因是___________ 。
(4)一种铜的配合物为 ,其配体为
,其配体为___________ 。
I.在
 催化下CO2和H2反应生成甲醇:
催化下CO2和H2反应生成甲醇: 。
。II.新型
 水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。请回答下列问题:
(1)I中涉及的CO2、H2、CH3OH、H2O,属于非极性分子的是
(2)HCOOH分子中σ键和π键数目之比为
(3)反应
 中,碳原子的杂化方式由
中,碳原子的杂化方式由(4)一种铜的配合物为
 ,其配体为
,其配体为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列问题。
(1)有下列粒子:①CH4 ②CH2O ③HCN ④NH3 ⑤ ⑥BF3 ⑦H2O。
⑥BF3 ⑦H2O。
①含有极性键的非极性分子的是______ (填编号,下同)。
②所有原子共平面的是_______ ,共线的是_______ 。
(2)过氧乙酸(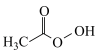 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有______ ,分子中σ键和π键的个数比为_______ 。
(3) GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为_____ ,每个 原子周围最近的
原子周围最近的 原子数目为
原子数目为______ 。已知GaAs的密度为d g/cm3,摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则晶胞的棱长为_____ nm(列式表示)。_____ (填字母)。
A.CO2 B.SiF4 C.SCl2 D. E.H3O+
E.H3O+
请分析键角大小比较的一般方法_____ 。
(1)有下列粒子:①CH4 ②CH2O ③HCN ④NH3 ⑤
 ⑥BF3 ⑦H2O。
⑥BF3 ⑦H2O。①含有极性键的非极性分子的是
②所有原子共平面的是
(2)过氧乙酸(
 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有(3)
 GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为 原子周围最近的
原子周围最近的 原子数目为
原子数目为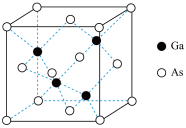
A.CO2 B.SiF4 C.SCl2 D.
 E.H3O+
E.H3O+请分析键角大小比较的一般方法
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】以Fe(NO3)3作为铁源制备高铁酸钾(K2FeO4),可用于去除水体中的As(Ⅲ)。已知:K2FeO4微溶于水。在酸性或中性溶液中迅速氧化H2O产生O2,在碱性溶液中较稳定。在Fe3+和Fe(OH)3催化作用下发生分解。
(1)制备高铁酸钾。向KOH和KClO混合溶液中加入Fe(NO3)3,过滤得到K2FeO4固体。
①制备K2FeO4的化学方程式为_______ 。
②制备过程中KOH和KClO需过量的原因是_______ 。
③过滤所得的滤液中加入稀硫酸,产生Cl2,原因可能是:酸性条件下K2FeO4氧化了Cl-,还可能是_______ 。
(2)测定K2FeO4的纯度。准确称取0.5280gK2FeO4样品置于锥形瓶中,用KOH溶液溶解,加入过量KCr(OH)4溶液,再加入硫酸酸化配成待测液。用0.3000mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准液20.00mL。计算样品中K2FeO4的纯度_______ (写出计算过程)。测定过程中涉及的离子反应有:
Cr(OH) +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-
2CrO +2H+=Cr2O
+2H+=Cr2O +H2O
+H2O
Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
(1)制备高铁酸钾。向KOH和KClO混合溶液中加入Fe(NO3)3,过滤得到K2FeO4固体。
①制备K2FeO4的化学方程式为
②制备过程中KOH和KClO需过量的原因是
③过滤所得的滤液中加入稀硫酸,产生Cl2,原因可能是:酸性条件下K2FeO4氧化了Cl-,还可能是
(2)测定K2FeO4的纯度。准确称取0.5280gK2FeO4样品置于锥形瓶中,用KOH溶液溶解,加入过量KCr(OH)4溶液,再加入硫酸酸化配成待测液。用0.3000mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准液20.00mL。计算样品中K2FeO4的纯度
Cr(OH)
 +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-2CrO
 +2H+=Cr2O
+2H+=Cr2O +H2O
+H2OCr2O
 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某学习小组为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案:
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。
①完成本实验需要不断用玻璃棒搅拌,其目的是_______________________________ 。
②若实验前所称样品的质量为m g,加热至恒重时固体质量为a g,则样品中纯碱的质量分数为________ 。
(2)方案二:按如图所示装置进行实验,并回答下列问题:
①实验前先检查装置的气密性,并称取一定质量的样品放入A中,将稀硫酸装入分液漏斗中。D装置的作用是________________ 。
②实验中除称量样品质量外,还需分别称量_______ 装置反应前、后质量(填装置字母代号)。
③根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显的缺陷,该缺陷是_________ 。
④有同学认为,用E装置替代A装置能提高实验准确度。你认为是否正确?_________ (填“是”或“否”)。
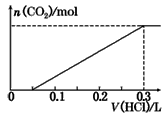
(3)方案三:称取一定量的样品置于锥形瓶中,加适量水,用盐酸进行滴定,从开始至有气体产生到气体不再产生,所滴加的盐酸体积如图所示,则小苏打样品中纯碱的质量分数为_________ (保留两位有效数字)。
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。
①完成本实验需要不断用玻璃棒搅拌,其目的是
②若实验前所称样品的质量为m g,加热至恒重时固体质量为a g,则样品中纯碱的质量分数为
(2)方案二:按如图所示装置进行实验,并回答下列问题:
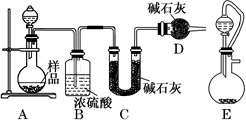
①实验前先检查装置的气密性,并称取一定质量的样品放入A中,将稀硫酸装入分液漏斗中。D装置的作用是
②实验中除称量样品质量外,还需分别称量
③根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显的缺陷,该缺陷是
④有同学认为,用E装置替代A装置能提高实验准确度。你认为是否正确?
(3)方案三:称取一定量的样品置于锥形瓶中,加适量水,用盐酸进行滴定,从开始至有气体产生到气体不再产生,所滴加的盐酸体积如图所示,则小苏打样品中纯碱的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】根据如图所示的转化关系推断各物质,已知A为淡黄色A体,B和C为气体,E医疗上治疗胃酸过多的一种药剂,H为单质,请问答下列问题:
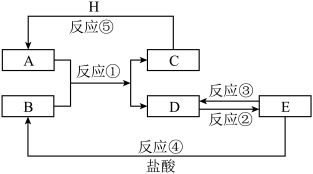
(1)请写出物质的化学式:A___________ ,A中阴阳离子个数比为___________ 。
(2)反应①的化学方程式为_______________ ,反应④的离子方程式为___________________________ 。
(3)D溶液中含有少量的E,可采用的除杂方法为_____________________ (用离子化学方程式表示)。
(4)请设计实验鉴别D溶液和E溶液:______________________ 。
(5)取一定质量的D和E混合物为烧至恒重,冷却至室温,共收集到4.4g气体。加热后剩余的固体物质与足量盐酸反应,共收集到8.8g气体,则原固体混合物中D的质量为___________ 。

(1)请写出物质的化学式:A
(2)反应①的化学方程式为
(3)D溶液中含有少量的E,可采用的除杂方法为
(4)请设计实验鉴别D溶液和E溶液:
(5)取一定质量的D和E混合物为烧至恒重,冷却至室温,共收集到4.4g气体。加热后剩余的固体物质与足量盐酸反应,共收集到8.8g气体,则原固体混合物中D的质量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又被H2还原,生成颗粒很细的铁粉,这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称"引火铁"。
请回答下列问题:
I.利用下图所示装置(加热装置省略)制取铁的氧化物。
(1)试管A中发生反应的化学方程式是___________ 。
(2)圆底烧瓶B的作用是_______ ;圆底烧瓶C的作用是________ 。
(3)AB两处需要加热,首先加热的是______ 处(填字母),原因是________ 。
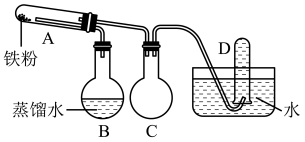
II.利用下图所示装置制取"引火铁"。
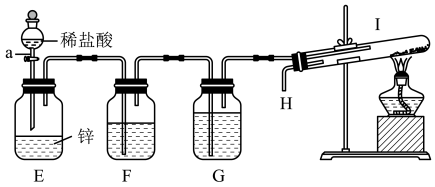
(4)仪器a的名称是___________ 。
(5)装置F的作用是___________ ;装置G中盛放的试剂是___________ ,其作用是___________ 。
(6)为了安全,在I管中的反应发生前,在H出口处必须_______ ;I管中的反应开始后,在H出口处应_______ 。
请回答下列问题:
I.利用下图所示装置(加热装置省略)制取铁的氧化物。

(1)试管A中发生反应的化学方程式是
(2)圆底烧瓶B的作用是
(3)AB两处需要加热,首先加热的是
II.利用下图所示装置制取"引火铁"。

(4)仪器a的名称是
(5)装置F的作用是
(6)为了安全,在I管中的反应发生前,在H出口处必须
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献.联合制碱法的主要过程如图所示。

沉淀池反应
(1)“侯氏制碱法”誉满全球,其中的“碱”为_______ (填化学式)。
(2)往沉淀池通入气体顺序:先通_______ ,后通_______ 。
(3)实验室模拟“侯氏制碱法”,下列操作未涉及的是_______。
(4)煅烧炉中发生反应的化学方程式为_______ 。
(5)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了_______ (填上述流程中的编号)的循环,流程循环中物质X为_______ (填化学式)。

沉淀池反应

(1)“侯氏制碱法”誉满全球,其中的“碱”为
(2)往沉淀池通入气体顺序:先通
(3)实验室模拟“侯氏制碱法”,下列操作未涉及的是_______。
A. | B. | C. | D. |
(5)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体( ):
):
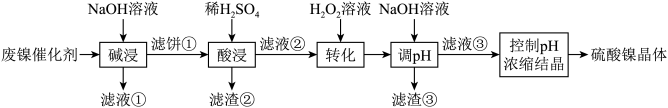
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH溶液可以有效地除去金属铝及其氧化物,写出NaOH溶液除去铝单质的离子方程式___________ 。
(2)“滤液②”中含有的金属离子有Fe2+和___________ ,检验Fe2+的试剂是铁氰化钾溶液,写出Fe2+和铁氰化钾溶液反应的离子方程式___________ 。
(3)“转化”中可替代 的物质是
的物质是___________ (填序号)
①O2 ②氯水 ③酸性 溶液
溶液
若工艺流程改为先“调pH”后“转化”,即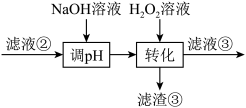 。“滤液③”中可能含有的杂质离子为
。“滤液③”中可能含有的杂质离子为___________ 。
(4)利用上述表格数据,计算 的
的
___________ (写出计算结果)。如果“转化”后的溶液中 浓度为
浓度为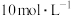 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是___________ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的 。写出该反应的离子方程式
。写出该反应的离子方程式___________ 。
 ):
):
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  | 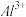 | Fe3+ |  |
开始沉淀时(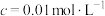 )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH溶液可以有效地除去金属铝及其氧化物,写出NaOH溶液除去铝单质的离子方程式
(2)“滤液②”中含有的金属离子有Fe2+和
(3)“转化”中可替代
 的物质是
的物质是①O2 ②氯水 ③酸性
 溶液
溶液若工艺流程改为先“调pH”后“转化”,即
 。“滤液③”中可能含有的杂质离子为
。“滤液③”中可能含有的杂质离子为(4)利用上述表格数据,计算
 的
的
 浓度为
浓度为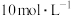 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的
 。写出该反应的离子方程式
。写出该反应的离子方程式
您最近一年使用:0次



