二氧化氯消毒剂是国际公认的高效消毒灭菌剂。二氧化氯漂白液中常含有ClO2和Cl2两种主要成分。化学兴趣小组同学为测定某二氧化氯漂白液中ClO2的浓度,进行如下实验:
[实验I]配制250mL0.1mol/L的Na2S2O3溶液,步骤如下:
①用天平准确称取一定质量的Na2S2O3·5H2O固体,放入烧杯,用适量蒸馏水溶解;
②待溶液恢复至室温后,将烧杯中的溶液转移至250mL容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡;
④继续向容量瓶中加水至距刻度线1~2cm处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是_______ 。
(2)配制溶液过程中需称量Na2S2O3·5H2O固体的质量为_______ g。
(3)配制溶液过程中,若未进行步骤③操作,则配制的溶液浓度_______ 。 填“偏高”、“偏低”或“无影响”
填“偏高”、“偏低”或“无影响”
[实验II]测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应:2ClO2+2KI=2KClO2+I2、Cl2+2KI=2KCl+I2
②加入淀粉作指示剂,向其中逐滴加入0.1mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为:2Na2S2O3+I2=Na2S4O6+2NaI
③加入稀硫酸调节溶液pH=3,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
④再逐滴加入0.1mol/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20mL。
回答下列问题:
(4)用单线桥标出反应中电子转移的方向和数目:2ClO2+2KI=2KClO2+I2。_______
(5)该二氧化氯漂白液中ClO2的浓度为_______ g/L(写出计算过程)。
[实验I]配制250mL0.1mol/L的Na2S2O3溶液,步骤如下:
①用天平准确称取一定质量的Na2S2O3·5H2O固体,放入烧杯,用适量蒸馏水溶解;
②待溶液恢复至室温后,将烧杯中的溶液转移至250mL容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡;
④继续向容量瓶中加水至距刻度线1~2cm处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是
(2)配制溶液过程中需称量Na2S2O3·5H2O固体的质量为
(3)配制溶液过程中,若未进行步骤③操作,则配制的溶液浓度
 填“偏高”、“偏低”或“无影响”
填“偏高”、“偏低”或“无影响”
[实验II]测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应:2ClO2+2KI=2KClO2+I2、Cl2+2KI=2KCl+I2
②加入淀粉作指示剂,向其中逐滴加入0.1mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为:2Na2S2O3+I2=Na2S4O6+2NaI
③加入稀硫酸调节溶液pH=3,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
④再逐滴加入0.1mol/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20mL。
回答下列问题:
(4)用单线桥标出反应中电子转移的方向和数目:2ClO2+2KI=2KClO2+I2。
(5)该二氧化氯漂白液中ClO2的浓度为
更新时间:2022-11-26 09:49:56
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某兴趣小组为探究 和
和 的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图:
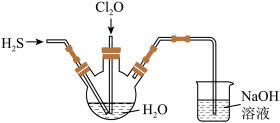
请回答:(1)三颈瓶中出现淡黄色沉淀,溶液呈强酸性,用一个化学方程式表示________ 。
(2)若通入水中的 已过量,设计实验方案检验
已过量,设计实验方案检验________ 。
 和
和 的性质,将两种气体同时通入水中,实验装置如图:
的性质,将两种气体同时通入水中,实验装置如图:
请回答:(1)三颈瓶中出现淡黄色沉淀,溶液呈强酸性,用一个化学方程式表示
(2)若通入水中的
 已过量,设计实验方案检验
已过量,设计实验方案检验
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】新冠肺炎期间,化学消毒剂大显身手。高铁酸钾( )是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的流程如下:
)是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的流程如下:

已知:Cl2与KOH反应,在温度过高时,会生成KClO3。
回答下列问题:
(1)写出可提高反应反应①中化学反应速率的措施:___________ 。
(2)写出反应①中化学反应方程式:___________ 。
(3)检验滤液1中阳离子的方法:___________ 。
(4)写出反应②发生反应的离子方程式:___________ 。
(5)反应②需放在冰水浴中进行的原因:___________ 。
(6)写出反应③发生反应的离子方程式:___________ 。
(7)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂。其原理如下图
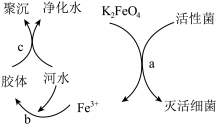
它能消毒杀菌是因为___________ ,它能净水的原因___________ 。
 )是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的流程如下:
)是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的流程如下:
已知:Cl2与KOH反应,在温度过高时,会生成KClO3。
回答下列问题:
(1)写出可提高反应反应①中化学反应速率的措施:
(2)写出反应①中化学反应方程式:
(3)检验滤液1中阳离子的方法:
(4)写出反应②发生反应的离子方程式:
(5)反应②需放在冰水浴中进行的原因:
(6)写出反应③发生反应的离子方程式:
(7)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂。其原理如下图

它能消毒杀菌是因为
您最近一年使用:0次
【推荐3】某小组同学探究H2O2、H2SO3、Br2的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。

(1)打开活塞a,逐滴加入H2SO3溶液至过量,烧瓶内溶液颜色变为无色,该反应的离子方程式为_________________________ ,得出的结论是H2SO3的氧化性比Br2的氧化性________ (填“强”或“弱”)。
(2)再打开活塞b,向所得溶液中逐滴加入H2O2溶液,刚开始溶液颜色无明显变化,继续滴加,溶液变为橙黄色,变橙黄色反应的离子方程式为_______ ,得出的结论是H2O2的氧化性比Br2的氧化性________ (填“强”或“弱”)。

(1)打开活塞a,逐滴加入H2SO3溶液至过量,烧瓶内溶液颜色变为无色,该反应的离子方程式为
(2)再打开活塞b,向所得溶液中逐滴加入H2O2溶液,刚开始溶液颜色无明显变化,继续滴加,溶液变为橙黄色,变橙黄色反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】如图表示配制一定物质的量浓度溶液的几个关键实验步骤和操作,现欲配制250mL0.100 mol/LNa2CO3溶液。

(1)将上述实验步骤 A~F 按实验过程先后次序排列___________ ,
(2)若用 Na2CO3·10H2O 来配制溶液,需称取Na2CO3·10H2O晶体的质量为___________ g,需选择规格为___________ 的容量瓶。
(3)步骤 B 通常称为转移,玻璃棒的作用是___________ ;步骤 A 通常称为___________ ,此时应注意视线与___________ , ___________ 相切。
(4)步骤 B 通常称为转移,若是配制 NaOH 溶液,用水溶解 NaOH 固体后未冷却至室温即转移,配制溶液的浓度将偏___________ (填“高”或“低”)。如果俯视刻度线,配制的浓度将偏___________ (填“高”或“低”)。

(1)将上述实验步骤 A~F 按实验过程先后次序排列
(2)若用 Na2CO3·10H2O 来配制溶液,需称取Na2CO3·10H2O晶体的质量为
(3)步骤 B 通常称为转移,玻璃棒的作用是
(4)步骤 B 通常称为转移,若是配制 NaOH 溶液,用水溶解 NaOH 固体后未冷却至室温即转移,配制溶液的浓度将偏
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室需用480mL 草酸钠(Na2C2O4)溶液,现通过如下步骤配制:
草酸钠(Na2C2O4)溶液,现通过如下步骤配制:
①计算,用托盘天平称量______ gNa2C2O4固体放入小烧杯中,加适量蒸馏水搅拌溶解。
②待①所得溶液恢复至室温后,将小烧杯中的溶液注入______ 中。
③______ 。
④继续加蒸馏水至液面距刻度线1~2cm处,改用______ 滴加蒸馏水至溶液凹液面最低点与刻度线相切。
⑤盖好瓶塞,反复上下颠倒、摇匀。
(1)将实验步骤补充完整。
(2)取出25mL配制好的Na2C2O4溶液稀释至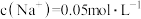 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度为
的物质的量浓度为______  ,稀释后溶液的体积为
,稀释后溶液的体积为______ mL。
 草酸钠(Na2C2O4)溶液,现通过如下步骤配制:
草酸钠(Na2C2O4)溶液,现通过如下步骤配制:①计算,用托盘天平称量
②待①所得溶液恢复至室温后,将小烧杯中的溶液注入
③
④继续加蒸馏水至液面距刻度线1~2cm处,改用
⑤盖好瓶塞,反复上下颠倒、摇匀。
(1)将实验步骤补充完整。
(2)取出25mL配制好的Na2C2O4溶液稀释至
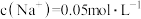 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度为
的物质的量浓度为 ,稀释后溶液的体积为
,稀释后溶液的体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某学生计划用12 mol·L-1的浓盐酸配制0.10 mol·L-1的稀盐酸450 mL。回答下列问题:
(1)实验过程中,不必使用的是________ (填字母)。
A.托盘天平 B.量筒 C.容量瓶 D.250 mL烧杯 E.胶头滴管 F. 500 mL试剂瓶
(2)除上述仪器中可使用的以外,还缺少的仪器是________ ;在该实验中的用途是______ 。
(3)量取浓盐酸的体积为______ mL,应选用的量筒规格为________ 。
(4)配制时应选用的容量瓶规格为______________ 。
(1)实验过程中,不必使用的是
A.托盘天平 B.量筒 C.容量瓶 D.250 mL烧杯 E.胶头滴管 F. 500 mL试剂瓶
(2)除上述仪器中可使用的以外,还缺少的仪器是
(3)量取浓盐酸的体积为
(4)配制时应选用的容量瓶规格为
您最近一年使用:0次



