某同学完成如下实验。
(1)实验记录(请补全表格中空格 )
(2)该实验的目的是______________________ 。
(3)氯、溴、碘单质氧化性逐渐减弱的原因:同主族元素,最外层电子数相同,从上到下,_________ ,得电子能力逐渐减弱。
(1)实验记录(
| 实验步骤 | 实验现象 | 离子方程式 |
 | ①溶液分层 ②下层呈橙色。 | |
 | ①溶液分层 ② | Br2+2I-=I2+2Br- |
(2)该实验的目的是
(3)氯、溴、碘单质氧化性逐渐减弱的原因:同主族元素,最外层电子数相同,从上到下,
更新时间:2017-07-13 19:38:09
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用,为探究氯气的性质,某同学设计了如图所示的实验装置。
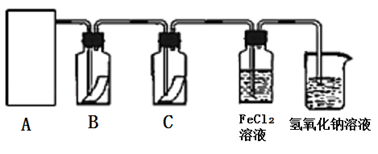
(1)实验中制取氯气的反应原理为(用化学方程式表示):______ 。
(2)利用以上制气原理,从图中选择合适的制气装置(A处)___ (填写序号) 。

(3)装置B、C依次放的是干燥的红色布条和湿润的红色布条,理论上装置______ 中的红色布条褪色,但实验过程中该同学发现装置B、C中的布条均褪色,其原因可能是______ ,说明该装置存在明显的缺陷,请提出合理的改进方法_____ 。
(4)为了验证氯气的氧化性, 将氯气通入FeCl2溶液中,写出氯气 与FeCl2溶液反应的离子方程式_ 。
(5)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是____ (填化学式)

(1)实验中制取氯气的反应原理为(用化学方程式表示):
(2)利用以上制气原理,从图中选择合适的制气装置(A处)

(3)装置B、C依次放的是干燥的红色布条和湿润的红色布条,理论上装置
(4)为了验证氯气的氧化性, 将氯气通入FeCl2溶液中,写出氯气 与FeCl2溶液反应的离子方程式
(5)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知A、B、C均为含铁化合物,请根据以下四种物质的转化过程回答相关问题:
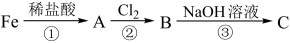
(1)反应①、②、③中属于氧化还原反应的是_______ (填序号);
(2)向B的溶液中滴入几滴KSCN溶液后,可观察到的现象是__________________ ;
(3)C的化学式为____________ ;
(4)氯气是一种有强烈刺激性气味的________ 色气体,写出反应②的离子方程式__________ ;
(5)加入铁粉可以实现B转化为A,请写出实现该转化的化学方程式___________________ 。
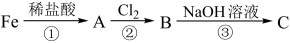
(1)反应①、②、③中属于氧化还原反应的是
(2)向B的溶液中滴入几滴KSCN溶液后,可观察到的现象是
(3)C的化学式为
(4)氯气是一种有强烈刺激性气味的
(5)加入铁粉可以实现B转化为A,请写出实现该转化的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】氯气是一种重要的工业原料。资料显示:
Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
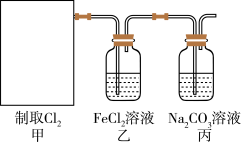
(1)在该实验中,甲部分的装置是________ (填字母)。
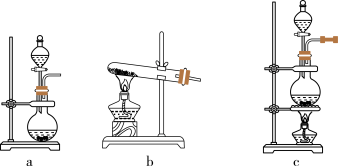
(2)乙装置中FeCl2溶液与Cl2反应的离子方程式是___________________________ 。
(3)丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中发生反应的化学方程式是_________________________________ 。
(4)该实验存在明显的缺陷,改进的方法是___________________________________ 。
Ca(ClO)2+CaCl2+2H2SO4
 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
(1)在该实验中,甲部分的装置是

(2)乙装置中FeCl2溶液与Cl2反应的离子方程式是
(3)丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中发生反应的化学方程式是
(4)该实验存在明显的缺陷,改进的方法是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】已知:Cl2+2I-=2Cl-+I2,海藻中富含碘元素。某化学兴趣小组的同学在实验室里用灼烧海藻的灰分提取碘,流程如图。
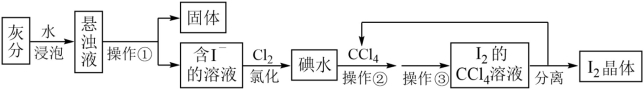
请回答下列问题:
(1)写出操作①、操作③的名称分别为:______________ ,_____________ 。
(2)操作②选用CCl4的理由是___________ 。
A.CCl4不溶于水 B.CCl4的密度比水大
C.碘在CCl4中比在水中溶解度更大 D.CCl4与碘水不反应
(3)用NaOH浓溶液反萃取后再加稀酸,可以分离I2和CCl4,有关化学方程式为:
碱性条件:3I2+6NaOH=5NaI+NaIO3+3H2O;
酸性条件:5NaI+NaIO3+3H2SO4=3Na2SO4+3I2+3H2O。
以下是反萃取过程的操作,请按要求填空:
①向装有I2的CCl4溶液的_____________ (填仪器名称)中加入少量1 mol/LNaOH溶液;
②振荡至溶液的__________ 色消失,静置、分层,则____________ (填“上”、“下”)层为CCl4;
③将含碘的碱溶液从仪器的__________ (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴1 mol/L 1H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体;
(4)本实验中可以循环利用的物质是_____________ 。

请回答下列问题:
(1)写出操作①、操作③的名称分别为:
(2)操作②选用CCl4的理由是
A.CCl4不溶于水 B.CCl4的密度比水大
C.碘在CCl4中比在水中溶解度更大 D.CCl4与碘水不反应
(3)用NaOH浓溶液反萃取后再加稀酸,可以分离I2和CCl4,有关化学方程式为:
碱性条件:3I2+6NaOH=5NaI+NaIO3+3H2O;
酸性条件:5NaI+NaIO3+3H2SO4=3Na2SO4+3I2+3H2O。
以下是反萃取过程的操作,请按要求填空:
①向装有I2的CCl4溶液的
②振荡至溶液的
③将含碘的碱溶液从仪器的
④边搅拌边加入几滴1 mol/L 1H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体;
(4)本实验中可以循环利用的物质是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】工业上从海水中提取液溴的部分流程如图:
浓缩海水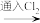 含
含 的水溶液
的水溶液 粗溴
粗溴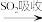 吸收液……
吸收液……
已知:溴的沸点为59℃,微溶于水,有毒性。
(1)某同学利用如图装置进行实验,通入氯气时,应关闭活塞_________ (填字母,下同),打开活塞_________ 。

(2)通入“热空气”时,可根据_________ (填现象)来简单判断热空气的流速。
(3)向浓缩海水中通入 发生反应的离子方程式为
发生反应的离子方程式为___________________ 。
浓缩海水
 含
含 的水溶液
的水溶液 粗溴
粗溴 吸收液……
吸收液……已知:溴的沸点为59℃,微溶于水,有毒性。
(1)某同学利用如图装置进行实验,通入氯气时,应关闭活塞

(2)通入“热空气”时,可根据
(3)向浓缩海水中通入
 发生反应的离子方程式为
发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X原子半径最小,Y形成物质种类最多,Q与X同主族,Z是地壳中含量最高的元素,R最外层电子数与周期数相等。请回答下列问题:
(1)写出R的原子结构示意图:____ 。
(2)五种元素原子半径由大到小的顺序是(写元素符号)___ 。
(3)X与Y能形成多种化合物,其中只含极性键且相对分子质量最小的物质是(写结构式)___ ,X和Z组成的化合物的化学式为___ 。
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A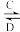 B(在水溶液中进行),其中,C是溶于水溶液显酸性的气体;D是淡黄色固体。写出C的电子式
B(在水溶液中进行),其中,C是溶于水溶液显酸性的气体;D是淡黄色固体。写出C的电子式____ ;D的电子式___ 。
①如果A、B均由三种元素组成,B为两性不溶物,则A B离子反应方程式为
B离子反应方程式为___ 。
②A、B均为盐溶液,如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。写出在A溶液中滴加过量稀盐酸的离子方程式_ 。
(1)写出R的原子结构示意图:
(2)五种元素原子半径由大到小的顺序是(写元素符号)
(3)X与Y能形成多种化合物,其中只含极性键且相对分子质量最小的物质是(写结构式)
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
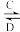 B(在水溶液中进行),其中,C是溶于水溶液显酸性的气体;D是淡黄色固体。写出C的电子式
B(在水溶液中进行),其中,C是溶于水溶液显酸性的气体;D是淡黄色固体。写出C的电子式①如果A、B均由三种元素组成,B为两性不溶物,则A
 B离子反应方程式为
B离子反应方程式为②A、B均为盐溶液,如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。写出在A溶液中滴加过量稀盐酸的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分。
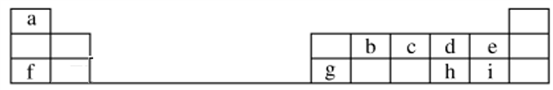
回答下列问题:
(1)元素b在元素周期表中的位置是________ 。
(2)元素e的负一价离子的结构示意图为________ ,与元素g的简单离子,二者的离子半径大小顺序为________ 。(用离子符号表示)
(3)元素i的气态氢化物比元素e的气态氢化物________ (填“稳定”或“不稳定”)。
(4)元素i的单质溶于元素f的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的电子式为______________ 。

回答下列问题:
(1)元素b在元素周期表中的位置是
(2)元素e的负一价离子的结构示意图为
(3)元素i的气态氢化物比元素e的气态氢化物
(4)元素i的单质溶于元素f的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的电子式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】几种元素在周期表中的位置如下,用化学用语 回答下列问题:
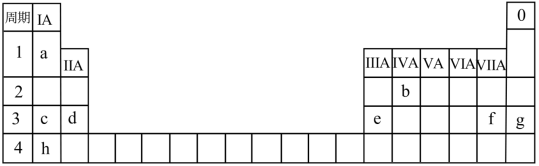
(1)表中所列元素,化学性质最不活泼的是___________ 。
(2)上图中,元素a与b形成的10 e-的分子是___________ 。
(3)元素c在空气中燃烧的产物中所含化学键有___________ 。
(4)d、e、h三种元素最高价氧化物对应水化物碱性最弱的是___________ ,其中h与水反应的化学方程式为___________ 。
(5)f单质的电子式为___________ 。
(6)德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。分析可知,铷在元素周期表中的位置是___________ ,关于铷的下列说法中正确的是___________ (填字母序号)。
a.与水反应比钠更剧烈b.单质具有很强氧化性
c. 在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱
在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱

(1)表中所列元素,化学性质最不活泼的是
(2)上图中,元素a与b形成的10 e-的分子是
(3)元素c在空气中燃烧的产物中所含化学键有
(4)d、e、h三种元素最高价氧化物对应水化物碱性最弱的是
(5)f单质的电子式为
(6)德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。分析可知,铷在元素周期表中的位置是
a.与水反应比钠更剧烈b.单质具有很强氧化性
c.
 在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱
在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】为了验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)

实验过程:
Ⅰ.打开弹簧夹,打开活塞 a,滴加浓盐酸
Ⅱ.当 B 和 C 中的溶液都变为黄色时,夹紧弹簧夹
Ⅲ.当 B 中溶液由黄色变为棕红色时,关闭活塞 a
Ⅳ.…
(1)A 中反应的化学方程式为:____ KMnO4+_____ HCl(浓)═____ KCl+____ MnCl2+____ Cl2↑+____ H2O,则氧化性 KMnO4________ Cl2(填“>”“<”或“=”).
(2)验证氯气的氧化性强于碘的实验现象是__________
(3)过程Ⅲ的实验目的是__________
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是__________ 。
(5)浸有 NaOH溶液的棉花团的作用是__________ 。此处发生 的化学方程式是__________ 。
(6)氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们阴离子的还原性强弱为:Cl- < Br- < CN- < SCN- < I-。试写出:
a.(CN)2与 KOH 反应的化学方程式__________ ;
b.在 NaBr 和 KSCN 的混合溶液中加入(CN)2的离子方程式__________ 。

实验过程:
Ⅰ.打开弹簧夹,打开活塞 a,滴加浓盐酸
Ⅱ.当 B 和 C 中的溶液都变为黄色时,夹紧弹簧夹
Ⅲ.当 B 中溶液由黄色变为棕红色时,关闭活塞 a
Ⅳ.…
(1)A 中反应的化学方程式为:
(2)验证氯气的氧化性强于碘的实验现象是
(3)过程Ⅲ的实验目的是
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是
(5)浸有 NaOH溶液的棉花团的作用是
(6)氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们阴离子的还原性强弱为:Cl- < Br- < CN- < SCN- < I-。试写出:
a.(CN)2与 KOH 反应的化学方程式
b.在 NaBr 和 KSCN 的混合溶液中加入(CN)2的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】探究同主族元素非金属性的递变规律
某研究性学习小组设计了一组实验来探究ⅦA族元素原子的得电子能力强弱规律。下图中A、B、C是三个可供选择制取氯气的装置,装置D的玻璃管中①、②处依次放置蘸有NaBr溶液、NaOH浓溶液的棉球。
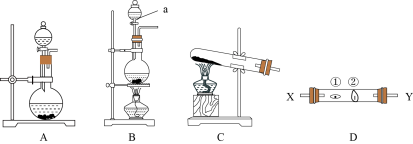
(1)写出装置B中仪器a的名称________________ 。
(2)实验室制取氯气还可采用如下原理:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,依据该反应原理选择_____________ (填“A”或“B”或“C”)装置制取氯气。
(3)反应装置的导气管连接装置D的X导管,①处发生反应的离子方程式为________________________ ;
(4)装置D中②处NaOH浓溶液的作用:________________________ ;写出对应的化学方程式________________ 。
某研究性学习小组设计了一组实验来探究ⅦA族元素原子的得电子能力强弱规律。下图中A、B、C是三个可供选择制取氯气的装置,装置D的玻璃管中①、②处依次放置蘸有NaBr溶液、NaOH浓溶液的棉球。

(1)写出装置B中仪器a的名称
(2)实验室制取氯气还可采用如下原理:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,依据该反应原理选择
(3)反应装置的导气管连接装置D的X导管,①处发生反应的离子方程式为
(4)装置D中②处NaOH浓溶液的作用:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某班同学想要设计实验验证元素性质变化规律,
I.第一组同学拟利用原电池反应检测金属的活动性顺序,设计如图甲所示原电池装置,用铝片和铜片作电极,电解质为H2SO4溶液,

(1)写出甲中负极的电极反应式:___________ 。此电池工作时导线中电流方向为:___________ (选填“铜→铝”或“铝→铜”)。
(2)乙同学将铜电极换成镁电极,如图乙所示,实验发现也可组成原电池,此时铝片上有气体产生,则此原电池中负极是___________ 。(填“镁片”或“铝片”)。
(3)由以上实验推断,当把A、B两种金属用导线连接后同时浸入稀硫酸溶液中,若B上发生还原反应,则A、B金属的活泼性可能是___________ (填“A>B”或“A<B”)。
II.为了验证元素周期律相关的结论,另一组同学也设计了一套实验方案,并记录了有关实验现象。
(4)方案①相关反应的离子方程式为___________ 。
(5)方案④相关反应的化学方程式为___________ ,由以上方案可知S、Cl、Br、I的非金属性由强到弱的顺序为___________ (用化学符号表示)。
(6)实验结论:周期表中元素的非金属性变化规律为___________ 。
I.第一组同学拟利用原电池反应检测金属的活动性顺序,设计如图甲所示原电池装置,用铝片和铜片作电极,电解质为H2SO4溶液,

(1)写出甲中负极的电极反应式:
(2)乙同学将铜电极换成镁电极,如图乙所示,实验发现也可组成原电池,此时铝片上有气体产生,则此原电池中负极是
(3)由以上实验推断,当把A、B两种金属用导线连接后同时浸入稀硫酸溶液中,若B上发生还原反应,则A、B金属的活泼性可能是
II.为了验证元素周期律相关的结论,另一组同学也设计了一套实验方案,并记录了有关实验现象。
| 实验方案 | 实验现象 |
| ①将新制氯水滴入NaBr溶液中,振荡后加入适量CCl4溶液,振荡,静置 | 分层,上层无色,下层橙红色 |
| ②将溴水滴入NaI溶液中,振荡后加入适量CCl4溶液,振荡,静置 | 分层,上层无色,下层紫红色 |
| ③将少量I2固体加入NaCl溶液中,振荡后加入适量淀粉溶液,振荡,静置 | 溶液变蓝色 |
| ④将少量I2固体加入Na2S溶液,振荡后静置 | 溶液变浑浊,出现淡黄色沉淀 |
(5)方案④相关反应的化学方程式为
(6)实验结论:周期表中元素的非金属性变化规律为
您最近一年使用:0次



