Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为______ ,基态Co原子的价层电子排布式为______ ,与Ni同周期且与Ni具有相同未成对电子数的元素有_______ 种。
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为____ 。Co(OH)3与盐酸反应有黄绿色气体生成,写出反应的离子方程式:_____ 。
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。
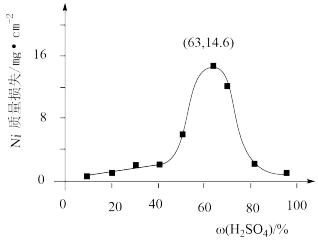
当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为_____ 。由于Ni与硫酸反应很慢,而与稀HNO3反应很快,工业上选用H2SO4和HNO3的混酸与Ni反应制备NiSO4,为了提高产物的纯度,在硫酸中添加HNO3的方式为_____ (填“一次过量”或“少量多次”),此法制备NiSO4的化学方程式为_____ 。
(1)Fe、Co、Ni在周期表中的位置为
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。

当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为
更新时间:2021-11-05 11:05:32
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】有4种元素:xA、yB、zC、uD,其中B的负二价离子和C的正一价离子均具有氩原子相同的核外电子排布,又已知x+y+z+u=64,u=x+5,根据以上条件进行推断:
(1)A原子的结构示意图_________ ,C+的离子结构示意图:_________ 。
(2)写出元素B的氢化物和D的单质之间发生置换反应的化学方程式:_________ 。由此得出元素B、D的单质的氧化性B________ D(填“>”、“<”)。
(3)A和D组成的化合物化学式是_________ ,其中阳离子与阴离子的电子层数相差___ 。
(1)A原子的结构示意图
(2)写出元素B的氢化物和D的单质之间发生置换反应的化学方程式:
(3)A和D组成的化合物化学式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学小组探究酸性条件下NO 、SO
、SO 、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
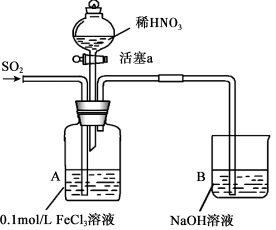
实验记录如表:
请回答下列问题:
(1)指出仪器a的名称_______ 。
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式_______ 。
(3)实验Ⅱ中发生反应的离子方程式是_______ 。
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是_______ 。(用语言叙述)。
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象是_______ 。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为_______ 。
 、SO
、SO 、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
、Fe3+三种微粒的氧化性强弱,设计如图实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
实验记录如表:
| 选项 | 实验操作 | 实验现象 |
| Ⅰ | 向A装置中通入一段时间SO2气体 | A中溶液最终变为浅绿色 |
| Ⅱ | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀 |
| Ш | 打开活塞a,将过量HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色 |
| Ⅳ | 取出Ш中少量A装置中的溶液,加入KSCN溶液 | 溶液变为红色 |
(1)指出仪器a的名称
(2)写出A装置中通入二氧化硫气体发生反应的离子方程式
(3)实验Ⅱ中发生反应的离子方程式是
(4)实验Ⅲ中,浅绿色溶液变为黄色的原因是
(5)若将实验Ⅳ改为:往A中通入空气,液面上方的现象是
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱顺序为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表为元素周期表的一部分,用化学用语回答下列问题:

(1)欲除去④中的杂质③,用离子方程式表示除杂过程_______ 。
(2)欲证明⑥单质的氧化性强于I2,可进行的实验操作是_______ ,观察到的现象是_______ ,有关反应的离子方程式是_______ 。
(3)③和水反应时,表面会形成一层氢氧化物膜阻碍内部金属与水继续反应,所以只有在_______ 的条件下,才能观察到镁与水反应产生气泡的缓慢过程。为避免酒精灯加热时产生的水蒸气的气泡干扰到对氢气的观察,可以把试管放在_______ 中加热。
(4)RO2分子的空间结构是_______ 形,通过现代实验手段(如_______ 等)可以测定某些分子的结构。
(5)用电子式表示②和⑦组成的化合物的形成过程_______ 。
(6)④的最高价氧化物对应的水化物是_______ 氢氧化物,说明④虽是金属,但已表现出一定的非金属性。④的最高价氧化物对应的水化物与氢氧化钠溶液反应的化学方程式是_______ 。

(1)欲除去④中的杂质③,用离子方程式表示除杂过程
(2)欲证明⑥单质的氧化性强于I2,可进行的实验操作是
(3)③和水反应时,表面会形成一层氢氧化物膜阻碍内部金属与水继续反应,所以只有在
(4)RO2分子的空间结构是
(5)用电子式表示②和⑦组成的化合物的形成过程
(6)④的最高价氧化物对应的水化物是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。
Ⅰ.活性炭纤维吸附法是工业提取碘单质的方法之一,其流程如图1所示:
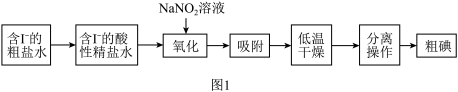
已知:a. 溶液只能将
溶液只能将 氧化成
氧化成 ,同时生成NO气体。
,同时生成NO气体。
b.酸性条件下, 会与
会与 反应生成
反应生成 和
和 。
。
(1)粗盐水中还含有 、
、 、
、 ,制成精盐水时所加试剂的顺序是___________(填标号)。
,制成精盐水时所加试剂的顺序是___________(填标号)。
(2)“氧化”过程中发生反应的离子方程式是___________ 。
(3)酸性 溶液是常用的氧化剂,但此过程中选择价格更贵的
溶液是常用的氧化剂,但此过程中选择价格更贵的 的原因是
的原因是___________ 。
(4)根据碘单质的特性,分离操作是___________ ,冷凝得粗碘。
Ⅱ.以金红石(主要成分为TiO₂)为原料制取海绵钛的工艺流程如图2所示:
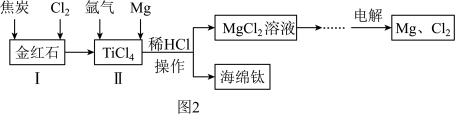
(5)高温条件下,反应1可生成一种可燃性气体,反应1的化学方程式是___________ 。
(6)上述流程中可循环利用的物质是___________ (填化学式),电解熔融 的化学方程式是
的化学方程式是___________ 。
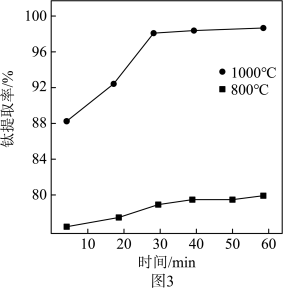
(7)反应2中钛的提取率在不同温度下随时间变化的曲线如图3,则反应最适宜的条件是___________ 。
Ⅰ.活性炭纤维吸附法是工业提取碘单质的方法之一,其流程如图1所示:

已知:a.
 溶液只能将
溶液只能将 氧化成
氧化成 ,同时生成NO气体。
,同时生成NO气体。b.酸性条件下,
 会与
会与 反应生成
反应生成 和
和 。
。(1)粗盐水中还含有
 、
、 、
、 ,制成精盐水时所加试剂的顺序是___________(填标号)。
,制成精盐水时所加试剂的顺序是___________(填标号)。A. 溶液、NaOH溶液、 溶液、NaOH溶液、 溶液、稀盐酸 溶液、稀盐酸 |
B.NaOH溶液、 溶液、 溶液、 溶液、稀盐酸 溶液、稀盐酸 |
C.NaOH溶液、 溶液、 溶液、 溶液、稀盐酸 溶液、稀盐酸 |
D. 溶液、 溶液、 溶液、NaOH溶液、稀盐酸 溶液、NaOH溶液、稀盐酸 |
(3)酸性
 溶液是常用的氧化剂,但此过程中选择价格更贵的
溶液是常用的氧化剂,但此过程中选择价格更贵的 的原因是
的原因是(4)根据碘单质的特性,分离操作是
Ⅱ.以金红石(主要成分为TiO₂)为原料制取海绵钛的工艺流程如图2所示:

(5)高温条件下,反应1可生成一种可燃性气体,反应1的化学方程式是
(6)上述流程中可循环利用的物质是
 的化学方程式是
的化学方程式是(7)反应2中钛的提取率在不同温度下随时间变化的曲线如图3,则反应最适宜的条件是

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为________________ 。
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为____________________ 。
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ·mol-1
写出肼和N2O4反应的热化学方程式________________________________________ 。
(4)肼-空气燃料电池是一种碱性电池,该电池放电时,正极的反应式为________________________________________ 。
(1)氮元素原子的L层电子数为
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ·mol-1
写出肼和N2O4反应的热化学方程式
(4)肼-空气燃料电池是一种碱性电池,该电池放电时,正极的反应式为
您最近一年使用:0次
【推荐3】为了从海带浸取液中提取碘,某同学设计了如图实验方案,解答下列问题:
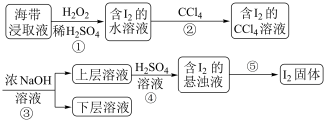
(1) 被称作绿色氧化剂的两个原因
被称作绿色氧化剂的两个原因_______ ;_______
(2)实验操作②的名称为_______ ,操作②需要的仪器除烧杯、玻璃棒外,尚缺少的玻璃仪器有_______ ,碘的 溶液位于
溶液位于_______ 层(填“上”或“下”),呈_______ 色。检验水层是否仍含碘单质的方法是_______ 。
(3)③是将富集在 中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为
中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为 ,接下来④发生的反应方程式为
,接下来④发生的反应方程式为_______ 。
(4)本实验中可以循环利用的物质是_______ 。

(1)
 被称作绿色氧化剂的两个原因
被称作绿色氧化剂的两个原因(2)实验操作②的名称为
 溶液位于
溶液位于(3)③是将富集在
 中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为
中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为 ,接下来④发生的反应方程式为
,接下来④发生的反应方程式为(4)本实验中可以循环利用的物质是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、 E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为___________ ,C的元素符号为___________ 。
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为___________
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为___________
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=___________ ;原子中能量最高的是___________ 电子。
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ ,___________ (填标号)
A.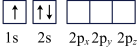 B.
B.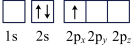 C.
C.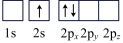 D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是___________ ,某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为___________ ,最高正价为___________ ,该原子位于元素周期表第___________ 周期第___________ 族,位于元素周期表___________ 区。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. C.
C. D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
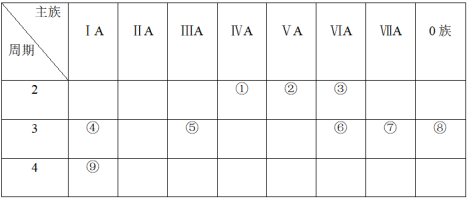
(1)在这些元素中,化学性质最不活泼的是:_______ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______ 。碱性最强的化合物的电子式是_______ 。
(3)最高价氧化物是两性氧化物的元素是_______ ;写出它的氧化物与氢氧化钠反应的离子方程式_______ 。
(4)用电子式表示元素④与⑥的化合物的形成过程:_______ ,该化合物属于_______ (填“共价”或“离子”)化合物。
(5)表示①与⑦的化合物的电子式_______ 。

(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素④与⑥的化合物的形成过程:
(5)表示①与⑦的化合物的电子式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】如图是元素周期表的另一种画法——塔式周期表,在上面标有部分族及部分元素。请回答下列问题:

(1)请在图上把过渡元素涂黑。_______
(2)已知A、B、C、D、E、F、G为元素周期表中短周期主族元素,且原于序数依次增大。A与E、D与F分别同主族,E、F、G同周期;A与D形成的化合物常温下为液态;B原子最外层电子数是次外层电子数的两倍。请回答下列问题:
①在如图塔式周期表相应位置标出上述属于碱金属和卤族元素的元素符号。____
②写出E与D形成含有非极性键化合物的电子式______ 。
③这些元素形成的最简单氢化物中,属于18电子的分子有____ (写化学式)
④A、D的单质和A、D、E形成的离子化合物的水溶液,在一定条件下可构成原电池,其中D的单质在___ 极发生反应,原电池反应中,A单质发生反应的电极反应式为_______ 这种电池相对于其它电池的优点是________ 。

(1)请在图上把过渡元素涂黑。
(2)已知A、B、C、D、E、F、G为元素周期表中短周期主族元素,且原于序数依次增大。A与E、D与F分别同主族,E、F、G同周期;A与D形成的化合物常温下为液态;B原子最外层电子数是次外层电子数的两倍。请回答下列问题:
①在如图塔式周期表相应位置标出上述属于碱金属和卤族元素的元素符号。
②写出E与D形成含有非极性键化合物的电子式
③这些元素形成的最简单氢化物中,属于18电子的分子有
④A、D的单质和A、D、E形成的离子化合物的水溶液,在一定条件下可构成原电池,其中D的单质在
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D是短周期元素,A元素的最高价氧化物对应的水化物与它的气态氢化物反应得到离子化合物,1 mol该化合物含有42 mol电子;B原子的最外层电子排布式为nsnnp2n。C、D两原子的最外层电子数分别是内层电子数的一半。C元素是植物生长的营养元素之一。试写出:
(1)A、B元素形成的酸酐的化学式:______________ 。
(2)D元素的单质与水反应的化学方程式:____________________________ 。
(3)A、C元素气态氢化物的稳定性大小:________ <________ (用化学式表示)。
(1)A、B元素形成的酸酐的化学式:
(2)D元素的单质与水反应的化学方程式:
(3)A、C元素气态氢化物的稳定性大小:
您最近一年使用:0次
【推荐2】研究发现,在CO2低压合成甲醇反应CO23H2CH3OHH2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为________ 。元素Mn与O中,第一电离能较大的是________ ,基态原子核外未成对电子数较多的是________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为________ 和________ 。
(3)比较CO2和H2O沸点________ ,原因是________ 。
(4)MnNO3中的化学键除了σ键外,还存在________ 。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)比较CO2和H2O沸点
(4)MnNO3中的化学键除了σ键外,还存在
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】我国科学家制备的NiO/Al2O3/Pt催化剂能实现氨硼烷(H3NBH3)高效制备氢气的目的,制氢原理:H3NBH3+4CH3OH NH4B(OCH3)4+3H2↑。请回答下列问题:
NH4B(OCH3)4+3H2↑。请回答下列问题:
(1)基态氮原子的价电子排布式为_______ 。
(2)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因为_______ 。
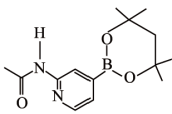
(3)某有机硼化合物的结构简式如图所示,其中氮原子的杂化轨道类型为_______ 。
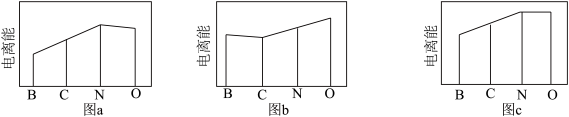
(4)图a、b、c分别表示B、C、N、O的逐级电离能变化趋势(纵坐标的标度不同)。第二电离能的变化图是_______ (填标号)。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与EDTA形成的螯合物的结构如图所示,

1个该配合物中通过螯合作用形成的配位键有_______ 个,在形成配位键前后C-N-C键角将_______ (填“增大"“减少”或“不变”)。
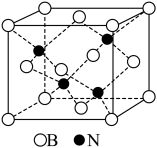
(6)BN晶体的晶胞如图所示,B、N的原子半径分别为apm和bpm,密度为2.25g·cm-3,阿伏伽德罗常数的值为NA,BN晶胞中原子的体积占晶胞体积的百分率为_______ 。
 NH4B(OCH3)4+3H2↑。请回答下列问题:
NH4B(OCH3)4+3H2↑。请回答下列问题:(1)基态氮原子的价电子排布式为
(2)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因为
(3)某有机硼化合物的结构简式如图所示,其中氮原子的杂化轨道类型为

(4)图a、b、c分别表示B、C、N、O的逐级电离能变化趋势(纵坐标的标度不同)。第二电离能的变化图是

(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与EDTA形成的螯合物的结构如图所示,

1个该配合物中通过螯合作用形成的配位键有
(6)BN晶体的晶胞如图所示,B、N的原子半径分别为apm和bpm,密度为2.25g·cm-3,阿伏伽德罗常数的值为NA,BN晶胞中原子的体积占晶胞体积的百分率为

您最近一年使用:0次



