下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
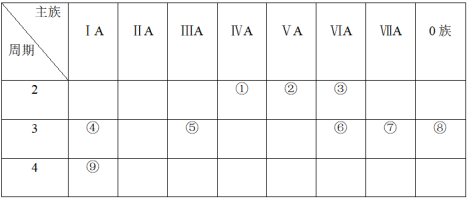
(1)在这些元素中,化学性质最不活泼的是:_______ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______ 。碱性最强的化合物的电子式是_______ 。
(3)最高价氧化物是两性氧化物的元素是_______ ;写出它的氧化物与氢氧化钠反应的离子方程式_______ 。
(4)用电子式表示元素④与⑥的化合物的形成过程:_______ ,该化合物属于_______ (填“共价”或“离子”)化合物。
(5)表示①与⑦的化合物的电子式_______ 。

(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素④与⑥的化合物的形成过程:
(5)表示①与⑦的化合物的电子式
更新时间:2022-12-20 21:05:43
|
相似题推荐
【推荐1】化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的电子排布式为_______ ,Y的轨道表示式为_______ ;
(2)ZX2的分子式是_______ ,YX2电子式是_________ ;
(3)Y与Z形成的化合物的分子式是_______ 。
(1)X的电子排布式为
(2)ZX2的分子式是
(3)Y与Z形成的化合物的分子式是
您最近一年使用:0次
【推荐2】元素周期表前四周期的A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级的电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有5个未成对电子。
(1)写出下列元素的名称:
C___________ ;D_______ ;E_______ 。
(2)基态C原子的电子排布图为_____ 。
(3)当n=2时,B的最简单气态氢化物的电子式为_____ ,BC2分子的结构式为_____ ;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是_________ 。
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是_____ (用元素符号表示)。
(5)E元素在元素周期表中的位置是______ ,其最高价氧化物的化学式是_____ 。
(1)写出下列元素的名称:
C
(2)基态C原子的电子排布图为
(3)当n=2时,B的最简单气态氢化物的电子式为
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是
(5)E元素在元素周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的符号:X_______ 、Y_______ 、Z_______ 、W_______
(2)X与Y所形成的化合物的化学式为_______ ,是_______ 化合物。用电子式表示其形成过程_______ 。
(1)X、Y、Z、W四种元素的符号:X
(2)X与Y所形成的化合物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某研究性学习小组用不纯的氧化铝(杂质为Fe2O3)为原料,设计了冶炼铝的以下工艺流程(部分反应产物没有标出):
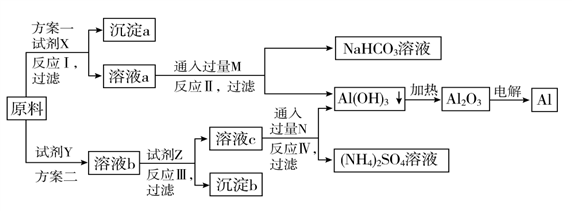
(1)试剂X的化学式为________ ,反应Ⅰ的离子方程式是________________________ 。实验室配制480 mL 1 mol·L-1X的溶液必须用到玻璃仪器除烧杯、玻璃棒、试剂瓶、胶头滴管外,还有________________ 。
(2)通入过量的M、N化学式分别为________ 、________ ,反应Ⅱ、Ⅳ的离子方程式分别____________________________ 、______________________ 。
(3)按照方案设计,试剂Z的作用是调节溶液的pH为3.1,以生成沉淀b[Fe(OH)3]。试剂Z可选用________ (填字母)。
A.Al2O3 B.H2SO4
C.NaOH D.Al(OH)3
(4)从实际工业的角度,你认为方案________ 更合理,理由是__________________ 。

(1)试剂X的化学式为
(2)通入过量的M、N化学式分别为
(3)按照方案设计,试剂Z的作用是调节溶液的pH为3.1,以生成沉淀b[Fe(OH)3]。试剂Z可选用
A.Al2O3 B.H2SO4
C.NaOH D.Al(OH)3
(4)从实际工业的角度,你认为方案
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如下。

下表列出了相关金属离子生成氢氧化物沉淀的pH:
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有__________ 种。
(2)Cr2O3与稀硫酸反应的化学方程式为_________________ 。
(3)第一次滴加氨水调节pH范围为__________ 。
(4)第二次滴加氨水调节pH为6.8~8.8的目的是__________ ,Cr(OH)3与Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:_________________ 。

下表列出了相关金属离子生成氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 2.3 | 8.8 | 4.9 | 7.5 |
| 沉淀完全的pH | 4.1 | 10.4 | 6.8 | 9.7 |
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有
(2)Cr2O3与稀硫酸反应的化学方程式为
(3)第一次滴加氨水调节pH范围为
(4)第二次滴加氨水调节pH为6.8~8.8的目的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,根据表中给出的12种元素,回答下列问题:
(1)①~⑫中,元素的气态氢化物与其最高价氧化物对应的水化物可直接化合生成一种盐,该元素是_______ (写元素符号)。
(2)元素的非金属性:②_______ ③(填“>”或“<”)。
(3)元素④与⑥按原子个数比为1:2形成的化合物的电子式可表示为_______ 。
(4)②、⑥、⑧三种元素的原子半径由大到小的顺序是_______ 。(用元素符号表示)
(5)元素⑧、⑨、⑪的最高价氧化物对应的水化物的酸性由强到弱的顺序是_______ 。(用化学式表示)。
(6)写出元素⑥和⑦的最高价氧化物对应的水化物相互反应的离子方程式:_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | Ⅶ | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)元素的非金属性:②
(3)元素④与⑥按原子个数比为1:2形成的化合物的电子式可表示为
(4)②、⑥、⑧三种元素的原子半径由大到小的顺序是
(5)元素⑧、⑨、⑪的最高价氧化物对应的水化物的酸性由强到弱的顺序是
(6)写出元素⑥和⑦的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:
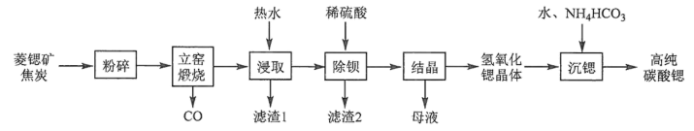
Sr(OH)2在水中的溶解度
(1)元素Sr位于元素周期表第_______ 周期第_______ 族。
(2)菱锶矿、焦炭混合粉碎的目的是_______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为_______ 。进行煅烧反应的立窑衬里应选择_______ (填“石英砂砖”或“碱性耐火砖”)。

Sr(OH)2在水中的溶解度
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)元素Sr位于元素周期表第
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】原子序数依次增大的A、B、C、D、E、F六种元素均为前四周期元素,A是形成化合物种类最多的元素,B与A同周期,其原子核外s能级上的电子总数与p能级上的电子总数相等,C为第3周期元素,其离子半径在该周期中最小,D原子核外p能级上的电子总数比s能级上的电子总数多2,E元素位于元素周期表中的第8列,F的单质为紫红色金属。回答下列问题:
(1)D在元素周期表中的位置为___________ 。
(2)A元素的原子核外共有___________ 种不同运动状态的电子;B元素基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)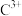 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为___________ 。
(4)E元素位于元素周期表中___________ 区(按电子排布分区),其基态原子价电子轨道表示式为___________ 。
(5)基态F原子的核外电子排布式为___________ ,其基态原子核外填充有电子的能量最高的电子层的符号为___________ ,该电子层上具有的原子轨道数是___________ 。
(1)D在元素周期表中的位置为
(2)A元素的原子核外共有
(3)
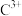 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为(4)E元素位于元素周期表中
(5)基态F原子的核外电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】元素周期表是学习和研究化学的重要工具。
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
①Al原子的核电荷数为____ 。②钠离子的结构示意图为____ 。
③周期表中磷元素的有关信息为 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是____ 。
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。
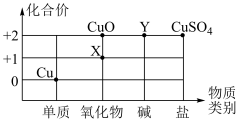
①写出物质 X 的化学式:________________ 。
②写出由物质 Y 转化为 CuSO4的化学反应方程式:_______________ 。
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是_________________ 。
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
| 第1周期 | H | He | ||||||
| 第2周期 | Li | Be | B | C | N | O | F | Ne |
| 第3周期 | Na | Mg | Al | Si | P | S | Cl | Ar |
①Al原子的核电荷数为
③周期表中磷元素的有关信息为
 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。

①写出物质 X 的化学式:
②写出由物质 Y 转化为 CuSO4的化学反应方程式:
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】有X、Y、Z、R四种短周期元素,Y、Z、R同周期。相关信息如下:
(1)Z元素在周期表的位置是_____ ,Y、Z、R简单离子的半径从大到小的顺序是__________ (用离子符号表示);
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。则甲的结构式为___________ ;
(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色。则Y2R2的电子式为_______ ,写出乙溶液在空气中变质过程的化学方程式___________________________ 。
| 相关信息 | |
| X | 单质为双原子分子。若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y | 含Y元素的物质焰色反应为黄色 |
| Z | 同周期元素中原子半径最小 |
| R | R元素原子的最外层电子数是K层电子数的3倍 |
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。则甲的结构式为
(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色。则Y2R2的电子式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】如图所示标出的是元素周期表的一部分元素,据图回答下列问题(用元素符号表示)。
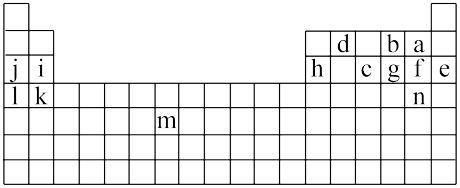
(1)图中用字母标出的14种元素中,金属性最强的是___ ,非金属性最强的是__ ,其单质的电子式___ 。
(2)b在周期表中的位置___ ,b、g气态氢化物中热稳定性最强的是___ ,结构式为___ 。
(3)j的最高价氧化物的水化物化学式___ ,该化合物中含有___ 键、___ 键,h与j的最高价氧化物的水化物反应的离子方程式___ 。

(1)图中用字母标出的14种元素中,金属性最强的是
(2)b在周期表中的位置
(3)j的最高价氧化物的水化物化学式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】已知:X、Y、Z、W是1~18号元素中的四种常见元素,其相关信息见下表:
请根据表中相关信息,回答下列问题:
(1)Y位于元素周期表第_______ 周期第_______ 族,Y和Z的最高价氧化物对应水化物的酸性较强的是_______ (填化学式)。
(2)Z的简单阴离子的电子式为_______ 。
(3)请用电子式描述W与X形成碱性氧化物的过程:_______ 。
(4)Y的氧化物与气态氢化物可发生归中反应,请写出相关化学反应方程式:_______ 。
| 元素 | 相关信息 |
| X | X元素原子的最外层电子数是次外层电子数的3倍 |
| Y | Y元素的最高正价与最低负价的代数和为4 |
| Z | Z和Y同周期,Z的非金属性大于Y |
| W | W的一种核素的质量数为23,中子数为12 |
(1)Y位于元素周期表第
(2)Z的简单阴离子的电子式为
(3)请用电子式描述W与X形成碱性氧化物的过程:
(4)Y的氧化物与气态氢化物可发生归中反应,请写出相关化学反应方程式:
您最近一年使用:0次



