解题方法
1 . 下表是元素周期表的一部分,针对编号①~⑫元素,回答下列有关问题:
(1)在这些元素中,非金属性最强的元素是_______ (填元素符号,下同),最不活泼的元素是_______ 。
(2)写出元素①对应气态氢化物的化学式和电子式:_______ 、_______ 。
(3)在元素③和④中,单质与水反应较剧烈的是_______ (填元素符号),它与水反应的化学方程式是_______ 。
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是_______ (填化学式)。
(5)能证明⑧和⑫单质氧化性强弱的实验事实 用离子方程式表示)是
用离子方程式表示)是_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |  |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)写出元素①对应气态氢化物的化学式和电子式:
(3)在元素③和④中,单质与水反应较剧烈的是
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是
(5)能证明⑧和⑫单质氧化性强弱的实验事实
 用离子方程式表示)是
用离子方程式表示)是
您最近一年使用:0次
名校
解题方法
2 . 短周期元素G、M、W、X、Y、Z的原子半径及其最高正化合价随原子序数递增的变化如图所示:

| A.碱性:GOH>XOH | B.还原性: HW> HZ>H2Y |
| C.酸性:HZO4<H2YO4 | D.离子半径:M3->W->X+ |
您最近一年使用:0次
2020-11-09更新
|
650次组卷
|
6卷引用:福建省泉州市培元中学2020-2021学年高二下学期期中考试化学试题
名校
解题方法
3 . 下列事实不能说明元素的金属性或非金属性相对强弱的是
| 选项 | 事实 | 推论 |
| A | 与冷水反应,Na比Mg剧烈 | 金属性:Na>Mg |
| B | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca>Mg |
| C | 氧化性:HClO>H2CO3 | 金属性:Cl>C |
| D | 热稳定性强弱:HBr>HI | 非金属性:Br>I |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-18更新
|
488次组卷
|
9卷引用:【全国百强校】福建省三明市第一中学2019届高三上学期期中考试化学试题
【全国百强校】福建省三明市第一中学2019届高三上学期期中考试化学试题山东省潍坊市2019-2020学年高一下学期4月阶段考试化学试题(已下线)模块六 物质结构与元素周期律(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第14讲 元素周期律和元素周期表(练) — 2022年高考化学一轮复习讲练测(新教材新高考)江苏省淮安市车桥中学2021-2022学年高二上学期入学调研(A)化学试题(已下线)《新教材变化解读及考法剖析 》第四章 物质结构 元素周期律(人教版2019必修第一册)(已下线)专题16 元素周期律和元素周期表(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第14讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(新教材新高考)广东省云浮市罗定实验中学2022-2023学年高一下学期第一次月考化学试题
解题方法
4 . 主族元素W、X、Y、Z的原子序数依次增加,且均不超过20。W、X、Y最外层电子数之和为15, 是实验室常用的一种化学试剂。下列说法中错误的是( )
是实验室常用的一种化学试剂。下列说法中错误的是( )
 是实验室常用的一种化学试剂。下列说法中错误的是( )
是实验室常用的一种化学试剂。下列说法中错误的是( )| A.Z2Y的水溶液呈碱性 |
| B.最简单氢化物沸点高低为:X>W |
| C.常见单质的氧化性强弱为:W>Y |
D. 中各原子最外层均满足8电子稳定结构 中各原子最外层均满足8电子稳定结构 |
您最近一年使用:0次
2020-03-14更新
|
658次组卷
|
5卷引用:福建省厦门市2020届高三毕业班五月质量检查理综化学试题
福建省厦门市2020届高三毕业班五月质量检查理综化学试题福建省厦门市2020届高三高考化学模拟(5月份)理综化学试题武汉市2020届高中毕业生学生质量检测化学试题(已下线)专题06 物质结构 元素周期律-2020年高考真题和模拟题化学分项汇编(已下线)易错07 元素周期律-备战2021年高考化学一轮复习易错题
解题方法
5 . 已知Te为第五周期第ⅥA族元素。下列结论错误的是
A.粒子半径: |
B.氧化性: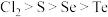 |
C.酸性: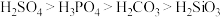 |
D.金属性: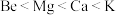 |
您最近一年使用:0次
2024-03-09更新
|
244次组卷
|
4卷引用:福建省漳州市第五中学2023-2024学年高一下学期第一次月考化学试卷
6 . 下表为元素周期表的一部分,表中所列的每个字母分别代表一种元素。
回答下列问题:
(1)元素f的原子结构示意图为___________ 。
(2)a与元素c和g形成的简单氢化物中稳定性强的是___________ 。(写化学式)
(3)由上述元素形成的最高价氧化物对应水化物中,酸性最强的是___________ (填化学式)。
(4) 的电子式为
的电子式为___________ 。
(5)元素d的最高价氧化物对应的水化物与元素e的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(6)c、d、e的简单离子半径由大到小的顺序为___________ 。(用离子符号表示)
(7)i与d形成的原子个数比为1:1的化合物中含有的化学键类型为___________ 。
(8)下列事实能说明d元素原子的失电子能力比e强的是___________(填标号)
| a | ||||||||
| b | i | c | ||||||
| d | e | f | g | |||||
| h | …… | |||||||
(1)元素f的原子结构示意图为
(2)a与元素c和g形成的简单氢化物中稳定性强的是
(3)由上述元素形成的最高价氧化物对应水化物中,酸性最强的是
(4)
 的电子式为
的电子式为(5)元素d的最高价氧化物对应的水化物与元素e的最高价氧化物对应的水化物反应的离子方程式为
(6)c、d、e的简单离子半径由大到小的顺序为
(7)i与d形成的原子个数比为1:1的化合物中含有的化学键类型为
(8)下列事实能说明d元素原子的失电子能力比e强的是___________(填标号)
A.单质的熔点: |
B.简单阳离子的氧化性: |
| C.常温下,d单质能与水剧烈反应而e不能 |
D.相同物质的量的d、e单质分别与足量盐酸反应,生成的 的量: 的量: |
您最近一年使用:0次
名校
解题方法
7 . 某化合物(结构如图所示)可用作酿造酵母的培养剂、强化剂、膨松剂、发酵助剂。已知X、Y、Z、W为元素周期表中前20号元素且位于不同周期,原子序数依次增大,Y为地壳中含量最高的元素。下列有关说法正确的是


| A.Y分别与X、Z、W三种元素均可形成至少两种化合物 |
B.单质的氧化性: |
| C.Z最高价氧化物对应水化物的酸性强于硫酸 |
| D.X与Z形成的最简单化合物的沸点比X与Y形成的最简单化合物的沸点高 |
您最近一年使用:0次
2023-01-08更新
|
306次组卷
|
3卷引用:福建省厦门市翔安第一中学2023-2024学年高三上学期10月月考化学试题
福建省厦门市翔安第一中学2023-2024学年高三上学期10月月考化学试题安徽省皖北县中2022-2023学年高三上学期第一次五校联考化学试题(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题11-16)
名校
8 . 下列性质的比较,错误的是
A.稳定性  | B.酸性 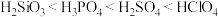 |
C.原子半径 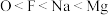 | D.氧化性 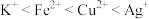 |
您最近一年使用:0次
名校
解题方法
9 . 已知X、Y、Z、W、M是同一短周期的五种主族元素。单质 具有强氧化性,可用于杀菌消毒。五种元素组成的盐是一种新型电池的电解质,结构如图所示。下列说法不正确的是
具有强氧化性,可用于杀菌消毒。五种元素组成的盐是一种新型电池的电解质,结构如图所示。下列说法不正确的是
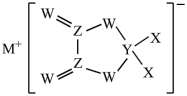
 具有强氧化性,可用于杀菌消毒。五种元素组成的盐是一种新型电池的电解质,结构如图所示。下列说法不正确的是
具有强氧化性,可用于杀菌消毒。五种元素组成的盐是一种新型电池的电解质,结构如图所示。下列说法不正确的是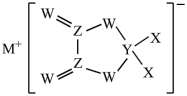
| A.原子半径:M>Y>Z>W>X | B.最高价氧化物对应水化物的酸性:Y>Z |
C. 中,W的化合价为+2价 中,W的化合价为+2价 | D.阴离子中四种元素的原子均满足8电子稳定结构 |
您最近一年使用:0次
2022-11-13更新
|
158次组卷
|
2卷引用:福建申宁德市部分达标校中学2022-2023学年高三上学期期中联考化学试题
名校
10 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。

(1)元素Ga在元素周期表中的位置为:___ (写明周期和族)。
(2)Sn的最高正价为___ ,Cl的最高价氧化物对应水化物的化学式为___ ,As的气态氢化物为___ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是___ (填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
③氢化物的还原性:H2O___ H2S(填“>”、“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找___ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(5)①Se2Cl2常用作分析试剂,其电子式为___ 。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是___ (填字母)。
A.原子半径:In>Se
B.In的金属性比Se强
C.In的金属性比Al弱
D.硒化铟的化学式为InSe2
③工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___ 。
(6)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
(4)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(5)①Se2Cl2常用作分析试剂,其电子式为
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:In>Se
B.In的金属性比Se强
C.In的金属性比Al弱
D.硒化铟的化学式为InSe2
③工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
(6)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
| 实验步骤 | 实验现象与结论 |
| 在试管中加入 | 现象: |
您最近一年使用:0次



