下表是元素周期表的一部分,针对编号①~⑫元素,回答下列有关问题:
(1)在这些元素中,非金属性最强的元素是_______ (填元素符号,下同),最不活泼的元素是_______ 。
(2)写出元素①对应气态氢化物的化学式和电子式:_______ 、_______ 。
(3)在元素③和④中,单质与水反应较剧烈的是_______ (填元素符号),它与水反应的化学方程式是_______ 。
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是_______ (填化学式)。
(5)能证明⑧和⑫单质氧化性强弱的实验事实 用离子方程式表示)是
用离子方程式表示)是_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |  |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)写出元素①对应气态氢化物的化学式和电子式:
(3)在元素③和④中,单质与水反应较剧烈的是
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是
(5)能证明⑧和⑫单质氧化性强弱的实验事实
 用离子方程式表示)是
用离子方程式表示)是
更新时间:2024-05-26 17:46:42
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E五种元素的原子序数均小于18,其原子的电子层结构的信息如下表,请根据信息回答下列问题:
(1)C的元素名称是_______ 。
(2)元素B形成的正离子的结构示意图_______ 。
(3)元素E负离子的电子式可能是_______ 、_______
(4)写出比A离子的电子少8个的两核负离子和五核正离子的化学式_______ 、_______
(5)元素D与氮元素形成化合物的化学式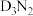 ,将此化合物投入水中,发生复分解反应,此反应的化学方程式是
,将此化合物投入水中,发生复分解反应,此反应的化学方程式是_______ 。
(6)若将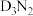 投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:
投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:_______ 、_______
(7)向 溶液中逐滴加入
溶液中逐滴加入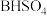 溶液,未看到有气泡产生,但溶液中
溶液,未看到有气泡产生,但溶液中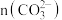 减小,此过程中反生的化学方程式是
减小,此过程中反生的化学方程式是_______ 。继续滴加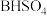 溶液,有气体放出,写出此时反生的化学方程式:
溶液,有气体放出,写出此时反生的化学方程式:_______ 。
| 元素符号 | 元素原子的电子层结构信息 |
| A | 原子M层比C原子L层多3个电子 |
| B | 带1个电荷的正离子的最外层电子数比电子层数多6 |
| C | 原子最外层电子数为K层电子数的2倍 |
| D | 原子M层和最内层电子数之和等于B原子L层电子数的1/2 |
| E | 原子最外层电子数是最内层的3倍 |
(2)元素B形成的正离子的结构示意图
(3)元素E负离子的电子式可能是
(4)写出比A离子的电子少8个的两核负离子和五核正离子的化学式
(5)元素D与氮元素形成化合物的化学式
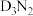 ,将此化合物投入水中,发生复分解反应,此反应的化学方程式是
,将此化合物投入水中,发生复分解反应,此反应的化学方程式是(6)若将
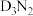 投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:
投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:(7)向
 溶液中逐滴加入
溶液中逐滴加入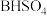 溶液,未看到有气泡产生,但溶液中
溶液,未看到有气泡产生,但溶液中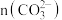 减小,此过程中反生的化学方程式是
减小,此过程中反生的化学方程式是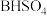 溶液,有气体放出,写出此时反生的化学方程式:
溶液,有气体放出,写出此时反生的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】元素周期表1~20号部分主族元素的原子半径与原子序数的关系如图,根据所学知识回答下列问题。

(1)焰色反应实验时透过蓝色钴玻璃能观察到紫色火焰的元素在周期表中的位置___________ 。
(2)d、e、f、h四种元素形成简单离子的半径由大到小的顺序是___________ (用离子符号填写)。
(3)c的简单氢化物与n的简单氢化物反应生成产物的电子式:___________ 。
(4)卤族元素大量存在于海洋中,获取 单质的过程中,需要利用m的一种氧化物富集,写其反应的离子方程式:
单质的过程中,需要利用m的一种氧化物富集,写其反应的离子方程式:___________ 。
(5)已知某些不同族元素的性质也有一定的相似性,如元素b与元素h有相似的性质。写出元素b的氢氧化物与NaOH溶液反应的离子方程式:___________ 。
(6)砷(As)的化合物可用于杀虫及医疗。
①As的原子结构示意图为___________ 。
②Y由d、f、n三种元素组成,是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为___________ 。
(7)从原子结构的角度,解释f、g、h元素金属性变化的原因:___________ 。

(1)焰色反应实验时透过蓝色钴玻璃能观察到紫色火焰的元素在周期表中的位置
(2)d、e、f、h四种元素形成简单离子的半径由大到小的顺序是
(3)c的简单氢化物与n的简单氢化物反应生成产物的电子式:
(4)卤族元素大量存在于海洋中,获取
 单质的过程中,需要利用m的一种氧化物富集,写其反应的离子方程式:
单质的过程中,需要利用m的一种氧化物富集,写其反应的离子方程式:(5)已知某些不同族元素的性质也有一定的相似性,如元素b与元素h有相似的性质。写出元素b的氢氧化物与NaOH溶液反应的离子方程式:
(6)砷(As)的化合物可用于杀虫及医疗。
①As的原子结构示意图为
②Y由d、f、n三种元素组成,是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
(7)从原子结构的角度,解释f、g、h元素金属性变化的原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E是中学化学常见单质, X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系 (反应物和产物中的H2O已略去):
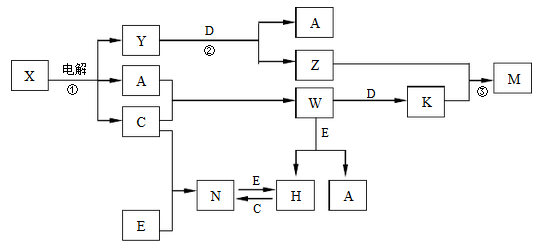
(1)Y的电子式为____________ ,构成E单质的元素在周期表中的位置_____________ 。
(2)反应②的离子方程式为_____________________ 。
(3)足量C通入Y的溶液中可得到一种常见的消毒剂。在该消毒剂中通入少量CO2可得一种酸式盐,从酸性强弱角度请你写出得到的结论:_______________________ 。
(4)①写出检验N中阳离子常用的试剂名称___________________ ,N也可用来净水,请写出相关离子方程式________________________ 。
②H的溶液在空气中久置,会变浑浊,请写出相关离子方程式_____________
(5)C可用来制取漂白粉,为测定漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为_____________ (不考虑生成CaSO4):
静置。待完全反应后,用1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为__________ (保留到小数点后两位)。

(1)Y的电子式为
(2)反应②的离子方程式为
(3)足量C通入Y的溶液中可得到一种常见的消毒剂。在该消毒剂中通入少量CO2可得一种酸式盐,从酸性强弱角度请你写出得到的结论:
(4)①写出检验N中阳离子常用的试剂名称
②H的溶液在空气中久置,会变浑浊,请写出相关离子方程式
(5)C可用来制取漂白粉,为测定漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为
静置。待完全反应后,用1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
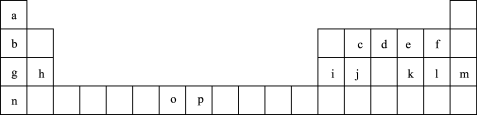
(1)基态o原子的外围电子排布图为_______ ;基态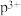 的最外层电子排布式为
的最外层电子排布式为_______ ;n的原子结构示意图为_______ 。表中所列元素的原子中,没有未成对电子的元素有_______ 种。
(2)原子序数为52的元素x在元素周期表中的位置为_______ 。
(3)上表中o、p两个字母表示的元素的第三电离能分别为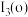 和
和 ,则
,则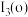
_______  (填“>”或“<”)。理由是
(填“>”或“<”)。理由是_______ 。
(4)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为_______ (用元素符号表示),第一电离能由大到小排序_______ (用元素符号表示)。

(1)基态o原子的外围电子排布图为
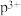 的最外层电子排布式为
的最外层电子排布式为(2)原子序数为52的元素x在元素周期表中的位置为
(3)上表中o、p两个字母表示的元素的第三电离能分别为
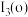 和
和 ,则
,则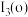
 (填“>”或“<”)。理由是
(填“>”或“<”)。理由是(4)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是部分元素周期表的结构图,表中每一个序号代表一种元素。请根据要求回答下列问题。
(1)以上元素中金属性最强的元素符号是___________ 。
(2)元素④、⑤所形成的简单离子半径较大的是___________ (用化学符号表示)。
(3)以上元素的最高价氧化物对应的水化物中,酸性最强的酸是___________ (填化学式)。
(4)A、B均为以上某两种元素组成的含四个原子核的分子,A中有10个电子,B中有18个电子,则A的电子式___________ ,B的分子式___________ 。
(5)由①、③、⑧三种元素以原子个数比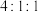 形成的化合物中含有的化学键类型是
形成的化合物中含有的化学键类型是___________ 。
(6)元素⑤、⑥的最高价氧化物对应水化物之间反应的离子方程式为___________ 。
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ | ⑧ | |||||
(2)元素④、⑤所形成的简单离子半径较大的是
(3)以上元素的最高价氧化物对应的水化物中,酸性最强的酸是
(4)A、B均为以上某两种元素组成的含四个原子核的分子,A中有10个电子,B中有18个电子,则A的电子式
(5)由①、③、⑧三种元素以原子个数比
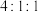 形成的化合物中含有的化学键类型是
形成的化合物中含有的化学键类型是(6)元素⑤、⑥的最高价氧化物对应水化物之间反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表标出的是元素周期表的一部分元素。
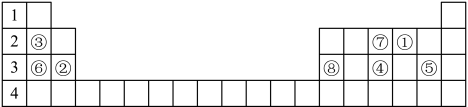
根据上表回答下列问题。
(1)元素①的原子序数是________ ,由元素①构成三原子单质的分子的化学式是__________ 。
(2)元素④与⑦相比,____ 元素的原子半径较大,____ 元素的氢化物更稳定(用元素符号填写)。
(3)元素③与⑥相比,最高价氧化物对应水化物碱性较大的是________ (填碱的化学式)。
(4)元素②和⑧的氧化物常用做耐火材料。元素②的氧化物的化学式是____________ ,元素⑧的氢氧化物与烧碱溶液反应的化学方程式是_____________________________ 。
(5)如图,将潮湿的由元素⑤构成的单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是______ 。

a.稀硫酸 b.浓硫酸 c.水 d.饱和食盐水

根据上表回答下列问题。
(1)元素①的原子序数是
(2)元素④与⑦相比,
(3)元素③与⑥相比,最高价氧化物对应水化物碱性较大的是
(4)元素②和⑧的氧化物常用做耐火材料。元素②的氧化物的化学式是
(5)如图,将潮湿的由元素⑤构成的单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是

a.稀硫酸 b.浓硫酸 c.水 d.饱和食盐水
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的正二价阳离子与C的负二价阴离子具有相同的电子层结构。AC2为非极性分子。B、C的简单氢化物的沸点比它们同族相邻周期元素的简单氢化物的沸点高。人体缺E元素会得软骨病,D与E位于同主族。请回答下列问题:
(1)A、B、C非金属性由强到弱的顺序为_____________________________ 。
E在元素周期表中的位置是________ (用元素符号表示)。
(2)C的一种氢化物是绿色氧化剂,其电子式是__________________________ 。
(3)B的简单氢化物的沸点比它的同族相邻周期元素的简单氢化物的沸点高,理由是_______________________________________________ 。B的简单氢化物溶于水的电离方程式为_____________________________________________________
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是___________________________________________ 。
(1)A、B、C非金属性由强到弱的顺序为
E在元素周期表中的位置是
(2)C的一种氢化物是绿色氧化剂,其电子式是
(3)B的简单氢化物的沸点比它的同族相邻周期元素的简单氢化物的沸点高,理由是
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表列出 八种元素在周期表中的位置:
八种元素在周期表中的位置:
回答下列问题:
(1) 、
、 、
、 三种元素中,原子半径最大的是
三种元素中,原子半径最大的是___________ (填元素符号,下同)。
(2)写出 与
与 两元素最高价氧化物对应水化物反应的离子方程式:
两元素最高价氧化物对应水化物反应的离子方程式:___________ 。
(3)这八种元素中非金属性最强的元素是___________ 。
(4)写出 、
、 两元素形成的原子个数比为
两元素形成的原子个数比为 的物质的电子式:
的物质的电子式:___________ 。
(5) 的氢化物属于
的氢化物属于___________ (填“离子化合物”或“共价化合物”)。
该氢化物与水反应的化学方程式为___________ 。
(6) 和
和 两种元素形成的简单氢化物的稳定性
两种元素形成的简单氢化物的稳定性
___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
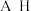 八种元素在周期表中的位置:
八种元素在周期表中的位置:| 周期 | 主族 | ||||||
Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | |
| 2 |  |  |  | ||||
| 3 |  |  |  |  | |||
| 4 |  | ||||||
(1)
 、
、 、
、 三种元素中,原子半径最大的是
三种元素中,原子半径最大的是(2)写出
 与
与 两元素最高价氧化物对应水化物反应的离子方程式:
两元素最高价氧化物对应水化物反应的离子方程式:(3)这八种元素中非金属性最强的元素是
(4)写出
 、
、 两元素形成的原子个数比为
两元素形成的原子个数比为 的物质的电子式:
的物质的电子式:(5)
 的氢化物属于
的氢化物属于该氢化物与水反应的化学方程式为
(6)
 和
和 两种元素形成的简单氢化物的稳定性
两种元素形成的简单氢化物的稳定性
 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表的一部分,请回答有关问题
(1)已知元素⑩的一种核素,其中中子数为45,用原子符号表示该核素为______ ;
(2)由元素②和④形成的三核直线型分子的结构式为______ ;
(3)由上述元素构成的淡黄色固体化合物的电子式______ ,该化合物所含的化学键类型_____ (填“离子键”、“极性键”或“非极性键”),若将该固体投入到含有下列离子的溶液中:NO 、 HCO
、 HCO 、CO
、CO 、SO
、SO 、SO
、SO 、Na+反应完毕后,溶液中上述离子数目几乎不变的有
、Na+反应完毕后,溶液中上述离子数目几乎不变的有_____ (用离子符号表示);
(4)元素⑦、⑧、⑨其离子半径由大到小的顺序是_________ ,元素⑨的最高价氧化物的水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为__________ ;
(5)下列事实不能说明元素⑧的非金属性比元素⑦的非金属性强的是____ ;
A 元素⑧的单质与⑦的氢化物的水溶液反应,溶液变浑浊
B 元素⑧的单质能将Fe氧化成三价铁,而元素⑦的单质只能将铁氧化成二价铁
C ⑦和⑧两元素的简单氢化物受热分解,后者的分解温度高
D 元素⑧的氢化物的水溶液的酸性比元素⑦的氢化物水溶液的酸性强
(6)由上表中的元素构成的A+、B+、C-、D、E五种10电子粒子,已知他们有如下转化关系:A++C- D+E↑;B++C-=2D;写出A+、B+的化学式
D+E↑;B++C-=2D;写出A+、B+的化学式________ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(1)已知元素⑩的一种核素,其中中子数为45,用原子符号表示该核素为
(2)由元素②和④形成的三核直线型分子的结构式为
(3)由上述元素构成的淡黄色固体化合物的电子式
 、 HCO
、 HCO 、CO
、CO 、SO
、SO 、SO
、SO 、Na+反应完毕后,溶液中上述离子数目几乎不变的有
、Na+反应完毕后,溶液中上述离子数目几乎不变的有(4)元素⑦、⑧、⑨其离子半径由大到小的顺序是
(5)下列事实不能说明元素⑧的非金属性比元素⑦的非金属性强的是
A 元素⑧的单质与⑦的氢化物的水溶液反应,溶液变浑浊
B 元素⑧的单质能将Fe氧化成三价铁,而元素⑦的单质只能将铁氧化成二价铁
C ⑦和⑧两元素的简单氢化物受热分解,后者的分解温度高
D 元素⑧的氢化物的水溶液的酸性比元素⑦的氢化物水溶液的酸性强
(6)由上表中的元素构成的A+、B+、C-、D、E五种10电子粒子,已知他们有如下转化关系:A++C-
 D+E↑;B++C-=2D;写出A+、B+的化学式
D+E↑;B++C-=2D;写出A+、B+的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有 、
、 、
、 、
、 、
、 、
、 、
、 七种短周期元素,原子序数依次增大。已知
七种短周期元素,原子序数依次增大。已知 与
与 、
、 与
与 分别同主族,
分别同主族, 、
、 、
、 同周期;
同周期; 、
、 的最外层电子数之和与
的最外层电子数之和与 的最外层电子数相等,
的最外层电子数相等, 与
与 形成的化合物常温下为液态,
形成的化合物常温下为液态, 分别与
分别与 、
、 形成的气体分子电子总数相等,
形成的气体分子电子总数相等, 有多种同素异形体,其中一种是目前已知自然界中最硬的物质,可做首饰品或做切削工具。请回答下列问题:
有多种同素异形体,其中一种是目前已知自然界中最硬的物质,可做首饰品或做切削工具。请回答下列问题:
(1) 在周期表中的位置是
在周期表中的位置是_______ 。
(2)灼烧 的化合物,焰色为
的化合物,焰色为_______ 色, 和
和 形成的一种化合物与
形成的一种化合物与 发生氧化还原反应,该反应的离子方程式为
发生氧化还原反应,该反应的离子方程式为_______ 。
(3) 和
和 的简单气态氢化物中稳定性较强的是
的简单气态氢化物中稳定性较强的是_______ (填化学式), 、
、 、
、 的简单离子半径由大到小的顺序为
的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(4)下列能说明 和G非金属性强弱的事实是
和G非金属性强弱的事实是_______ (填序号)。
① 的单质能与
的单质能与 的简单气态氢化物反应得到
的简单气态氢化物反应得到
②酸性:
③ 的单质与
的单质与 反应得到
反应得到 ,
, 的单质与
的单质与 反应得到
反应得到
④常温下, 的单质为固体,
的单质为固体, 的单质为气体
的单质为气体
 、
、 、
、 、
、 、
、 、
、 、
、 七种短周期元素,原子序数依次增大。已知
七种短周期元素,原子序数依次增大。已知 与
与 、
、 与
与 分别同主族,
分别同主族, 、
、 、
、 同周期;
同周期; 、
、 的最外层电子数之和与
的最外层电子数之和与 的最外层电子数相等,
的最外层电子数相等, 与
与 形成的化合物常温下为液态,
形成的化合物常温下为液态, 分别与
分别与 、
、 形成的气体分子电子总数相等,
形成的气体分子电子总数相等, 有多种同素异形体,其中一种是目前已知自然界中最硬的物质,可做首饰品或做切削工具。请回答下列问题:
有多种同素异形体,其中一种是目前已知自然界中最硬的物质,可做首饰品或做切削工具。请回答下列问题:(1)
 在周期表中的位置是
在周期表中的位置是(2)灼烧
 的化合物,焰色为
的化合物,焰色为 和
和 形成的一种化合物与
形成的一种化合物与 发生氧化还原反应,该反应的离子方程式为
发生氧化还原反应,该反应的离子方程式为(3)
 和
和 的简单气态氢化物中稳定性较强的是
的简单气态氢化物中稳定性较强的是 、
、 、
、 的简单离子半径由大到小的顺序为
的简单离子半径由大到小的顺序为(4)下列能说明
 和G非金属性强弱的事实是
和G非金属性强弱的事实是①
 的单质能与
的单质能与 的简单气态氢化物反应得到
的简单气态氢化物反应得到
②酸性:

③
 的单质与
的单质与 反应得到
反应得到 ,
, 的单质与
的单质与 反应得到
反应得到
④常温下,
 的单质为固体,
的单质为固体, 的单质为气体
的单质为气体
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。针对表中①~⑧号元素回答下列问题。
(1)元素①和③的简单化合物含有10个电子,其电子式为___________ ,它的沸点比PH3高,原因是___________ ;
(2)利用元素②的一种中子数为8的核素即___________ (填核素符号),可测定文物的年代;
(3)元素②和元素⑥分别形成的最高价氧化物中,熔点更高的是___________ (用化学式表示),其晶体类型是___________ ;
(4)元素④、⑤、⑧中,原子半径最大的是___________ ,离子半径最大的是___________ ;(填化学式)
(5)写出证明元素⑧比元素⑦非金属性强的反应的化学方程式:___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)利用元素②的一种中子数为8的核素即
(3)元素②和元素⑥分别形成的最高价氧化物中,熔点更高的是
(4)元素④、⑤、⑧中,原子半径最大的是
(5)写出证明元素⑧比元素⑦非金属性强的反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知 A、B、C、D、E 五种主族元素分属三个短周期,且原子序数依次增大。A、C 同主族,可形成离子化合物 CA;B、D 同主族,可形成 DB2、DB3 两种分子。请回答下列问题:
(1)五种元素原子半径由小到大的顺序为_______________ (用元素符号回答)。
(2)A、B 两种元素能形成既含极性键又含非极性键的化合物 M,M 的电子式为_______________ 。
(3)非金属性强弱:D_______________ E(填“>”“<”),用离子方程式表示__________________________ 。
(4)写出均由 A、B、C、D 四种元素组成的两物质的浓溶液发生反应的离子方程式_____________________________ 。
(1)五种元素原子半径由小到大的顺序为
(2)A、B 两种元素能形成既含极性键又含非极性键的化合物 M,M 的电子式为
(3)非金属性强弱:D
(4)写出均由 A、B、C、D 四种元素组成的两物质的浓溶液发生反应的离子方程式
您最近一年使用:0次



