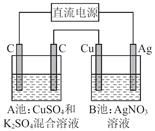
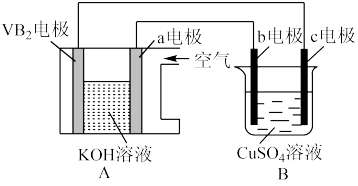
用VB2-空气电池电解硝酸银溶液(a、b、c均为惰性电极)装置如图所示。VB2电极的反应式为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,当外电路中通过0.04mol电子时,B装置内共收集到0.448 L气体(标准状况),则下列说法错误的是

| A.原电池工作时总反应为:4VB2+11O2=4B2O3+2V2O5 |
| B.b电极为阳极,发生氧化反应 |
| C.电解过程中,c电极表面先有固体物质析出,后有气泡产生 |
| D.若B装置内的液体体积为100 mL(忽略体积变化),则硝酸银溶液的物质的量浓度为0.4mol•L-1 |
更新时间:2020-08-10 14:11:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】设NA代表阿伏加德罗常量的值。下列说法正确的是
| A.100 g 20%NaOH溶液中含有的氧原子数为0.5NA |
| B.标准状况下,11.2 L乙烷和乙烯混合物中含有的碳原子数为NA |
| C.2 mol SO2与1 mol O2在密闭容器中充分反应后,容器中的分子总数为2NA |
| D.用铜作电极电解饱和NaCl溶液,当电路上通过0.2 mol e-时,阴、阳两极产生的气体分子总数为0.2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用情性电极电解一定浓度的CuSO4溶液,通电—段时间后,向所得的溶液中加入19.6g Cu(OH)2后恰好恢复到电解前的浓度和pH。则下列说法正确的是
| A.电解过程中阴极没有气体生成 | B.电解过程中转移的电子的物质的量为0.6mol |
| C.原CuSO4溶液的浓度为0.1 mol·L-1 | D.电解过程中阴、阳极共收集到气体体积为8.96L(标准状况) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】研究微生物燃料电池不仅可以获得高效能源,还能对工业污水等进行处理。利用微生物燃料电池处理含硫废水并电解制备KIO3的原理如图所示,下列说法正确的是


| A.光照强度大小不影响KIO3的制备速率 |
| B.右侧电池中K+通过阳离子交换膜从P极移向Q极 |
C.电极N处发生电极反应:S-6e-+4H2O= +8H+ +8H+ |
| D.不考虑损耗,电路中每消耗1 molO2,理论上Q极可制得342.4 g KIO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
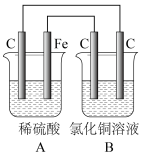
【推荐2】烧杯A中盛放0.1 mol·L-1的H2SO4溶液,烧杯B中盛放0.1 mol·L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不 正确的是( )

| A.A为原电池 |
| B.B为电解池 |
| C.当A烧杯中产生0.1 mol气体时,B烧杯中产生气体的物质的量也为0.1 mol |
| D.一段时间后,B烧杯中溶液的浓度增大 |
您最近一年使用:0次


 向b极迁移
向b极迁移