某同学做同主族元素性质的相似性和递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:___________ 。
(2)实验用品:①试剂:金属钠、金属钾、新制氯水、溴水、0.1 mol·L-1NaBr溶液、0.1 mol·L-1NaI溶液、CCl4溶液等。
②仪器:_______ 、_______ 、______ 、镊子、小刀、玻璃片等。
(3)实验内容(请把表中与实验方案对应的实验现象的标号和化学方程式补写完整):
(4)实验结论:______________ 。
实验方案 | 实验现象 |
| ①将新制氯水滴加到NaBr溶液中,振荡静置 | A.浮在水面上,熔成小球,四处游动,随后消失 |
| ②将一小块金属钠放入冷水中 | B.溶液变为橙红色 |
| ③将溴水滴加到NaI溶液中,振荡静置 | C.浮在水面上,熔成小球,四处游动,并伴有轻微的爆炸声,很快消失 |
| ④将一小块金属钾放入冷水中 | D.溶液变为橙色 |
(1)实验目的:
(2)实验用品:①试剂:金属钠、金属钾、新制氯水、溴水、0.1 mol·L-1NaBr溶液、0.1 mol·L-1NaI溶液、CCl4溶液等。
②仪器:
(3)实验内容(请把表中与实验方案对应的实验现象的标号和化学方程式补写完整):
| 实验方案 | 实验现象 | 化学方程式 |
① | D | Cl2+2NaBr=2NaCl+Br2 |
② | A | 2Na+2H2O=2NaOH+H2↑ |
③ | ||
④ |
19-20高一·全国·课时练习 查看更多[1]
(已下线)4.1.2 原子结构与元素的性质练习(1)——《高中新教材同步备课》(人教版 必修第一册)
更新时间:2020-08-12 18:30:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________ 与盐酸反应最剧烈,________ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为___________________ 。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(3)仪器B的名称为____________ ,干燥管D的作用是防止_____________________ 。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液的现象___________ ,即可证明。请写出一种制取氯气的化学反应方程式:_______________________________________ ,从环境保护的角度考虑,此装置缺少尾气处理装置,可用___________ 溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液________________________ 的现象,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有__________ 溶液的洗气瓶。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(3)仪器B的名称为
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液的现象
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
您最近一年使用:0次
【推荐2】某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。甲同学取钠、镁、锡各1 mol分别投入到足量的盐酸中,预测实验结果。
(1)甲同学设计实验的目的是______ 。
(2)与盐酸反应最剧烈的是______ 。
(3)利用如图所示装置可以验证非金属性的变化规律。

①仪器A的名称为______ ,干燥管D的作用是______ 。
②实验室中现有药品: 溶液、
溶液、 、浓盐酸、
、浓盐酸、 ,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为______ 、______ 、______ ,装置C中的实验现象为有黄色沉淀生成,相关反应的离子方程式为______ 。
③若要证明非金属性: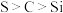 ,则A中加
,则A中加______ ,B中加 ,C中加
,C中加______ ,观察到C中的现象为______ 。
(1)甲同学设计实验的目的是
(2)与盐酸反应最剧烈的是
(3)利用如图所示装置可以验证非金属性的变化规律。

①仪器A的名称为
②实验室中现有药品:
 溶液、
溶液、 、浓盐酸、
、浓盐酸、 ,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为③若要证明非金属性:
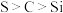 ,则A中加
,则A中加 ,C中加
,C中加
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某同学学习过元素周期律、元素周期表后,在做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关的实验现象。现在请你帮助该学生整理并完成实验报告。
(1) 实验目的:探究同一主族元素性质的递变规律。
(2) 实验用品:
仪器:________ 、________ 。(请填写两件主要的玻璃仪器)
药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳。
(3) 实验内容(在如表横线中填写相关内容):
(4) 实验结论: _______________________________________________ 。
(5) 问题和讨论:
①上述两个实验中发生反应的离子方程式分别为______________ 、_____________ 。
②由于F2过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举事实说明氟的非金属性比氯强___________________ 。
(1) 实验目的:探究同一主族元素性质的递变规律。
(2) 实验用品:
仪器:
药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳。
(3) 实验内容(在如表横线中填写相关内容):
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈 |
| ② | 向盛有少量碘化钾溶液的试管中滴加少量溴水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈 |
(5) 问题和讨论:
①上述两个实验中发生反应的离子方程式分别为
②由于F2过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举事实说明氟的非金属性比氯强
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】甲乙两个兴趣小组分别设计了以下两组实验:
(一)甲组同学设计实验探究Cl和S元素的非金属性。__________________ 。
(2)B中饱和食盐水的作用是__________________ 。
(3)C中证明元素非金属性Cl大于S的化学方程式为____________ 。
(二)实验探究:探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各小题。
(4)实验装置:______
(5)实验步骤:
连接仪器、______ 、加药品后,打开a,然后滴入浓硫酸,加热(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是__________________ ;
装置E中足量酸性 溶液的作用是
溶液的作用是__________________ ;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是____________ ;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性______ (填“能”或“否”),理由是__________________ 。
(一)甲组同学设计实验探究Cl和S元素的非金属性。
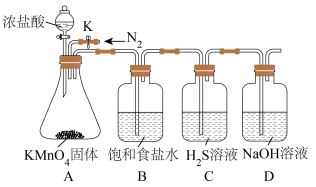
(2)B中饱和食盐水的作用是
(3)C中证明元素非金属性Cl大于S的化学方程式为
(二)实验探究:探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各小题。
(4)实验装置:
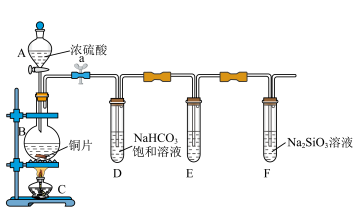
(5)实验步骤:
连接仪器、
①铜与浓硫酸反应的化学方程式是
装置E中足量酸性
 溶液的作用是
溶液的作用是②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强(提示:Na2S +2HCl = 2NaCl+ H2S↑),某化学实验小组设计了如下实验,请回答下列问题:

(1)画出虚线框内的实验装置图____ ,所加试剂为___________ ,该装置的作用是__________ 。
(2)装置B中盛放的试剂是____ (填序号),
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
B装置中发生反应的离子方程式为___________________________ 。
(3)已知:①硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。②高氯酸的酸性比硫酸强;③铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;④HCl比H2S稳定;⑤硫酸比次氯酸稳定;能说明氯的非金属性比硫强的是____ (填序号)。
A.全部 B. ①②③④ C.①②④⑤ D. ①③④⑤
(4)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:_____________________ 。

(1)画出虚线框内的实验装置图
(2)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
B装置中发生反应的离子方程式为
(3)已知:①硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。②高氯酸的酸性比硫酸强;③铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;④HCl比H2S稳定;⑤硫酸比次氯酸稳定;能说明氯的非金属性比硫强的是
A.全部 B. ①②③④ C.①②④⑤ D. ①③④⑤
(4)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________ 与盐酸反应最剧烈,________ 与盐酸反应产生的气体最多。资料显示:钠、镁、铝都可以用于制备储氢的金属氢化物。NaAlH4是一种良好的储氢材料。NaAlH4与水反应产生氢气的化学方程式为____________________ 。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:___________________ 。
(3)下列事实能说明氯元素原子得电子能力比硫元素原子强的是________ (填序号)。①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S大 ④HCl的还原性比H2S弱⑤HClO4的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧
(4)利用下图装置证明非金属性:C>Si,则A中加________ 、B中加Na2CO3、C中加________ ,观察到C中溶液的现象为______________________________________ 。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:
(3)下列事实能说明氯元素原子得电子能力比硫元素原子强的是
(4)利用下图装置证明非金属性:C>Si,则A中加

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
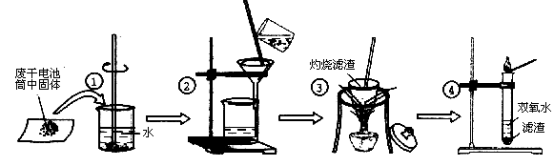
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作①的名称是________ ;
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、______ 、泥三角和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种无色无味能使澄清石灰水变浑浊的气体,由此推测灼烧前的滤渣中存在的物质有___________ 。
(3)往操作④的试管中加入操作③灼烧后所得黑色固体,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定灼烧后的黑色固体为_________ , 操作④相关的化学方程式为_______________ 。
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4+,该同学取少许滤液于试管中________________ (填写操作与现象),则证实滤液中含有NH4+。
(5)该同学利用在废旧干电池中回收的Zn片和石墨电极,设计一个原电池实验,比较铜与锌的金属活动性强弱。
限用材料:铜片、锌片、石墨电极、稀硫酸、CuSO4溶液、ZnSO4溶液;
限用仪器:直流电源、电流计、导线、烧杯、试管、盐桥等中学化学常见的药品和仪器
请画出实验装置图_______ ,并作相应标注,同时写出正极方程式_______________ 。

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作①的名称是
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、
(3)往操作④的试管中加入操作③灼烧后所得黑色固体,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定灼烧后的黑色固体为
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4+,该同学取少许滤液于试管中
(5)该同学利用在废旧干电池中回收的Zn片和石墨电极,设计一个原电池实验,比较铜与锌的金属活动性强弱。
限用材料:铜片、锌片、石墨电极、稀硫酸、CuSO4溶液、ZnSO4溶液;
限用仪器:直流电源、电流计、导线、烧杯、试管、盐桥等中学化学常见的药品和仪器
请画出实验装置图
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】铁有两种氯化物都是重要的化工试剂,它们的一些性质及制备方法。
Ⅰ.氯化铁:熔点为306℃,沸点为315℃,易吸收空气中的水分,工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
Ⅱ.氯化亚铁:熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
实验室可用如图所示的装置模拟工业生产无水氯化铁,请回答相关问题:

(1)装置A用KMnO4固体与浓盐酸反应制氯气,反应的离子方程式为____ 。
(2)导管b口应与____ (从虚线框内装置中选择装置后用字母代号填空)连接,这样可避免反应系统与环境间的相互影响。
(3)实验完成后,取广口瓶C中收集到的产物进行如下测定分析:①称取4.52g样品溶于过量的稀盐酸中;②加入足量H2O2;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中铁元素的质量分数为____ %(结果精确到小数点后两位)。
(4)①用此装置制得无水氯化铁含铁量____ (填“偏高”或“偏低”),显然其中含有较多的____ (填化学式)杂质。
②若要得到较纯净的无水氯化铁,可采取的装置改进措施是____ 。
(5)工业将Cl2通入石灰乳中制备漂白粉,漂白粉的有效成分是____ 。(填化学式)
Ⅰ.氯化铁:熔点为306℃,沸点为315℃,易吸收空气中的水分,工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
Ⅱ.氯化亚铁:熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
实验室可用如图所示的装置模拟工业生产无水氯化铁,请回答相关问题:

(1)装置A用KMnO4固体与浓盐酸反应制氯气,反应的离子方程式为
(2)导管b口应与
(3)实验完成后,取广口瓶C中收集到的产物进行如下测定分析:①称取4.52g样品溶于过量的稀盐酸中;②加入足量H2O2;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中铁元素的质量分数为
(4)①用此装置制得无水氯化铁含铁量
②若要得到较纯净的无水氯化铁,可采取的装置改进措施是
(5)工业将Cl2通入石灰乳中制备漂白粉,漂白粉的有效成分是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】(Ⅰ)某探究小组用 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验
浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验 的用量为25.00mL,大理石用量为10.00g。
的用量为25.00mL,大理石用量为10.00g。
(1)请完成实验设计表,并在实验目的一栏中填空:a___________ ,e___________ 。
(2)实验①中 质量随时间变化的关系如图。计算实验①中70s~90s范围内用
质量随时间变化的关系如图。计算实验①中70s~90s范围内用 表示的平均反应速率
表示的平均反应速率___________  (忽略溶液体积变化,不需要写出计算过程)。在0~70s、70~90s、90~200s各相同的时间段里,反应速率最大的时间段是
(忽略溶液体积变化,不需要写出计算过程)。在0~70s、70~90s、90~200s各相同的时间段里,反应速率最大的时间段是___________ 。

(II)某小组利用 溶液和硫酸酸化的
溶液和硫酸酸化的 溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性
溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性 溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
(3)表中
___________ mL。
(4)探究温度对化学反应速率影响的实验编号是___________ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是___________ 。
(5)实验①测得 溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率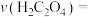
___________  。
。
 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验
浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验 的用量为25.00mL,大理石用量为10.00g。
的用量为25.00mL,大理石用量为10.00g。| 实验编号 | 温度(℃) | 大理石规格 |  浓度 浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (I)实验①和②探究浓度对反应速率的影响; (II)实验①和③探究温度对反应速率的影响; (III)实验①和④探究e对反应速率的影响 |
| ② | 25 | 粗颗粒 | a | |
| ③ | b | 粗颗粒 | 2.00 | |
| ④ | c | 细颗粒 | d |
(2)实验①中
 质量随时间变化的关系如图。计算实验①中70s~90s范围内用
质量随时间变化的关系如图。计算实验①中70s~90s范围内用 表示的平均反应速率
表示的平均反应速率 (忽略溶液体积变化,不需要写出计算过程)。在0~70s、70~90s、90~200s各相同的时间段里,反应速率最大的时间段是
(忽略溶液体积变化,不需要写出计算过程)。在0~70s、70~90s、90~200s各相同的时间段里,反应速率最大的时间段是
(II)某小组利用
 溶液和硫酸酸化的
溶液和硫酸酸化的 溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性
溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性 溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
| 实验 |  酸性 酸性 溶液的体积/mL 溶液的体积/mL |  溶液的体积/mL 溶液的体积/mL |  的体积/mL 的体积/mL | 实验温度/℃ | 溶液褪色所需时间/min |
| ① | 10 |  | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 |  | 50 |

(4)探究温度对化学反应速率影响的实验编号是
(5)实验①测得
 溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率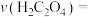
 。
。
您最近一年使用:0次



