下列有关热化学方程式的书写及对应的表述均正确的是
A.已知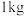 金属铍完全燃烧放出的热量为 金属铍完全燃烧放出的热量为 ,则铍燃烧的热化学方程式为: ,则铍燃烧的热化学方程式为: |
B.稀醋酸与 溶液反应: 溶液反应: |
C.已知 氢气完全燃烧生成液态水所放出的热量为 氢气完全燃烧生成液态水所放出的热量为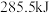 ,则水分解的热化学方程式为: ,则水分解的热化学方程式为: |
D.已知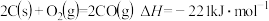 ,则可知 ,则可知 的燃烧热 的燃烧热 |
更新时间:2020/08/26 18:07:16
|
相似题推荐
单选题-单题
|
较易
(0.85)
名校
解题方法
【推荐1】“中国芯”的主要原料是单晶硅,“精炼硅”反应历程中的能量变化如下图所示。下列有关描述正确的是
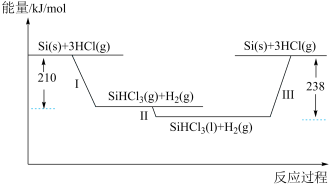
| A.历程Ⅰ是吸热反应 |
| B.历程Ⅱ发生了化学变化 |
| C.历程Ⅲ 的热化学方程式是:SiHCl3(l) + H2(g) = Si(s)+3HCl(g) ΔH=+238 kJ/mol |
| D.实际工业生产中,粗硅变为精硅的过程无需外界能量供给 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知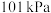 时辛烷的燃烧热为
时辛烷的燃烧热为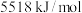 ,强酸与强碱在稀溶液中发生反应时的中和热为
,强酸与强碱在稀溶液中发生反应时的中和热为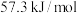 ,则下列热化学方程式书写正确的是
,则下列热化学方程式书写正确的是
①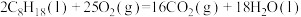

②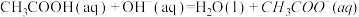
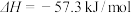
③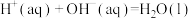
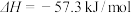
④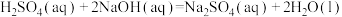
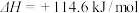
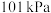 时辛烷的燃烧热为
时辛烷的燃烧热为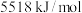 ,强酸与强碱在稀溶液中发生反应时的中和热为
,强酸与强碱在稀溶液中发生反应时的中和热为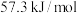 ,则下列热化学方程式书写正确的是
,则下列热化学方程式书写正确的是①
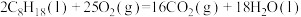

②
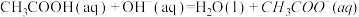
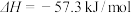
③
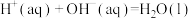
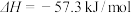
④
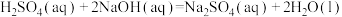
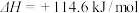
| A.①③ | B.②③ | C.②④ | D.③ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】沼气是一种能源,它的主要成分是CH4,常温下0.5molCH4完全燃烧生成CO2和水时,放出445kJ热量,则下列热化学方程式中正确的是
| A.2CH4(g)+4O2(g)=2CO2(g)+4H2O(g) ΔH=+890kJ·mol-1 |
| B.CH4(g)+2O2(g)= CO2(g)+2H2O(l) ΔH=+445kJ·mol-1 |
| C.CH4(g)+2O2(g)= CO2(g)+2H2O(l) ΔH=-890kJ·mol-1 |
| D.2CH4(g)+4O2(g)=2CO2(g)+4H2O(g) ΔH=-890kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关热化学方程式的叙述正确的是
| A.已知2H2(g)+O2(g) = 2H2O(l);ΔH=−571.6 kJ∙mol−1,则氢气的燃烧热为285.8 kJ∙mol−1 |
| B.已知C(石墨,s)= C(金刚石,s);ΔH>0,则金刚石比石墨稳定 |
| C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq) = CH3COONa(aq) + H2O(l) ΔH =−57.4 kJ∙mol−1 |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】测定中和反应反应热的装置如图所示,下列有关该实验的说法中不正确的是
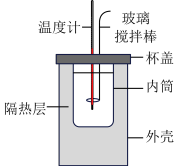
| A.杯盖和外壳的作用是隔热,减少热量的散失 |
| B.使用玻璃搅拌器使反应更充分 |
| C.实验需要记录反应前初始温度及反应后溶液达到的最高温度 |
| D.测定中和反应热时,可以选用NaOH固体和稀盐酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列热化学方程式表达正确的是
| A.C2H5OH(g) + 3O2(g) = 2CO2(g) + 3H2O(l) △H = -1499.0 kJ/mol(燃烧热) |
| B.NaOH(aq) + HCl(aq) = NaCl(aq) + H2O(1) △H = +57.3 kJ/mol(中和热) |
| C.S(s) + O2(g) = SO2(g) △H = +269.8 kJ/mol(反应热) |
| D.2NO2= O2+ 2NO △H = +116.2 kJ/mol(反应热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于说法正确的是
| A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件下和在点燃条件下的△H不同 |
| B.CO(g)的燃烧热△H =-283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
| C.热化学方程式未注明温度和压强时,△H表示标准状况下的数据 |
| D.在加热或点燃条件下才能进行的化学反应一定为吸热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.甲烷的摩尔燃烧焓为 甲烷完全燃烧放出 甲烷完全燃烧放出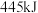 热量时,生成 热量时,生成 个数为 个数为 |
B.氢氧燃料电池中,负极有 气体参与反应时,转移的电子数为 气体参与反应时,转移的电子数为 |
C.氯碱工业中,制备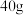 烧碱时阴极生成气体的分子数为 烧碱时阴极生成气体的分子数为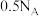 |
D. 和 和 于密闭容器中充分反应后, 于密闭容器中充分反应后, 分子的总数为 分子的总数为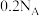 |
您最近一年使用:0次



