某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电高效燃料电池,充一次电可连续使用一个月。如图是一个电化学过程的示意图。

请填空:
(1)充电时:原电池的负极与电源______ 极相连。B极的电极反应式为_______ 。
(2)放电时,负极的电极反应式为_______ 。
(3)在此过程中若完全反应,乙池中A极的质量升高648 g,则甲池中理论上消耗O2______ L(标准状况下)。
(4)若在常温常压下,1g CH3OH燃烧生成CO2和液态H2O时放出热量22.68 kJ,则表示该反应的热化学方程式为_______

请填空:
(1)充电时:原电池的负极与电源
(2)放电时,负极的电极反应式为
(3)在此过程中若完全反应,乙池中A极的质量升高648 g,则甲池中理论上消耗O2
(4)若在常温常压下,1g CH3OH燃烧生成CO2和液态H2O时放出热量22.68 kJ,则表示该反应的热化学方程式为
更新时间:2020-09-14 08:38:40
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】“嫦娥二号”卫星于2010年10月1日18时59分57秒在西昌卫星发射中心发射升空,并且获得了圆满成功。火箭推进器中装有强还原剂液态肼(N2H4)和强氧化剂液态H2O2,当它们混合反应时,产生大量氮气和水蒸气,并放出大量的热。已知1 mol液态肼与足量的液态H2O2反应生成氮气和水蒸气,放出642 kJ的热量。
(1)该反应的热化学方程式为___________ 。
(2)又知H2O(l)=H2O(g) ΔH=+44 kJ/mol,则1 mol液态肼与足量液态过氧化氢反应生成氮气和液态水时放出的热量是___________ kJ。
(3)此反应用于火箭推进,除释放出大量的热和快速产生大量气体外,还有一个很大的优点是___________ 。
(1)该反应的热化学方程式为
(2)又知H2O(l)=H2O(g) ΔH=+44 kJ/mol,则1 mol液态肼与足量液态过氧化氢反应生成氮气和液态水时放出的热量是
(3)此反应用于火箭推进,除释放出大量的热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】依据事实,按要求填空:
(1)在25℃、101kPa下,1mol乙醇燃烧生成CO2和液态水时放热1269.6kJ.则表示乙醇燃烧热的热化学方程式为______ .
(2)已知拆开1mol H﹣H键,1molN﹣H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为______ .
(3)已知:2SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)═2NO2(g)△H=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)的△H=______ kJ•mol﹣1.
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:______ .
(1)在25℃、101kPa下,1mol乙醇燃烧生成CO2和液态水时放热1269.6kJ.则表示乙醇燃烧热的热化学方程式为
(2)已知拆开1mol H﹣H键,1molN﹣H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为
(3)已知:2SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)═2NO2(g)△H=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)的△H=
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】以黄铁矿为原料生产硫酸的工艺流程图如下:
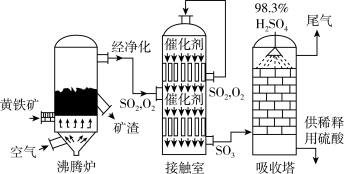
(1)将燃烧黄铁矿的化学方程式补充完整4_______ +11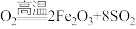
(2)接触室中发生反应的化学方程式是_______ 。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)_______。
(4)每160g SO3气体与H2O化合放出260.6kJ的热量,该反应的热化学方程是_______ 。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是_______ 。

(1)将燃烧黄铁矿的化学方程式补充完整4
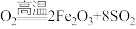
(2)接触室中发生反应的化学方程式是
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)_______。
| A.为使黄铁矿充分燃烧,需将其粉碎 |
| B.过量空气能提高SO2的转化率 |
| C.使用催化剂能提高SO2的反应速率和转化率 |
| D.沸腾炉排出的矿渣可供炼铁 |
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙两池电极材料都是铁棒与碳棒(如图),乙池箭头方向为电子移动方向。请回答:
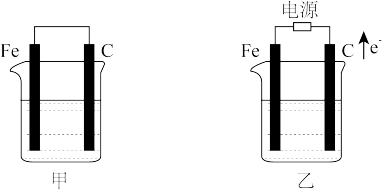
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的_________ 棒;乙池中的________ 棒。
②在乙池中阳极的电极反应是__________ 。
(2)若两池中均盛放滴加少量酚酞的饱和NaCl溶液。
①甲池中的铁容易发生腐蚀,该腐蚀属于电化学腐蚀中的_________ 腐蚀。
②测得乙池中有0.2mol电子发生转移,则标准状况下理论共有_________ L气体生成。

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的
②在乙池中阳极的电极反应是
(2)若两池中均盛放滴加少量酚酞的饱和NaCl溶液。
①甲池中的铁容易发生腐蚀,该腐蚀属于电化学腐蚀中的
②测得乙池中有0.2mol电子发生转移,则标准状况下理论共有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按下图装置进行实验,并回答下列问题
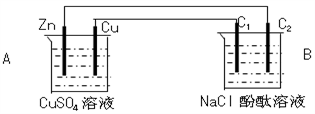
(1)锌极为__________ 极,电极反应式为__________________________________
(2)石墨棒C1为______ 极,电极反应式为________________________________ ,石墨棒C2附近发生的实验现象为__________________________________
(3)当C2极析出224mL气体(标准状态)时,此时装置B中OH-的物质的量为________ mol。

(1)锌极为
(2)石墨棒C1为
(3)当C2极析出224mL气体(标准状态)时,此时装置B中OH-的物质的量为
您最近一年使用:0次
【推荐3】如图是一个化学过程的示意图.已知甲池的总反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O

请回答:
(1)甲池是___ ,通入O2的电极作为___ 极,电极反应式为_______ .
(2)乙池是_____ ,A电极名称为__ 极,电极反应式为_________ .
乙池中的总反应离子方程式为_________ ,一段时间后溶液的pH______ (填“增大”、“减小”或“不变”).
(3)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2____ mL(标准状况下).当丙为硫酸铜溶液且体积为500 mL,通电后丙溶液的pH=________ 。

请回答:
(1)甲池是
(2)乙池是
乙池中的总反应离子方程式为
(3)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:
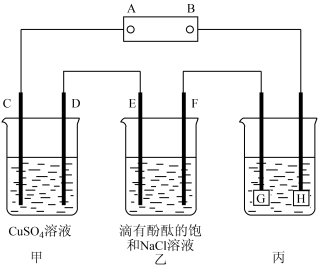
(1)B极是电源的_______ 极(填“正”或“负”)。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________ 。
(3)现用丙装置给铜件镀银,则H应该是________ (填“镀层金属”或“镀件”),电镀液是_____ 溶液。当乙中溶液的c(OH-)=0.1 mol·L-1时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________ ,甲中溶液的pH________ (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是____________ 。

(1)B极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应该是
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图所示,某同学设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
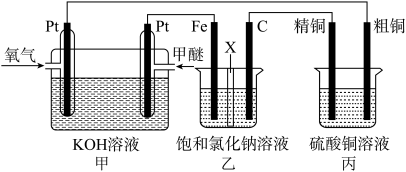
(1)写出甲中负极的电极反应式__ 。
(2)反应一段时间后,乙装置中生成NaOH主要在___ (填“铁极”或“石墨极”)区。
(3)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为___ ,反应一段时间,硫酸铜溶液浓度将___ (填“增大”“减小”或“不变”)。
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为___ 。

(1)写出甲中负极的电极反应式
(2)反应一段时间后,乙装置中生成NaOH主要在
(3)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。

请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是:____________________________________ 。
(2)乙中X是_________ 交换膜,向乙中加入几滴酚酞溶液,工作一段时间后铁电极附近溶液变红,请用化学用语解释相关原因______________________________________________
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为__________ 。
(4)欲用丙装置给铜镀银,b应是____________ (填化学式)。
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO3—的原理如图所示。
①Ag-Pt电极上的电极反应式为___________________________ 。
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为________ g。


请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是:
(2)乙中X是
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为
(4)欲用丙装置给铜镀银,b应是
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO3—的原理如图所示。
①Ag-Pt电极上的电极反应式为
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为

您最近一年使用:0次



