某学生通过测定反应过程中所放出的热量来计算中和热。他将 的盐酸与
的盐酸与 的
的 溶液加入如图甲所示的装置中,进行中和反应。请回答下列问题:
溶液加入如图甲所示的装置中,进行中和反应。请回答下列问题:
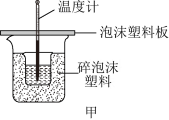
(1)从实验装置上看,图甲中尚缺少的一种仪器是___________ ;由图甲可知该装置有不妥之处,改正的操作是______________________________________________ 。
(2)实验中改用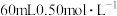 的盐酸与
的盐酸与 的
的 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量___________ (填“相等”或“不相等”);所求中和热的数值_________ (填“相等”或“不相等”),理由是______________________________________________ 。
(3)该同学做实验时有些操作不规范造成测得中和热的数值偏低,请你分析可能的原因是________ (填序号)。
A.测量盐酸的温度后,温度计没有用水冲洗干净,然后去测 溶液的温度
溶液的温度
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将 氢氧化钠溶液错取成了
氢氧化钠溶液错取成了 的氨水
的氨水
(4)假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容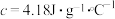 。为了计算中和热,某学生实验记录数据如表:
。为了计算中和热,某学生实验记录数据如表:
依据该学生的实验数据计算,该实验测得的中和热
_________________ (结果保留一位小数)。
(5)将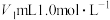 盐酸和
盐酸和 未知浓度的
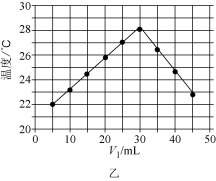
未知浓度的 溶液混合均匀后测量并记录温度,实验结果如图乙所示(实验中始终保持
溶液混合均匀后测量并记录温度,实验结果如图乙所示(实验中始终保持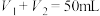 ),通过分析图象可知,做该实验时环境温度
),通过分析图象可知,做该实验时环境温度____________ (填“高于”“低于”或“等于”)22℃,该 溶液的浓度约为
溶液的浓度约为________________  。
。
 的盐酸与
的盐酸与 的
的 溶液加入如图甲所示的装置中,进行中和反应。请回答下列问题:
溶液加入如图甲所示的装置中,进行中和反应。请回答下列问题: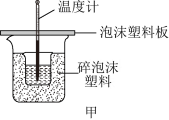

(1)从实验装置上看,图甲中尚缺少的一种仪器是
(2)实验中改用
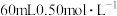 的盐酸与
的盐酸与 的
的 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量(3)该同学做实验时有些操作不规范造成测得中和热的数值偏低,请你分析可能的原因是
A.测量盐酸的温度后,温度计没有用水冲洗干净,然后去测
 溶液的温度
溶液的温度B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将
 氢氧化钠溶液错取成了
氢氧化钠溶液错取成了 的氨水
的氨水(4)假设盐酸和氢氧化钠溶液的密度都是
 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容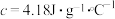 。为了计算中和热,某学生实验记录数据如表:
。为了计算中和热,某学生实验记录数据如表:| 实验序号 | 起始温度 | 终止温度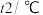 | |
| 稀盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.3 | 20.5 | 25.6 |
依据该学生的实验数据计算,该实验测得的中和热

(5)将
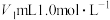 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录温度,实验结果如图乙所示(实验中始终保持
溶液混合均匀后测量并记录温度,实验结果如图乙所示(实验中始终保持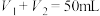 ),通过分析图象可知,做该实验时环境温度
),通过分析图象可知,做该实验时环境温度 溶液的浓度约为
溶液的浓度约为 。
。
更新时间:2020-09-13 16:20:19
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】某实验小组用50mL0.50mol•L-1的盐酸与50mL0.55mol•L-1的NaOH溶液进行中和反应反应热的测定,装置如图所示,回答下列问题:
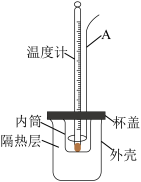
(1)如图所示装置中,仪器A的名称是:___ 。
(2)实验中NaOH溶液相对盐酸溶液是过量的,可能的原因是:___ 。
(3)近似认为0.55mol•L-1NaOH溶液与0.50mol•L-1盐酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容与水的相同为c=4.18J•g-1•℃-1,并忽略量热计的比热容。
则生成1molH2O时放出的热量为___ (结果保留至小数点后一位)。
(4)为了提高测定反应热的准确度,下列措施合理的是___ 。

(1)如图所示装置中,仪器A的名称是:
(2)实验中NaOH溶液相对盐酸溶液是过量的,可能的原因是:
(3)近似认为0.55mol•L-1NaOH溶液与0.50mol•L-1盐酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容与水的相同为c=4.18J•g-1•℃-1,并忽略量热计的比热容。
| 编号 | 起始温度t始/℃ | 终止温度t末/℃ | 温度差(t末-t始)/℃ | |
| HCl溶液 | NaOH溶液 | |||
| 1 | 25.2 | 25.0 | 28.5 | |
| 2 | 24.9 | 25.1 | 28.4 | |
| 3 | 25.0 | 24.9 | 26.1 | |
(4)为了提高测定反应热的准确度,下列措施合理的是
| A.用KOH溶液代替NaOH溶液 |
| B.为了使反应充分发生,向酸溶液中分次加入碱溶液 |
| C.溶液混合后,密切关注温度变化,准确读取体系的最高温度 |
| D.提高实验装置的保温、隔热效果 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应反应热。回答下列问题:
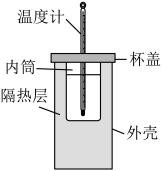
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是_________ 。
(2)如果不盖杯盖,所求得的中和反应反应热的绝对值将会__________ (填“偏大”“偏小”或“无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验__________ (填“相等”或“不相等”,下同);所求中和反应反应热与原实验________ ,简述理由:_______________ 。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会______ (填“偏大”、"偏小”、“无影响”)。
(5)已知:①H+(aq)+OH-(aq)=H2O(1) △H=- 57. 3kJ/ mol;②Ba2+(aq)+ (aq)=BaSO4(s) △H=-13.4kJ/mol。现将100 mL1.0 mol/L Ba(OH)2溶液与100 mL 1.2 mol/L的稀硫酸充分混合,理论上该过程放出的热量为
(aq)=BaSO4(s) △H=-13.4kJ/mol。现将100 mL1.0 mol/L Ba(OH)2溶液与100 mL 1.2 mol/L的稀硫酸充分混合,理论上该过程放出的热量为_______ kJ。

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)如果不盖杯盖,所求得的中和反应反应热的绝对值将会
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
(5)已知:①H+(aq)+OH-(aq)=H2O(1) △H=- 57. 3kJ/ mol;②Ba2+(aq)+
 (aq)=BaSO4(s) △H=-13.4kJ/mol。现将100 mL1.0 mol/L Ba(OH)2溶液与100 mL 1.2 mol/L的稀硫酸充分混合,理论上该过程放出的热量为
(aq)=BaSO4(s) △H=-13.4kJ/mol。现将100 mL1.0 mol/L Ba(OH)2溶液与100 mL 1.2 mol/L的稀硫酸充分混合,理论上该过程放出的热量为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学兴趣小组采用如图所示装置,用50mL 0.5mol/L盐酸与50mL 0.55mol/L NaOH溶液在其中进行中和反应,通过测定反应过程中所放出的热量来计算中和热。回答下列问题:
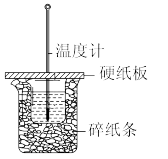
(1)在大小烧杯间填满碎泡沫塑料的作用是_______ 。
(2)大烧杯上如不盖硬纸板,求得的中和热数值_______ (填“偏大”“偏小”或“无影响”)。
(3)从实验装置图上看少了一种仪器是_______ ,能否用铜丝代替这种仪器?其原因是_______ 。
(4)实验时所用盐酸及NaOH溶液的密度均为1g/cm3,生成溶液的比热容c =4.18J/( g·℃),实验起始温度为t1℃,终止温度为t2℃,试计算生成1mol水时的反应热△H =_______ 。

(1)在大小烧杯间填满碎泡沫塑料的作用是
(2)大烧杯上如不盖硬纸板,求得的中和热数值
(3)从实验装置图上看少了一种仪器是
(4)实验时所用盐酸及NaOH溶液的密度均为1g/cm3,生成溶液的比热容c =4.18J/( g·℃),实验起始温度为t1℃,终止温度为t2℃,试计算生成1mol水时的反应热△H =
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室用50 mL 0.50 mol/L盐酸与50 mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量来计算中和反应的反应热。
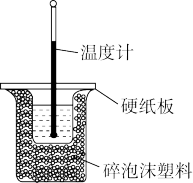
(1)实验室提供了0.50 mol/L和0.55 mol/L两种浓度的NaOH溶液,最好选择___________ mol/L的溶液进行实验,目的是___________ 。
(2)该装置有两处明显错误,其一是温度计不该接触小烧杯底部,另一处是缺少一种玻璃仪器,该仪器的名称为___________ ;该玻璃仪器若换成铜质的,导致 的测定结果
的测定结果___________ (填“偏大”、“偏小”或“无影响”),原因是___________ 。
(3)已知: ,
, 。某学生实验记录数据如下,据此计算,该实验测得的
。某学生实验记录数据如下,据此计算,该实验测得的

___________ (计算结果保留小数点后1位)。
(4)大量实验测得: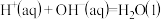
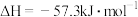 。该学生测定结果出现偏差的原因可能是___________(填字母)。
。该学生测定结果出现偏差的原因可能是___________(填字母)。

(1)实验室提供了0.50 mol/L和0.55 mol/L两种浓度的NaOH溶液,最好选择
(2)该装置有两处明显错误,其一是温度计不该接触小烧杯底部,另一处是缺少一种玻璃仪器,该仪器的名称为
 的测定结果
的测定结果(3)已知:
 ,
, 。某学生实验记录数据如下,据此计算,该实验测得的
。某学生实验记录数据如下,据此计算,该实验测得的

| 实验序号 | 起始温度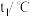 | 终止温度 | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
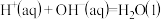
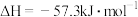 。该学生测定结果出现偏差的原因可能是___________(填字母)。
。该学生测定结果出现偏差的原因可能是___________(填字母)。| A.实验装置保温、隔热效果差 |
| B.分多次把NaOH溶液倒入盛有盐酸的小烧杯中 |
| C.读取终止温度时未注意观察,错过了混合溶液的最高温度 |
| D.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某学生通过测定反应过程中所放出的热量来计算中和反应的反应热,将100mL 0.5 mol/L盐酸与100mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应(在稀溶液中,可以近似地认为酸、碱的密度、比热容与水的相等)。回答下列问题:

(1)从实验装置上看,图中缺少的一种玻璃仪器是___________ ,其作用是___________ 。
(2)简易量热计如果不盖杯盖,生成1mol H2O时所测得中和反应的反应热( )将
)将___________ (填“偏大”、“偏小”或“不变”),判断的理由是___________ 。
(3)实验中改用80mL 0.50 mol/L盐酸和80mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,二者所放出的热量___________ (填“相等”或“不相等”)。
(4)若用等体积等物质的量浓度的CH3COOH进行上述实验,生成1mol H2O时,所测得的中和反应的反应热的绝对值( )将
)将___________ (填“偏大”“偏小”或“无影响”),判断的理由是___________ 。
(5)下列说法正确的是___________ (填标号)。
a.向内筒中加入稀碱时,应当缓慢而匀速地加入
b.将用量筒量取好的稀盐酸加入内筒后,应当快速用水冲洗量筒内壁剩余的稀盐酸至内筒中,以免造成测量误差
c.用量筒量取稀酸或碱时,眼睛必须与液体凹面最低处相平
d.内筒洗净后,未及时烘干,直接用该内筒进行实验,对生成1mol H2O时所测得的中和反应的反应热( )无影响
)无影响

(1)从实验装置上看,图中缺少的一种玻璃仪器是
(2)简易量热计如果不盖杯盖,生成1mol H2O时所测得中和反应的反应热(
 )将
)将(3)实验中改用80mL 0.50 mol/L盐酸和80mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,二者所放出的热量
(4)若用等体积等物质的量浓度的CH3COOH进行上述实验,生成1mol H2O时,所测得的中和反应的反应热的绝对值(
 )将
)将(5)下列说法正确的是
a.向内筒中加入稀碱时,应当缓慢而匀速地加入
b.将用量筒量取好的稀盐酸加入内筒后,应当快速用水冲洗量筒内壁剩余的稀盐酸至内筒中,以免造成测量误差
c.用量筒量取稀酸或碱时,眼睛必须与液体凹面最低处相平
d.内筒洗净后,未及时烘干,直接用该内筒进行实验,对生成1mol H2O时所测得的中和反应的反应热(
 )无影响
)无影响
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】I.在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
(1)写出该反应的热化学方程式______ 。
(2)已知H2O(l)=H2O(g) △H=+44kJ/mol,则16g液态肼燃烧生成氮气和液态水时,放出的热量是______ kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是______ 。
(4)已知①2O2(g)+N2(g)=N2O4(l);△H1
②N2(g)+2H2(g)=N2H4(l);△H2
③O2(g)+2H2(g)=2H2O(g);△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g);△H4
上述反应热效应之间的关系式为△H4=______ 。
II.中和热的测定是高中重要的定量实验.取0.55moL/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
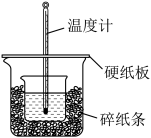
(5)从图中实验装置看,其中尚缺少的一种玻璃用品是______ 。
(6)若改用60mL0.25mol•L-1H2SO4和50mL0.55mol•L-1NaOH溶液进行反应与上述实验相比,所放出的热量______ (填“相等”、“不相等”),若实验操作均正确,则所求中和热______ (填“相等”、“不相等”)。
(7)若上述实验测出来的中和热比57.3kJ/mol更小,则产生偏差的原因可能是______ (填字母)。
a.实验装置保温、隔热效果差
b.量取硫酸溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(1)写出该反应的热化学方程式
(2)已知H2O(l)=H2O(g) △H=+44kJ/mol,则16g液态肼燃烧生成氮气和液态水时,放出的热量是
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是
(4)已知①2O2(g)+N2(g)=N2O4(l);△H1
②N2(g)+2H2(g)=N2H4(l);△H2
③O2(g)+2H2(g)=2H2O(g);△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g);△H4
上述反应热效应之间的关系式为△H4=
II.中和热的测定是高中重要的定量实验.取0.55moL/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:

(5)从图中实验装置看,其中尚缺少的一种玻璃用品是
(6)若改用60mL0.25mol•L-1H2SO4和50mL0.55mol•L-1NaOH溶液进行反应与上述实验相比,所放出的热量
(7)若上述实验测出来的中和热比57.3kJ/mol更小,则产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.量取硫酸溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】测定50mL 0.50mol·L-1盐酸和50mL 0.5mol·L-1 NaOH溶液反应的反应热的实验装置如图所示。回答下列问题:
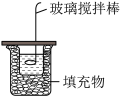
(1)图中缺少的一种仪器是_______ 。
(2)实验时玻璃搅拌器的运动方向是_______ (填标号)。
a.上下 b.左右 c.顺时针 d.逆时针
(3)假设盐酸和氢氧化钠溶液的密度都是1g·cm-3,又知中和反应后生成的溶液的比热容c=4.18J/(g·°C)。实验记录数据如下:
则中和反应生成1mol H2O(1)的ΔH=_______ kJ·mol-1(保留1位小数)。若计算结果与理论数据(57.3kJ·mol-1)相比较,有误差,则可能导致该误差的原因是_______ (填标号)。
a.实验装置保温、隔热效果差
b.用量筒量取盐酸的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定盐酸的起始温度后直接去测定NaOH溶液的温度

(1)图中缺少的一种仪器是
(2)实验时玻璃搅拌器的运动方向是
a.上下 b.左右 c.顺时针 d.逆时针
(3)假设盐酸和氢氧化钠溶液的密度都是1g·cm-3,又知中和反应后生成的溶液的比热容c=4.18J/(g·°C)。实验记录数据如下:
| 实验序号 | 起始温度t1/°C | 终止温度t2/°C | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
a.实验装置保温、隔热效果差
b.用量筒量取盐酸的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定盐酸的起始温度后直接去测定NaOH溶液的温度
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验探究:中和反应反应热的测定
(1)测定原理:环境温度不变时,根据测得的体系的_____ 变化和有关物质的_____ 等来计算反应热。即利用公式:_____ 进行计算。
(2)实验装置
①实验装置中各仪器安装如图。

②各部分仪器的作用
玻璃搅拌器的作用是_____ 。
隔热层的作用是_____ 。
温度计的作用是测定反应前后_____ 的温度。
(3)实验步骤
①反应物温度测量(t1):测量混合前50mL0.50mol·L-1盐酸、50mL0.55mol·L-1氢氧化钠溶液的温度,取_____ ,记录为起始温度t1。
②反应后体系温度测量(t2):将_____ 溶液迅速混合,用_____ 轻轻搅动溶液,并准确读取混合溶液的_____ ,记录为终止温度t2。
③重复实验操作两次,记录每次的实验数据,取其_____ 作为计算依据。
(4)实验数据处理
设溶液的密度均为1g·cm-3,中和后溶液的比热容c=_____ ,根据实验数据计算出该反应放出的热量Q≈_____ kJ,则生成1molH2O时放出的热量为_____ kJ。
(5)实验结论
大量实验测得,在25℃和101kPa下,强酸的稀溶液与强碱的稀溶液,发生中和反应生成_____ H2O时,放出_____ 的热量。
(1)测定原理:环境温度不变时,根据测得的体系的
(2)实验装置
①实验装置中各仪器安装如图。

②各部分仪器的作用
玻璃搅拌器的作用是
隔热层的作用是
温度计的作用是测定反应前后
(3)实验步骤
①反应物温度测量(t1):测量混合前50mL0.50mol·L-1盐酸、50mL0.55mol·L-1氢氧化钠溶液的温度,取
②反应后体系温度测量(t2):将
③重复实验操作两次,记录每次的实验数据,取其
(4)实验数据处理
温度 实验次数 | 起始温度 | 终止温度 | 温度差平均值 | |||
| 盐酸 | NaOH | 平均值 | 温差 | 平均值 | ||
| 1 | 25.0 | 25.2 | ______ | 28.5 | ______ | ______ |
| 2 | 24.9 | 25.1 | ______ | 28.3 | ______ | |
| 3 | 25.6 | 25.4 | ______ | 29.0 | ______ | |
(5)实验结论
大量实验测得,在25℃和101kPa下,强酸的稀溶液与强碱的稀溶液,发生中和反应生成
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】中和热是指在稀溶液中,H+(aq)与OH-(aq)发生中和反应生成1molH2O(l)时的反应热。利用如图所示装置测定中和热,取30mL0.50mol·L-1稀硫酸与60mL0.50mol·L-1NaOH溶液进行实验,实验数据如表。
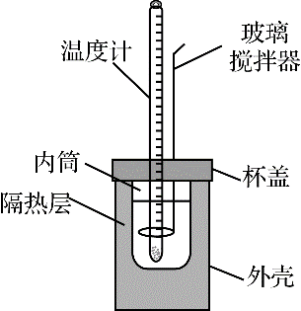
回答下列问题:
(1)上述实验中温度变化的平均值为___ ℃,若近似认为0.50mol·L-1稀硫酸与0.5mol·L-1NaOH溶液的密度均为1g·cm-3,反应所得溶液的比热容c=4.18J·(g·℃)-1,则中和热ΔH的数值为___ kJ·mol-1(保留1位小数)。
(2)上述实验结果与中和热数值57.3kJ·mol-1有偏差,产生偏差的原因不可能是因为___ (填标号)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入内筒中
d.测过稀硫酸的温度计未洗净直接用于测定NaOH溶液的温度
(3)本次实验共需NaOH溶液240mL,则配制0.5mol·L-1NaOH溶液时,需称取NaOH固体___ g。
(4)若改用30mL0.50mol·L-1稀硫酸与30mL0.5mol·L-1Ba(OH)2溶液进行实验,(填“能”或“不能”)___ 据此实验求中和热。

| 温度 实验次数 | 起始温度T1/℃ | 终止温度T2/℃ | ||
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.2 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.3 |
(1)上述实验中温度变化的平均值为
(2)上述实验结果与中和热数值57.3kJ·mol-1有偏差,产生偏差的原因不可能是因为
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入内筒中
d.测过稀硫酸的温度计未洗净直接用于测定NaOH溶液的温度
(3)本次实验共需NaOH溶液240mL,则配制0.5mol·L-1NaOH溶液时,需称取NaOH固体
(4)若改用30mL0.50mol·L-1稀硫酸与30mL0.5mol·L-1Ba(OH)2溶液进行实验,(填“能”或“不能”)
您最近半年使用:0次



