题型:填空题
难度:0.65
引用次数:560
题号:11165903
某0.2L无土栽培用的营养液中含有KCl、 、
、 三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示。
三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示。
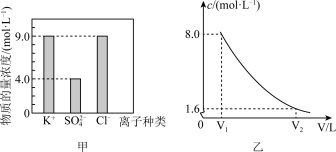
(1)该营养液中 的物质的量浓度为
的物质的量浓度为__________  ,含KCl的质量为
,含KCl的质量为__________ 。
(2)该营养液中 的物质的量为
的物质的量为_____________ 。
(3)若 不参与其他任何反应,将该营养液加水稀释,稀释过程中
不参与其他任何反应,将该营养液加水稀释,稀释过程中 的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则
的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则
__________ ,
__________ 。
 、
、 三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示。
三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示。
(1)该营养液中
 的物质的量浓度为
的物质的量浓度为 ,含KCl的质量为
,含KCl的质量为(2)该营养液中
 的物质的量为
的物质的量为(3)若
 不参与其他任何反应,将该营养液加水稀释,稀释过程中
不参与其他任何反应,将该营养液加水稀释,稀释过程中 的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则
的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则

更新时间:2020-09-23 08:07:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的成分,阅读后并回答下列问题:
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是__________ (填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)__________________ (只要求写表达式,不需计算)mol·L-1。
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是________ (填字母),还缺少的玻璃仪器有__________________ (填仪器名称)。

(4)配制过程中,下列操作对配制结果没有影响的是__________ (填字母)。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可加入的试剂中要含有__________ 。(填化学符号)
| 成分 | 质量/g | 摩尔质量/(g·mol-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是

(4)配制过程中,下列操作对配制结果没有影响的是
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可加入的试剂中要含有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】阅读并分析体检报告,可以初步判断体检者的身体状况。

(1)在图中所示的体检报告中,表示葡萄 糖指标的物理量是______ (填字母)
a.质量分数 b.溶解度
c.摩尔质量 d.物质的量浓度
(2)科学家发现了利用泪液来检测糖尿病的方法,其原理是用氯金酸钠(NaAuCl4)溶液与溶液中的葡萄糖发生反应生成纳米金单质颖粒(直径为 20~60 nm)。检测时 NaAuCl4发生了______ (填“氧化”或“还原”)反应。

(1)在图中所示的体检报告中,表示葡萄 糖指标的物理量是
a.质量分数 b.溶解度
c.摩尔质量 d.物质的量浓度
(2)科学家发现了利用泪液来检测糖尿病的方法,其原理是用氯金酸钠(NaAuCl4)溶液与溶液中的葡萄糖发生反应生成纳米金单质颖粒(直径为 20~60 nm)。检测时 NaAuCl4发生了
您最近半年使用:0次
【推荐3】(1)0.5mol·L-1MgCl2溶液中c(Cl-)为___ mol·L-1,从100mL该溶液中取出20mL再稀释至100mL,c(MgCl2)为__ mol·L-1。
(2)将SO2通入氯化钡溶液中无现象;若将SO2通入硝酸钡溶液中有白色沉淀产生,其化学反应方程式如下(未配平):SO2+Ba(NO3)2+H2O→BaSO4↓+HNO3+NO↑。
①配平上述化学反应方程式并用双线桥表示电子转移的方向和数目___ 。
②该反应中,__ 元素发生氧化反应,氧化剂是__ (写化学式)。氧化产物与还原产物的物质的量之比为___ 。
③当反应消耗19.2gSO2时,反应中转移电子__ mol,在标准状况下,生成NO的体积为__ L。
(2)将SO2通入氯化钡溶液中无现象;若将SO2通入硝酸钡溶液中有白色沉淀产生,其化学反应方程式如下(未配平):SO2+Ba(NO3)2+H2O→BaSO4↓+HNO3+NO↑。
①配平上述化学反应方程式并用双线桥表示电子转移的方向和数目
②该反应中,
③当反应消耗19.2gSO2时,反应中转移电子
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)在100 g浓度为c mol·L-1,密度为ρ g·cm-3的硫酸中加入一定量的水稀释成c/2 mol·L-1的硫酸,则加入水的体积_____ 100 mL(填“=”“>”或“<”,下同)。
(2)若把(1)中的H2SO4改成氨水,应加入水的体积_____ 100 mL。
(3)若把(1)(2)中的物质的量浓度均改为溶质的质量分数,则加入水的体积________ 100 mL。
(2)若把(1)中的H2SO4改成氨水,应加入水的体积
(3)若把(1)(2)中的物质的量浓度均改为溶质的质量分数,则加入水的体积
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.写出下列反应的离子方程式。
(1)向含HCl和NH4Al(SO4)2的混合溶液中逐滴加入NaOH溶液,生成沉淀的量与加入NaOH溶液的量关系如图所示,依据反应的“先后顺序”写出下列各段反应的离子方程式:
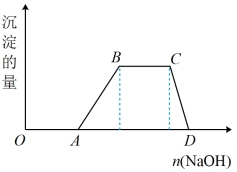
①“OA”段:___________ ;
②“AB”段:___________ ;
③“BC”段:___________ ;
④“CD”段:___________ 。
Ⅱ.“新冠”疫情期间,人们广泛使用“84”消液(有效成分)回答下列问题:
(2)如图是某“84”消毒液的标签, 的物质的量浓度为
的物质的量浓度为___________  (保留1位小数)。使用时通常稀释100倍(体积比),稀释时需要使用的玻璃仪器为胶头滴管、玻璃棒、
(保留1位小数)。使用时通常稀释100倍(体积比),稀释时需要使用的玻璃仪器为胶头滴管、玻璃棒、___________ 。
(3)资料显示“84”消毒液不能与洁厕灵(含 )混合使用,对此某小组开展如图所示的研究。
)混合使用,对此某小组开展如图所示的研究。

①两表面皿之间充满黄绿色气体。则“84”消毒液与洁厕灵反应的化学方程式为___________ ; 的作用是
的作用是___________ 。
②“84”消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ 。
(1)向含HCl和NH4Al(SO4)2的混合溶液中逐滴加入NaOH溶液,生成沉淀的量与加入NaOH溶液的量关系如图所示,依据反应的“先后顺序”写出下列各段反应的离子方程式:

①“OA”段:
②“AB”段:
③“BC”段:
④“CD”段:
Ⅱ.“新冠”疫情期间,人们广泛使用“84”消液(有效成分)回答下列问题:
| 84消毒液 (有效成分)  (规格)  (质量分数)25% (密度) 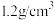 |
 的物质的量浓度为
的物质的量浓度为 (保留1位小数)。使用时通常稀释100倍(体积比),稀释时需要使用的玻璃仪器为胶头滴管、玻璃棒、
(保留1位小数)。使用时通常稀释100倍(体积比),稀释时需要使用的玻璃仪器为胶头滴管、玻璃棒、(3)资料显示“84”消毒液不能与洁厕灵(含
 )混合使用,对此某小组开展如图所示的研究。
)混合使用,对此某小组开展如图所示的研究。
①两表面皿之间充满黄绿色气体。则“84”消毒液与洁厕灵反应的化学方程式为
 的作用是
的作用是②“84”消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请按要求完成下列各题。
(1)将2mol•L-1Al2(SO4)3和0.2mol•L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=___ mol•L-1.若用容量瓶以质量分数为98%、密度为1.84g/cm3的浓硫酸,配制480mL浓度成0.2mol•L-1稀硫酸,计算需要量取___ mL的浓硫酸。(读到小数点后一位)
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是___ ,混合气体的平均摩尔质量是___ 。
(3)还原铁粉与高温水蒸气反应的化学方程式:___ 。
(4)除去Mg粉中的Al粉的试剂是___ ,反应的离子方程式为:___ 。
(1)将2mol•L-1Al2(SO4)3和0.2mol•L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是
(3)还原铁粉与高温水蒸气反应的化学方程式:
(4)除去Mg粉中的Al粉的试剂是
您最近半年使用:0次



