某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。

(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成;
(2)设计实验:①利用上图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是__________ (填“澄清石灰水”或“NaOH溶液”) ;
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有____________ 沉淀生成(填沉淀的颜色),说明Na2CO3和NaHCO3的热稳定性是: Na2CO3_________ NaHCO3(填“ > ”或“ < ”);
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为__________ L(标准状况)。

(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成;
(2)设计实验:①利用上图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
12-13高二上·湖南株洲·开学考试 查看更多[4]
(已下线)2011-2012学年湖南省醴陵市第四中学高二上学期入学考试化学试卷(已下线)2011-2012学年湖南省凤凰县华鑫中学高二下期中考试文化学试卷2015-2016学年湖南省娄底市湘中名校高一上期末考试化学试卷(已下线)2011年湖南省普通高中学业水平考试化学试题
更新时间:2016-12-09 03:13:38
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某小组同学为验证 受热分解的产物,设计如图实验(部分夹持装置已略去,气密性已检验)。
受热分解的产物,设计如图实验(部分夹持装置已略去,气密性已检验)。

(1)实验Ⅰ中,澄清石灰水变浑浊,说明 受热分解的产物中含有
受热分解的产物中含有___________ 。
(2)实验Ⅰ中,加热试管 至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为
至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为 。试剂
。试剂 是
是___________ 。
(3) 受热分解的化学方程式为
受热分解的化学方程式为___________ 。
(4)依据上述实验,除去 固体中的少量
固体中的少量 ,可采用的方法是
,可采用的方法是___________ 。
(5)为确定 固体中是否含
固体中是否含 ,下列实验操作及判断正确的是
,下列实验操作及判断正确的是
 受热分解的产物,设计如图实验(部分夹持装置已略去,气密性已检验)。
受热分解的产物,设计如图实验(部分夹持装置已略去,气密性已检验)。
(1)实验Ⅰ中,澄清石灰水变浑浊,说明
 受热分解的产物中含有
受热分解的产物中含有(2)实验Ⅰ中,加热试管
 至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为
至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为 。试剂
。试剂 是
是(3)
 受热分解的化学方程式为
受热分解的化学方程式为(4)依据上述实验,除去
 固体中的少量
固体中的少量 ,可采用的方法是
,可采用的方法是(5)为确定
 固体中是否含
固体中是否含 ,下列实验操作及判断正确的是
,下列实验操作及判断正确的是| A.加热,观察能否放出气体 |
| B.溶于水中,加入澄清石灰水,观察是否有白色沉淀生成 |
| C.加盐酸观察能否放出气体 |
D.溶于水中,滴加少量 溶液,观察是否有白色沉淀生成 溶液,观察是否有白色沉淀生成 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示:

(1)“侯氏制碱法”誉满全球,其中的“碱”为_______ 。
(2)实验室模拟“侯氏制碱法”,下列操作未涉及的是_______。
(3)煅烧的化学方程式为_______ 。
(4)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了_______ (填上述流程中的编号)的循环,流程循环II中X的分子式_______ 。
(5)该流程提取的副产品为_______ 。

(1)“侯氏制碱法”誉满全球,其中的“碱”为
(2)实验室模拟“侯氏制碱法”,下列操作未涉及的是_______。
A. | B. |
C. | D. |
(3)煅烧的化学方程式为
(4)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了
(5)该流程提取的副产品为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】实验室利用右图所示装置进行NaHCO3的受热分解实验。请回答:

(1)加热一段时间后,烧杯中观察到的实验现象是______________ ,反应的离子方程式___________________ 。
(2)实验结束时的正确操作是__________ (填序号),否则会引起_________________ 。
①先将导管从液体中移出,再熄灭酒精灯②先熄灭酒精灯,再将导管从液体中移出
(3)NaHCO3受热分解的化学方程式是______________ 。

(1)加热一段时间后,烧杯中观察到的实验现象是
(2)实验结束时的正确操作是
①先将导管从液体中移出,再熄灭酒精灯②先熄灭酒精灯,再将导管从液体中移出
(3)NaHCO3受热分解的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某同学学习了“广泛存在的含碳化合物”之后,对碳酸钠和碳酸氢钠的性质产生了浓厚的兴趣,因此对二者的性质做了进一步研究,请完成下列相关问题。取a g碳酸氢钠放入图Ⅰ装置的锥形瓶中,取b g碳酸钠放入另一相同装置的锥形瓶中,分别加入相同体积,相同浓度的足量盐酸。相同条件下,分别通过图Ⅱ装置测量生成气体的体积,进行转换处理,得到时间一质量关系曲线如图Ⅲ所示。
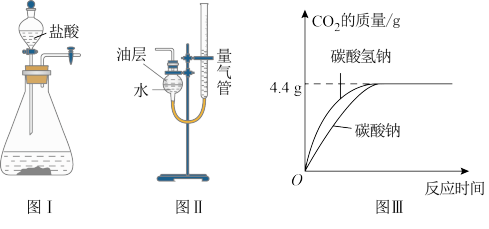
(1)已知二氧化碳不溶于图Ⅱ装置中的油层,则该油层的作用是_______________________________ 。
(2)数据分析:根据图Ⅲ数据,计算可得
_____________ 。
(3)结论:在相同条件下,碳酸氢钠和碳酸钠与盐酸反应生成相同体积 的快慢顺序是
的快慢顺序是_________ 。
(4)反思与讨论:实验中取ag碳酸氢钠和bg碳酸钠的目的是___________________________ 。

(1)已知二氧化碳不溶于图Ⅱ装置中的油层,则该油层的作用是
(2)数据分析:根据图Ⅲ数据,计算可得

(3)结论:在相同条件下,碳酸氢钠和碳酸钠与盐酸反应生成相同体积
 的快慢顺序是
的快慢顺序是(4)反思与讨论:实验中取ag碳酸氢钠和bg碳酸钠的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】如图是教师在课堂中演示的两个实验装置(铁架台等辅助仪器略去未画)
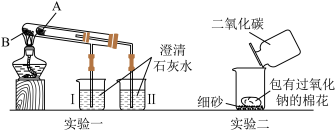
回答下列问题:
(1)实验一是为了探究碳酸钠和碳酸氢钠的热稳定性,请问试管A中盛放的药品是_______ (填序号)(①碳酸钠②碳酸氢钠)。
(2)实验一中观察到的实验现象是_______ ,得到的结论是_______ 写出受热分解的化学方程式_______ 。
(3)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:包有Na2O2的棉花燃烧。请写出Na2O2与CO2反应的化学方程式:_______ 。

回答下列问题:
(1)实验一是为了探究碳酸钠和碳酸氢钠的热稳定性,请问试管A中盛放的药品是
(2)实验一中观察到的实验现象是
(3)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:包有Na2O2的棉花燃烧。请写出Na2O2与CO2反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某校化学兴趣小组,通过下列装置探究碳酸钠和碳酸氢钠的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
提出假设:碳酸钠或碳酸氢钠加热分解时可能有二氧化碳生成。

(1)设计实验:①利用如图装置分别对一定量的碳酸钠和碳酸氢钠进行加热;②为了检验二氧化碳的生成,试管B中应加入的物质是__________________ 。
(2)现象与结论:同学们发现只有在加热碳酸氢钠时,试管B中才有气泡产生且有____________ (填沉淀颜色)沉淀生成,说明碳酸钠的热稳定性________ (填“>”或“<”)碳酸氢钠的热稳定性。
(3)写出碳酸氢钠受热分解的反应方程式__________________________ 。
(4)某同学在探究碳酸氢钠的热稳定性时,称取了8.4 g 碳酸氢钠,充分加热,请你计算理论上可产生二氧化碳气体的体积(标准状况)为________________ 。
提出假设:碳酸钠或碳酸氢钠加热分解时可能有二氧化碳生成。

(1)设计实验:①利用如图装置分别对一定量的碳酸钠和碳酸氢钠进行加热;②为了检验二氧化碳的生成,试管B中应加入的物质是
(2)现象与结论:同学们发现只有在加热碳酸氢钠时,试管B中才有气泡产生且有
(3)写出碳酸氢钠受热分解的反应方程式
(4)某同学在探究碳酸氢钠的热稳定性时,称取了8.4 g 碳酸氢钠,充分加热,请你计算理论上可产生二氧化碳气体的体积(标准状况)为
您最近一年使用:0次



