某溶液X含有K+、Mg2+、Fe3+、A13+、Fe2+、Cl- 、 、OH- 、
、OH- 、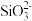 、
、 、
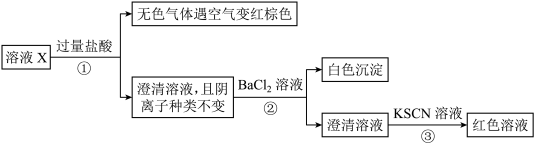
、 中的几种,已知该溶液中各离子物质的量浓度均为0.20 mol/L (不考虑水的电离及离子的水解)。为确定该溶液中含有的离子,现进行了如下的操作:下列说法正确的是
中的几种,已知该溶液中各离子物质的量浓度均为0.20 mol/L (不考虑水的电离及离子的水解)。为确定该溶液中含有的离子,现进行了如下的操作:下列说法正确的是
 、OH- 、
、OH- 、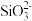 、
、 、
、 中的几种,已知该溶液中各离子物质的量浓度均为0.20 mol/L (不考虑水的电离及离子的水解)。为确定该溶液中含有的离子,现进行了如下的操作:下列说法正确的是
中的几种,已知该溶液中各离子物质的量浓度均为0.20 mol/L (不考虑水的电离及离子的水解)。为确定该溶液中含有的离子,现进行了如下的操作:下列说法正确的是
| A.无色气体可能是NO和CO2的混合物 |
| B.另取100 mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4 g |
| C.溶液X中所含离子种类共有4种 |
| D.由步骤③可知,原溶液肯定存在Fe3+ |
18-19高二下·浙江·期末 查看更多[9]
更新时间:2020-10-15 08:59:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某水溶液只可能含有K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-中的若干种离子。某同学取100mL的溶液分成两等份进行如下实验:
①第一份加过量的氢氧化钠溶液后加热,收集到0.02mol的气体,无沉淀产生,同时得到溶液甲。
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02g固体。
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到11.65g固体。
据此,该同学得到的结论正确的是( )
①第一份加过量的氢氧化钠溶液后加热,收集到0.02mol的气体,无沉淀产生,同时得到溶液甲。
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02g固体。
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到11.65g固体。
据此,该同学得到的结论正确的是( )
| A.实验①中产生的气体为氨气,并可得原溶液中c(NH4+)=0.2mol·L-1 |
| B.实验③中的白色沉淀中一定有BaSO4,无BaCO3 |
| C.原溶液中一定有K+,且c(K+)=0.4mol·L-1 |
| D.若要判断原溶液中是否有Cl-,无需另外设计实验验证 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】水溶液X中只可能溶有K+、Mg2+、Al3+、AlO 、SiO
、SiO 、SO
、SO 、HCO
、HCO 、SO
、SO 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是
 、SiO
、SiO 、SO
、SO 、HCO
、HCO 、SO
、SO 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验:
下列判断正确的是
| A.气体甲一定是纯净物 |
| B.沉淀甲是硅酸和硅酸铝的混合物 |
| C.所有阴离子都可能存在于溶液X中 |
| D.沉淀乙可能是Mg(OH)2和Al(OH)3的混合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】现有易溶强电解质的混合溶液10L,其中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,向其中通入
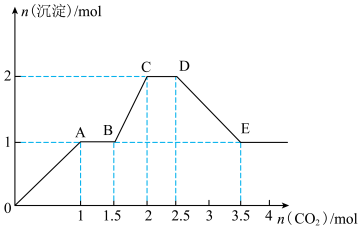
中的几种,向其中通入 气体,产生沉淀的量与通入
气体,产生沉淀的量与通入 的量之间的关系如图所示,下列说法正确的是( )
的量之间的关系如图所示,下列说法正确的是( )
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,向其中通入
中的几种,向其中通入 气体,产生沉淀的量与通入
气体,产生沉淀的量与通入 的量之间的关系如图所示,下列说法正确的是( )
的量之间的关系如图所示,下列说法正确的是( )
A.该溶液中能确定存在的离子是 、 、 、 、 |
B.肯定不存在的离子是 、 、 |
| C.若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为0.2mol/L |
D.OA段反应的离子方程式:2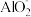 +CO2+3H2O=2Al(OH)3↓+ +CO2+3H2O=2Al(OH)3↓+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列①②对应的试剂(或条件)不能完成实验目的的是( )

| 实验目的 | 试剂(条件) | |
| A | 温度对Na2S2O3溶液与H2SO4溶液反应速率的影响 | ①热水浴②冷水浴 |
| B | 用Na块检验乙醇分子存在不同于烃分子里的氢原子 | ①乙醇②煤油 |
| C | 用硝酸酸化的AgNO3溶液检验自来水中能否蒸馏除去Cl- | ①自来水②蒸馏水 |
| D | 催化剂对H2O2分解速率的影响 | ①0.1mol/LFeCl3 ②0.2mol/LFeCl3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】固体粉末X中可能含有NaAlO2、K2SO3、FeSO4中的若干种。为确定该固体粉末的成分,取适量X进行以下实验,实验过程及现象如图所示。下列说法不正确 的是
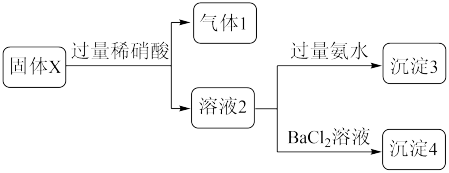

| A.气体1一定不含有SO2 |
| B.沉淀4一定是纯净物 |
| C.固体X中至少含有两种物质 |
| D.若沉淀3为白色沉淀且在空气中久置不变色,则X中一定含有K2SO3 |
您最近一年使用:0次

 粉末,向其中滴加过量盐酸,产生无色气体
粉末,向其中滴加过量盐酸,产生无色气体 溶液中加入足量
溶液中加入足量 溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解
溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解 ,加热;再加入银氨溶液,未出现银镜
,加热;再加入银氨溶液,未出现银镜


