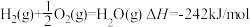下列说法正确的是正确的是( )
| A.已知2SO2(g)+O2(g) =2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
B. 定条件下,将 定条件下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 放热 放热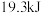 ,其热化学方程式: ,其热化学方程式: 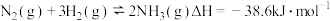 |
| C.在测定中和热时若选用浓硫酸和氢氧化钠,所得中和热值会偏小 |
| D.已知2H2(g)+O2(g)=2H2O(l) △H1 2H2(g)+O2(g)=2H2O(g) △H2 ,则ΔH1<ΔH2 |
更新时间:2020-10-15 13:47:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 是一种温室气体,其存储能量的能力是
是一种温室气体,其存储能量的能力是 的12000~20000倍,在大气中的寿命可长达740年,以下是几种化学键的键能:
的12000~20000倍,在大气中的寿命可长达740年,以下是几种化学键的键能:
下列说法中正确的是
 是一种温室气体,其存储能量的能力是
是一种温室气体,其存储能量的能力是 的12000~20000倍,在大气中的寿命可长达740年,以下是几种化学键的键能:
的12000~20000倍,在大气中的寿命可长达740年,以下是几种化学键的键能:| 化学键 |  | 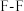 | 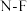 |
键能( ) ) | 946 | 154.8 | 283.0 |
A.过程 放出能量 放出能量 |
B.过程 放出能量 放出能量 |
C.反应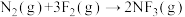 的 的 |
D. 吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应 吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是:
| A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1 |
| B.500℃、30Mpa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)⇌2NH3(g) ΔH=-38.6kJ·mol-1 |
| C.已知C(石墨,s)=C(金刚石,s);△H>0,则石墨比金刚石稳定 |
| D.向50mL0.50mol·L—1盐酸中加入1.0gNaOH固体,可测得中和热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列装置能达到其实验目的的是
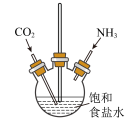 | 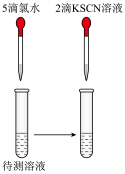 | 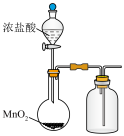 | 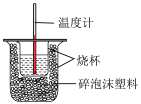 |
| A.可用来制备小苏打 | B.检验溶液中是否含有Fe2+ | C.实验室制氯气 | D.可以测定中和热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq) + OH﹣(aq) ═ H2O (l)△H=﹣57.3kJ•mol﹣1。分别向 1L 0.5mol•L﹣1 的 NaOH 溶液中加入①浓硫酸、②稀醋酸、③稀硝酸,恰好完全反应放出的热量分别为 Q1、Q2、Q3,下列关系正确的是
| A.Q1>Q3>Q2 | B.Q1<Q2<Q3 |
| C.Q1>Q2=Q3 | D.Q1=Q2<Q3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在25℃和101kPa,8g  燃烧生成液态水放出445kJ的热量,则下列热化学方程式中书写正确的是
燃烧生成液态水放出445kJ的热量,则下列热化学方程式中书写正确的是
 燃烧生成液态水放出445kJ的热量,则下列热化学方程式中书写正确的是
燃烧生成液态水放出445kJ的热量,则下列热化学方程式中书写正确的是A.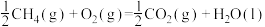  |
B.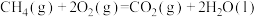 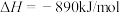 |
C.  |
D.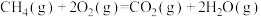 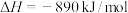 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】乙醇水蒸气重整释氢过程中主要反应的热化学方程式为:
反应Ⅰ: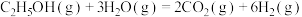

反应Ⅱ: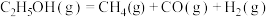

反应Ⅲ:
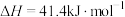
以 和
和 为原料气,通过装有催化剂的反应器,反应相同时间,乙醇转化率、
为原料气,通过装有催化剂的反应器,反应相同时间,乙醇转化率、 、
、 、
、 选择性随温度变化的曲线如图所示。下列说法
选择性随温度变化的曲线如图所示。下列说法不 正确的是
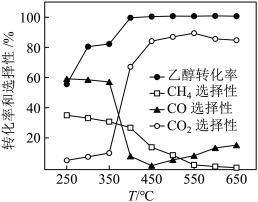
反应Ⅰ:
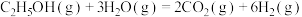

反应Ⅱ:
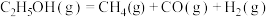

反应Ⅲ:

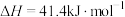
以
 和
和 为原料气,通过装有催化剂的反应器,反应相同时间,乙醇转化率、
为原料气,通过装有催化剂的反应器,反应相同时间,乙醇转化率、 、
、 、
、 选择性随温度变化的曲线如图所示。下列说法
选择性随温度变化的曲线如图所示。下列说法
A.向乙醇水蒸气重整反应体系中通入适量 ,可以为重整反应提供热量 ,可以为重整反应提供热量 |
| B.其他条件不变,升高温度乙醇的平衡转化率增大 |
C.300~450℃时,随温度升高, 的产率增大 的产率增大 |
D.增加原料气中水的比例,可以增大 的选择性 的选择性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法或表示方法中正确的是
| A.已知 2C(s) + 2O2 (g) = 2CO2(g) △H = a kJ/mol、2C(s) + O2(g) = 2CO(g) △H = b kJ/mol,则a > b |
| B.甲烷的燃烧热为 890 kJ/mol,则甲烷燃烧的热化学方程式为 CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) △H = - 890 kJ/mol |
| C.已知 P(s,白磷) = P(s,红磷) △H < 0,则白磷比红磷稳定 |
| D.已知 HCl(aq) + NaOH(aq) = Na Cl(aq) + H2O(l) △H = - 57.3 kJ/mol,则含 40.0 g NaOH 的稀溶液与稀醋酸完全中和,放出小于 57.3 kJ 的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法或表示法正确的是
| A.氢气与氧气反应生成等量的水蒸气和液态水,前者放出热量多 |
| B.需要加热的反应说明它是吸热反应 |
| C.在稀溶液中:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol,若将含0.5 mol H2SO4 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
| D.1 mol S完全燃烧放热297.3 kJ,其热化学方程式:S+O2===SO2 ΔH=-297.3 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列热化学方程式正确的是
| A.已知2C(s)+2O2(g)=2CO2(g) ΔH=akJ·mol-1,2C(s)+O2(g)=2CO(g) ΔH=bkJ·mol-1,则a<b |
| B.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0 |
| C.HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
| D.甲烷的燃烧热ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1 |
您最近一年使用:0次

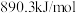 ,则甲烷燃烧的热化学方程式可表示为:
,则甲烷燃烧的热化学方程式可表示为: 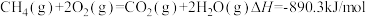
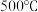 、将
、将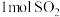 和
和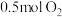 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成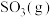 ,放热
,放热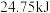 ,其热化学方程式为
,其热化学方程式为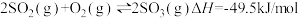
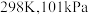 时,强酸与强碱的稀溶液发生中和反应的中和热为
时,强酸与强碱的稀溶液发生中和反应的中和热为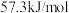 ,硫酸溶液与氢氧化钾溶液反应的热化学方程式为
,硫酸溶液与氢氧化钾溶液反应的热化学方程式为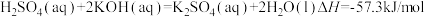
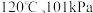 下,
下,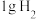 燃烧生成水蒸气放出
燃烧生成水蒸气放出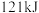 热量,其热化学方程式为:
热量,其热化学方程式为: