下列有关热化学方程式及其叙述正确的是( )
A.氢气的燃烧热为-285.5kJ/mol,则水电解的热化学方程式为: 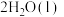 = =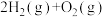 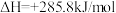 |
B.1mol甲烷完全燃烧生成O2和H2O(l)时放出890kJ热量,它的热化学方程式为: 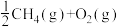 = =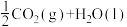  |
C.已知 = =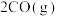 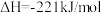 则C的燃烧热是110.5 则C的燃烧热是110.5 |
D.CH3COOH与NaOH溶液反应: 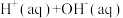 = = △H=-57.3kJ•mol-1 △H=-57.3kJ•mol-1 |
更新时间:2020-10-16 07:08:59
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
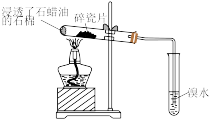
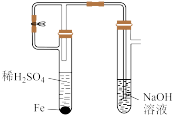
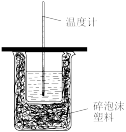
【推荐1】用下列装置和药品进行相应实验,能达到实验目的是
验证 易溶于水且溶液呈碱性 易溶于水且溶液呈碱性 | 证明石蜡油中含有不饱和烃 |
|
|
| A | B |
制备 | 测定中和反应的反应热 |
|
|
| C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法或表示法错误的是
| A.吸热反应是由于反应物的总能量比生成物的总能量低 |
| B.放热反应的ΔH<0 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.酸碱中和反应都是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列判断正确的是
| A.反应 TiO2(s)+2Cl2(g) = TiCl4(g) +O2(g) △H>0能自发进行,其原因是△S>0 |
| B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)⇌2NH3(g)△H=-38.6kJ•mol-1 |
| C.0.5mol H2SO4与0.5mol Ba(OH)2反应生成1 mol H2O时的反应热叫中和热 |
| D.已知H﹣H键能436 kJ•mol﹣1,F﹣F键能157 kJ•mol﹣1,H﹣F键能568 kJ•mol﹣1,则H2(g)+F2(g)=2HF(g) △H=﹣25 kJ•mol﹣1 |
您最近一年使用:0次
【推荐1】下列依据热化学方程式得出的结论正确的是
选项 | 热化学方程式 | 结论 |
A | H2(g)+Cl2(g) 2HCl(g) ΔH=-a kJ·mol-1 2HCl(g) ΔH=-a kJ·mol-1 | H2的燃烧热ΔH=-a kJ·mol-1 |
B | OH-(aq)+H+(aq)==H2O(l) ΔH=-57.3 kJ·mol-1 | 溶质物质的量为0.5 mol的Ba(OH)2稀溶液与足量稀H2SO4完全中和,放出的热量等于57.3 kJ |
C | C(s)+O2(g)=CO2(g) ΔH=-a kJ·mol-1; C(s)+  O2(g)=CO(g) ΔH=-b kJ·mol-1 O2(g)=CO(g) ΔH=-b kJ·mol-1 | b<a |
D | P4(s,白磷)=4P(s,红磷) ΔH=-29.2 kJ·mol-1 | P4(s,白磷)比P(s,红磷)稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol。下列说法正确的是( )
| A.在相同条件下,2L氢气与1L氧气化合生成2L水蒸气放出483.6kJ热量 |
B.H2(g)+ O2(g)=H2O(l) ΔH=-Q1 kJ/mol,则Q1>241.8 O2(g)=H2O(l) ΔH=-Q1 kJ/mol,则Q1>241.8 |
| C.H2的燃烧热为241.8kJ/mol |
| D.2mol氢气与1 mol氧气反应生成2mol水的反应热为483.6kJ/mol |
您最近一年使用:0次