钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
I.如图装置中,U 形管内为红墨水,a、b 试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于____ 腐蚀。

(1)红墨水柱两边的液面变为左低右高,则_____ (填“a”或“b”)边盛有食盐水。
(2)b 试管中铁发生的是_____ 腐蚀。
II.下面两个图都是金属防护的例子。
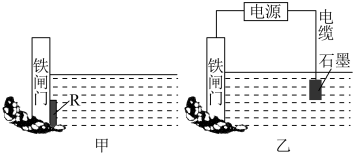
(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R 可以采用_______ (从下面选项中选择),此方法叫做_____ 保护法。 A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的______ 极。
(5)采取以上两种方法,_________ (填“甲”或“乙”)种能使铁闸门保护得更好。
I.如图装置中,U 形管内为红墨水,a、b 试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于

(1)红墨水柱两边的液面变为左低右高,则
(2)b 试管中铁发生的是
II.下面两个图都是金属防护的例子。

(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R 可以采用
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的
(5)采取以上两种方法,
20-21高二上·福建三明·阶段练习 查看更多[2]
福建省三明第一中学2020-2021学年高二上学期第一次月考化学试题(已下线)第28讲 金属的腐蚀与防护(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
更新时间:2020-10-16 15:03:42
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)天然气和可燃冰(mCH4·nH2O)既是高效洁净的能源,也是重要的化工原料,
①甲烷分子的空间构型为__________ ,可燃冰(mCH4·nH2O)属于________ 晶体。
②已知25℃、101kPa时,1g甲烷完全燃烧生成液态水放出55.65kJ热量,则该条件下反应
CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H=______ kJ·mol-1
(2)用甲烷-氧气碱性(KOH溶液)燃料电池作电源,电解CuCl2溶液。反应装置如下图所示:
①b电极名称为___________ ,d电极的电极反应式为_________ 。
②假设CuCl2溶液足量,当某电极上析出3.2g金属Cu时,理论上燃料电池消耗氧气在标准状况下的体积是______ mL。
(3)在相同条件下,下面各组热化学方程式中,△H1<△H2的是________ 。(填字母)
A组:2H2(g)+O2(g)=2H2O(g) △H12H2(g)+O2(g)═2H2O(l) △H2
B组:S(g)+O2(g)=SO2(g) △H1S(s)+O2(g)=SO2(g) △H2
C组:C(s)+1/2O2(g)=CO(g) △H1C(s)+O2(g)=CO2(g) △H2
D组:CO(g)+1/2O2(g)=CO2(g) △H12CO(g)+O2(g)=2CO2(g) △H2
(4)25℃,10lkPa条件下,14gN2和3gH2应生成NH3的能量变化如下图所示:
已知:①x=1127;
②25℃101kPa下,N2(g)+3H2(g) 2NH3(g) △H=-92kJ·mol-1。则y=
2NH3(g) △H=-92kJ·mol-1。则y=___________ 。
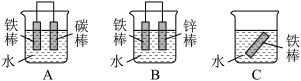
(5)金属材料的腐蚀是人类面临的严重问题,金属的防腐对节约能源、保护环境起着十分重要的作用。下列三个装置中,铁被腐蚀速率由快到慢的顺序为_________ (填字母)。
(1)天然气和可燃冰(mCH4·nH2O)既是高效洁净的能源,也是重要的化工原料,
①甲烷分子的空间构型为
②已知25℃、101kPa时,1g甲烷完全燃烧生成液态水放出55.65kJ热量,则该条件下反应
CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H=
(2)用甲烷-氧气碱性(KOH溶液)燃料电池作电源,电解CuCl2溶液。反应装置如下图所示:

①b电极名称为
②假设CuCl2溶液足量,当某电极上析出3.2g金属Cu时,理论上燃料电池消耗氧气在标准状况下的体积是
(3)在相同条件下,下面各组热化学方程式中,△H1<△H2的是
A组:2H2(g)+O2(g)=2H2O(g) △H12H2(g)+O2(g)═2H2O(l) △H2
B组:S(g)+O2(g)=SO2(g) △H1S(s)+O2(g)=SO2(g) △H2
C组:C(s)+1/2O2(g)=CO(g) △H1C(s)+O2(g)=CO2(g) △H2
D组:CO(g)+1/2O2(g)=CO2(g) △H12CO(g)+O2(g)=2CO2(g) △H2
(4)25℃,10lkPa条件下,14gN2和3gH2应生成NH3的能量变化如下图所示:

已知:①x=1127;
②25℃101kPa下,N2(g)+3H2(g)
 2NH3(g) △H=-92kJ·mol-1。则y=
2NH3(g) △H=-92kJ·mol-1。则y=(5)金属材料的腐蚀是人类面临的严重问题,金属的防腐对节约能源、保护环境起着十分重要的作用。下列三个装置中,铁被腐蚀速率由快到慢的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)与钢铁比,纯净的铁有很强的抗腐蚀性,原因是____ 。氯化铁受热会发生升华现象,这说明氯化铁是______ (选填“离子”、“共价”)化合物。
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:Fe(s)+CO2(g) FeO(s)+CO(g),该反应的平衡常数表达式K=
FeO(s)+CO(g),该反应的平衡常数表达式K=_____________ 。下列措施中能使平衡时c(CO)/c(CO2)增大的是________ (选填编号)
a.升高温度 b.增大压强 c.充入一定量CO d.再加入一些铁粉
(3)FeS2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-形式存在,请完成该反应的化学方程式。
______________________________________________________________________
(4)溶液的酸碱性对许多物质的氧化性有很大影响;生成物的溶解性会影响复分解反应的方向。将Na2S溶液滴加到FeCl3溶液中,有单质硫生成;将FeCl3溶液滴加到Na2S溶液中生成的是Fe2S3而不是S或Fe(OH)3从以上反应可得出的结论是________________________________ 。
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:Fe(s)+CO2(g)
 FeO(s)+CO(g),该反应的平衡常数表达式K=
FeO(s)+CO(g),该反应的平衡常数表达式K=a.升高温度 b.增大压强 c.充入一定量CO d.再加入一些铁粉
(3)FeS2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-形式存在,请完成该反应的化学方程式。
(4)溶液的酸碱性对许多物质的氧化性有很大影响;生成物的溶解性会影响复分解反应的方向。将Na2S溶液滴加到FeCl3溶液中,有单质硫生成;将FeCl3溶液滴加到Na2S溶液中生成的是Fe2S3而不是S或Fe(OH)3从以上反应可得出的结论是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】亚氯酸钠( )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:① 的溶解度随温度升高而增大,适当条件下可结晶析出
的溶解度随温度升高而增大,适当条件下可结晶析出 。
。
②纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
(1)钠元素在周期表的位置___________ ; 的电子式
的电子式____________
(2)发生器中鼓入空气的作用可能是_____________ (选填序号).
a.将 氧化成
氧化成 ,增强酸性 b.稀释
,增强酸性 b.稀释 以防止爆炸
以防止爆炸
c.将 氧化成
氧化成 d.加大容器压强,加快反应速率
d.加大容器压强,加快反应速率
(3)吸收塔内发生反应的化学方程式:___________________________ ;
(4)从滤液中得到 ,粗晶体的实验操作依次是
,粗晶体的实验操作依次是_________ (选填序号)。
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
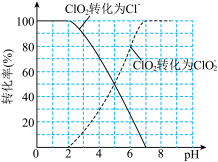
(5) 被
被 还原为
还原为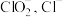 的转化率与溶液pH的关系如图所示。
的转化率与溶液pH的关系如图所示。 时,被S2-还原的产物ClO2-、Cl-物质的量的比
时,被S2-还原的产物ClO2-、Cl-物质的量的比______ ;写出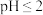 时
时 与
与 反应的离子方程式
反应的离子方程式______________________ 。
Ⅱ.铁和铜及其化合物在人类生产生活中具有重要作用,回答下列问题:
(6)中国古代四大发明之一的司南由天然磁石制成。其主要成分是__________ (填字母序号)。
a. b.
b. c.
c. d.
d.
(7)中国古代制造的青铜器久置空气中发生电化学腐蚀生成铜绿,则正极反应式为___________ ,若利用稀盐酸擦拭铜绿,其离子方程式为___________________ 。
 )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
已知:①
 的溶解度随温度升高而增大,适当条件下可结晶析出
的溶解度随温度升高而增大,适当条件下可结晶析出 。
。②纯
 易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。(1)钠元素在周期表的位置
 的电子式
的电子式(2)发生器中鼓入空气的作用可能是
a.将
 氧化成
氧化成 ,增强酸性 b.稀释
,增强酸性 b.稀释 以防止爆炸
以防止爆炸c.将
 氧化成
氧化成 d.加大容器压强,加快反应速率
d.加大容器压强,加快反应速率(3)吸收塔内发生反应的化学方程式:
(4)从滤液中得到
 ,粗晶体的实验操作依次是
,粗晶体的实验操作依次是a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
(5)
 被
被 还原为
还原为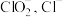 的转化率与溶液pH的关系如图所示。
的转化率与溶液pH的关系如图所示。 时,被S2-还原的产物ClO2-、Cl-物质的量的比
时,被S2-还原的产物ClO2-、Cl-物质的量的比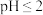 时
时 与
与 反应的离子方程式
反应的离子方程式
Ⅱ.铁和铜及其化合物在人类生产生活中具有重要作用,回答下列问题:
(6)中国古代四大发明之一的司南由天然磁石制成。其主要成分是
a.
 b.
b. c.
c. d.
d.
(7)中国古代制造的青铜器久置空气中发生电化学腐蚀生成铜绿,则正极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】研究金属腐蚀和防腐的原理很有现实意义。

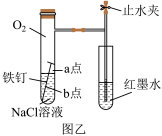
(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有___________(填序号)。
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化如下表,根据数据判断腐蚀的速率随时间逐渐___________ (填“加快”、“不变”、“减慢”),你认为影响因素为___________ 。
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,请完成表格空白:
根据以上实验探究,试判断___________ (填“a”或“b”)为负极,该点腐蚀更严重。
(4)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于 溶液中,一定条件下Fe钝化形成致密
溶液中,一定条件下Fe钝化形成致密 氧化膜,试写出该阳极电极反应式
氧化膜,试写出该阳极电极反应式___________ 。


(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有___________(填序号)。
| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化如下表,根据数据判断腐蚀的速率随时间逐渐
| 时间/min | 1 | 3 | 5 | 7 | 9 |
| 液柱高度/cm | 0.8 | 2.1 | 3.0 | 3.7 | 4.2 |
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,请完成表格空白:
| 实验操作 | 实验现象 |
| 向NaCl溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 |
| 然后再滴加2~3滴② | b点周围出现蓝色沉淀 |
(4)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于
 溶液中,一定条件下Fe钝化形成致密
溶液中,一定条件下Fe钝化形成致密 氧化膜,试写出该阳极电极反应式
氧化膜,试写出该阳极电极反应式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】“阳光”牌小包装“脱氧剂”成分为Fe粉、活性炭及少量NaCl、水,使用一段时间后Fe粉会变质。某校化学兴趣小组欲探究使用过的 “脱氧剂”的变质程度(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行了如下探究过程,请你参与实验并回答有关问题。
步骤⑴取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末。由此得出的结论为上述“脱氧剂”中的铁已变质,发生了_______ 腐蚀,生成的铁锈主要成分是________ (填化学式);
步骤⑵将步骤⑴中的固体溶于水,过滤,将滤渣洗涤、干燥。该步骤的目的是_________ ;
步骤⑶ 取步骤⑵中的滤渣,将其分为两等份,每一份质量为8.0g。将其中一份在氧气流中充分灼烧,生成的气体全部通入足量的澄清石灰水,得到干燥、纯净的沉淀20.0 g。据此计算8.0 g滤渣中活性炭的质量为_______________ ;
步骤⑷ 将步骤⑶中的另一份滤渣放入烧杯中,加入一定体积2.0mol/L的稀H2SO4,微热至反应完全。为保证滤渣充分溶解,加入的稀H2SO4的体积应大于或等于__________ mL;
步骤⑸ 向步骤⑷中的混合物中加入过量的氢氧化钠溶液,得到的固体经洗涤后转移到坩埚中充分加热,冷却、称量,得到6.86g固体。
结论:该“脱氧剂”中的Fe粉和活性炭质量之比为_______________ 。
步骤⑴取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末。由此得出的结论为上述“脱氧剂”中的铁已变质,发生了
步骤⑵将步骤⑴中的固体溶于水,过滤,将滤渣洗涤、干燥。该步骤的目的是
步骤⑶ 取步骤⑵中的滤渣,将其分为两等份,每一份质量为8.0g。将其中一份在氧气流中充分灼烧,生成的气体全部通入足量的澄清石灰水,得到干燥、纯净的沉淀20.0 g。据此计算8.0 g滤渣中活性炭的质量为
步骤⑷ 将步骤⑶中的另一份滤渣放入烧杯中,加入一定体积2.0mol/L的稀H2SO4,微热至反应完全。为保证滤渣充分溶解,加入的稀H2SO4的体积应大于或等于
步骤⑸ 向步骤⑷中的混合物中加入过量的氢氧化钠溶液,得到的固体经洗涤后转移到坩埚中充分加热,冷却、称量,得到6.86g固体。
结论:该“脱氧剂”中的Fe粉和活性炭质量之比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.某同学将一试管斜立倒置于水槽中,并在试管内放了一枚铁钉,放置数天后观察:
(1)若试管内液面上升,则发生_____________ 腐蚀,正极反应式为______________ 。
(2)若试管内液面下降,则发生_____________ 腐蚀,负极反应式为_____________ 。
Ⅱ.如图所示装置,两玻璃管中盛满滴有酚酞的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
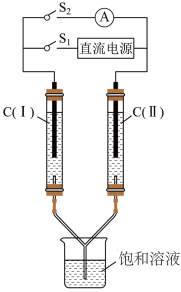
(1)接通S1 后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,此时:该装置名称为_______________________ 。
(2)C(Ⅱ)的电极名称是______________________ (填写正极或负极)
(1)若试管内液面上升,则发生
(2)若试管内液面下降,则发生
Ⅱ.如图所示装置,两玻璃管中盛满滴有酚酞的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。

(1)接通S1 后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,此时:该装置名称为
(2)C(Ⅱ)的电极名称是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】根据如图所示实验装置,回答相关问题。
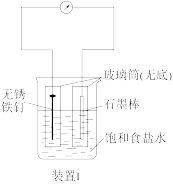
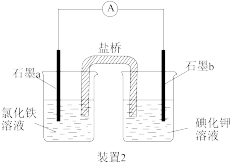
(1)“装置1”中铁钉发生的电化学腐蚀类型为___________ ,石墨电极的电极反应式为___________ 。
(2)“装置2”中外电路电子的移动方向为___________ (填“由a到b”或“由b到a”),该装置发生的总反应的离子方程式为___________ 。
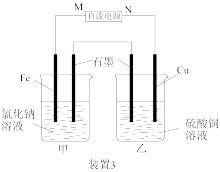
(3)“装置3”中甲烧杯盛有100mL0.2mol/LNaCl溶液,乙烧杯盛有100mL0.5mol/LCuSO4溶液。一段时间后,铜电极增重1.28g。
①直流电源的M端为___________ 极,乙烧杯中电解反应的化学方程式为___________ 。
②装置3产生的气体在标准状况下的体积为___________ mL;欲恢复乙烧杯中的溶液至电解前的状态,可加入___________ (填字母标号)。
a.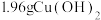 b.1.6gCuO
b.1.6gCuO
c.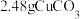 d.
d.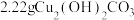



(1)“装置1”中铁钉发生的电化学腐蚀类型为
(2)“装置2”中外电路电子的移动方向为
(3)“装置3”中甲烧杯盛有100mL0.2mol/LNaCl溶液,乙烧杯盛有100mL0.5mol/LCuSO4溶液。一段时间后,铜电极增重1.28g。
①直流电源的M端为
②装置3产生的气体在标准状况下的体积为
a.
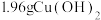 b.1.6gCuO
b.1.6gCuOc.
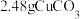 d.
d.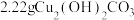
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】全世界每年被腐蚀损耗的钢铁量非常惊人,在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因。
(1)在潮湿空气中,钢铁发生吸氧腐蚀时的负极反应的电极反应式为_____________ 。
(2)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4 CO↑ + CO2↑ + H2O,
CO↑ + CO2↑ + H2O,
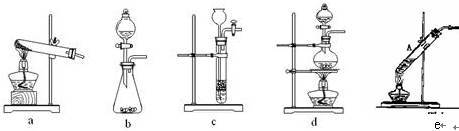
下列装置中,可用作草酸分解制取气体的是______ (填答案编号)。
(3)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3·nH2O和Fe两种成分),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
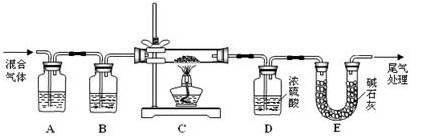
①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次可能是_______ 、
________ (填答案编号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液 d.无水氯化钙
②在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;(b)____________ 。
③E装置的作用是______________________________________________________ ,
上述装置最后尾气处理的方法是_____________ 。
④准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n =________ 。
⑤在本实验中,下列情况会使测定结果n偏大的是__________ (填答案编号)。
a.缺少装置B b.缺少装置E c.反应后的固体中有少量Fe2O3·nH2O
(1)在潮湿空气中,钢铁发生吸氧腐蚀时的负极反应的电极反应式为
(2)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4
 CO↑ + CO2↑ + H2O,
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是

(3)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3·nH2O和Fe两种成分),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。

①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次可能是
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液 d.无水氯化钙
②在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;(b)
③E装置的作用是
上述装置最后尾气处理的方法是
④准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n =
⑤在本实验中,下列情况会使测定结果n偏大的是
a.缺少装置B b.缺少装置E c.反应后的固体中有少量Fe2O3·nH2O
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】从“铁器时代”开始,铁单质及其化合物一直备受青睐。
Ⅰ.古代铁质文物的腐蚀研究
(1)古代兵器中铜质部件修饰铁质兵刃反倒使兵刃更易生锈,其主要原因为_________ 。
(2)已知:i.铁质文物在潮湿的土壤中主要发生吸氧腐蚀,表面生成疏松的FeOOH;
ii.铁质文物在干燥的土壤中表面会生成致密的 ,过程如下:
,过程如下:
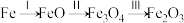
①写出i中 参与的电极反应式为
参与的电极反应式为___________________ 。
②若ii中每一步反应转化的铁元素质量相等,则三步反应中电子转移数之比为___________ 。
Ⅱ.铁的冶炼
(3)工业上采用高炉炼铁法冶炼铁单质,其反应的热化学方程式为:
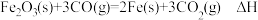
已知:
①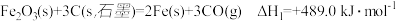 ;
;
②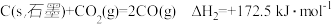 。
。
则
___________ 。
Ⅲ.现代对含铁化合物的应用
(4)电子工业中常常用 溶液为“腐蚀液”与覆铜板反应用于制备印刷电路板,其反应的离子方程式为
溶液为“腐蚀液”与覆铜板反应用于制备印刷电路板,其反应的离子方程式为____________ 。
(5)高铁酸钾( )是一种强氧化剂,可用作水处理剂和高容量电池材料。
)是一种强氧化剂,可用作水处理剂和高容量电池材料。
①将 加入KClO与KOH的混合液中可以制得
加入KClO与KOH的混合液中可以制得 溶液,其反应的离子方程式为
溶液,其反应的离子方程式为___________________ 。
②已知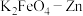 碱性锌电池的电池反应为:
碱性锌电池的电池反应为: 。写出其正极反应式
。写出其正极反应式______ 。
Ⅰ.古代铁质文物的腐蚀研究
(1)古代兵器中铜质部件修饰铁质兵刃反倒使兵刃更易生锈,其主要原因为
(2)已知:i.铁质文物在潮湿的土壤中主要发生吸氧腐蚀,表面生成疏松的FeOOH;
ii.铁质文物在干燥的土壤中表面会生成致密的
 ,过程如下:
,过程如下: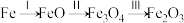
①写出i中
 参与的电极反应式为
参与的电极反应式为②若ii中每一步反应转化的铁元素质量相等,则三步反应中电子转移数之比为
Ⅱ.铁的冶炼
(3)工业上采用高炉炼铁法冶炼铁单质,其反应的热化学方程式为:
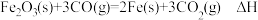
已知:
①
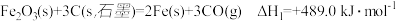 ;
;②
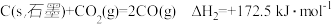 。
。则

Ⅲ.现代对含铁化合物的应用
(4)电子工业中常常用
 溶液为“腐蚀液”与覆铜板反应用于制备印刷电路板,其反应的离子方程式为
溶液为“腐蚀液”与覆铜板反应用于制备印刷电路板,其反应的离子方程式为(5)高铁酸钾(
 )是一种强氧化剂,可用作水处理剂和高容量电池材料。
)是一种强氧化剂,可用作水处理剂和高容量电池材料。①将
 加入KClO与KOH的混合液中可以制得
加入KClO与KOH的混合液中可以制得 溶液,其反应的离子方程式为
溶液,其反应的离子方程式为②已知
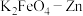 碱性锌电池的电池反应为:
碱性锌电池的电池反应为: 。写出其正极反应式
。写出其正极反应式
您最近一年使用:0次



