某无色透明溶液中除了H+和OH-,可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+、 、
、 中的几种,请填写下列空白:
中的几种,请填写下列空白:
(1)不用做任何实验就可以肯定原溶液中一定不存在的离子是_________ ,一定存在的离子是__________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是______________ 。
(3)取(2)中滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有______ ,写出加入氢氧化钠溶液发生反应的离子方程式:__________ 。
 、
、 中的几种,请填写下列空白:
中的几种,请填写下列空白:(1)不用做任何实验就可以肯定原溶液中一定不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
更新时间:2020-11-10 21:54:27
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如图所示(部分产物已略去):

(1)写出用惰性电极电解M溶液的离子方程式____________。写出F的电子式____________。
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是___________________。
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如图所示,“则A与B溶液”反应后溶液中的溶质为______________(填化学式)。
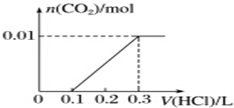
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所能观察到的实验现象是___________________。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚后溶液显紫色,则由A转化成E的离子方程式是__________;
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,请写出足量E与D反应的化学方程式________________。
(7)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32﹣中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其浓度之比为_______________________。


(1)写出用惰性电极电解M溶液的离子方程式____________。写出F的电子式____________。
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是___________________。
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如图所示,“则A与B溶液”反应后溶液中的溶质为______________(填化学式)。

(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所能观察到的实验现象是___________________。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚后溶液显紫色,则由A转化成E的离子方程式是__________;
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,请写出足量E与D反应的化学方程式________________。
(7)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32﹣中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其浓度之比为_______________________。

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。
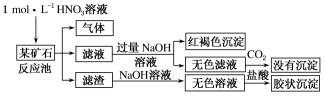
(1)Si在周期表中的位置是____________________ 。
(2)下列说法正确的是______________ 。
a.酸性:H2CO3>H2SiO3b.结合质子的能力:CO32->AlO2->HCO3-
c.稳定性:H2O>CH4>SiH4d.离子半径:O2-<Al3+
(3)该矿石的组成是_____ ,滤渣和NaOH溶液反应的离子方程式是______________ 。
(4)该矿石和1 mol L-1HNO3反应的离子方程式________________________________ 。
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,用化学方程式解释该方法的目的:____________________ ;若按以上方案:NO与O2循环通入反应池处理该矿石2.36103kg,得到滤渣1.2103kg,理论上至少需要1 mol L-1HNO3的体积为_____ L。

(1)Si在周期表中的位置是
(2)下列说法正确的是
a.酸性:H2CO3>H2SiO3b.结合质子的能力:CO32->AlO2->HCO3-
c.稳定性:H2O>CH4>SiH4d.离子半径:O2-<Al3+
(3)该矿石的组成是
(4)该矿石和1 mol L-1HNO3反应的离子方程式
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,用化学方程式解释该方法的目的:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】由A、B、C、D、E五种溶液,其组成的阳离子有Na+、Fe3+、Ba2+、Al3+、Ag+,阴离子有NO 、OH-、SO
、OH-、SO 、Cl-、CO
、Cl-、CO (在溶液中离子不重复出现)。现做如下实验:
(在溶液中离子不重复出现)。现做如下实验:
①A和E溶液显碱性,0.1mol/L的A溶液的pH小于13;
②在B溶液中逐渐加入氨水有白色沉淀生成,继续加入氨水至过量,沉淀消失;
③在C溶液中加入铁粉,溶液的质量增加;
④在D溶液中加入过量Ba(OH) 2溶液,没有沉淀
(1)A是______ ;B是______ ;C是______ ;D是______ ;E是______ ;
(2)写出实验② 中有关反应的离子方程式________________ 。
 、OH-、SO
、OH-、SO 、Cl-、CO
、Cl-、CO (在溶液中离子不重复出现)。现做如下实验:
(在溶液中离子不重复出现)。现做如下实验:①A和E溶液显碱性,0.1mol/L的A溶液的pH小于13;
②在B溶液中逐渐加入氨水有白色沉淀生成,继续加入氨水至过量,沉淀消失;
③在C溶液中加入铁粉,溶液的质量增加;
④在D溶液中加入过量Ba(OH) 2溶液,没有沉淀
(1)A是
(2)写出实验② 中有关反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
为了鉴别上述化合物.分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)C常用作净水剂,写出C、D的化学式:C______ ,D______ 。
(2)A是侯氏制碱的产物之一,将含1mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:_____________________ 。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为_____________________ 。
(4)若向含溶质0.5mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为_________ g。
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42﹣ HCO3﹣ NO3﹣ OH﹣ |
为了鉴别上述化合物.分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)C常用作净水剂,写出C、D的化学式:C
(2)A是侯氏制碱的产物之一,将含1mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:
(3)在A溶液中加入少量澄清石灰水,其离子方程式为
(4)若向含溶质0.5mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe2+、Ba2+、H+、SO42-、CO32-。为了进一步确认,对该溶液进行实验检测:

步骤一:仔细观察,该溶液呈无色、透明、均一状态。
步骤二:加入足量BaCl2溶液,生成23.3g 白色沉淀,再加稀硝酸,沉淀不消失。
(1)原溶液中除上图中的离子以外,肯定还含有的离子是________ ,肯定不含有的离子是________ 。
(2)实验操作的步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、______________ 、检验沉淀已洗干净的方法是____________ 。
(3)原溶液中H+物质的量浓度为_________ mol/L。
(4)向原溶液中加入NaHCO3溶液,反应的离子方程式为_____________ 。
(5)若向100 mL原溶液中加入1mo/L 的Ba(OH)2溶液,当生成的沉淀质量刚好最大时,则加入的Ba(OH)2溶液体积为_________ L。

步骤一:仔细观察,该溶液呈无色、透明、均一状态。
步骤二:加入足量BaCl2溶液,生成23.3g 白色沉淀,再加稀硝酸,沉淀不消失。
(1)原溶液中除上图中的离子以外,肯定还含有的离子是
(2)实验操作的步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、
(3)原溶液中H+物质的量浓度为
(4)向原溶液中加入NaHCO3溶液,反应的离子方程式为
(5)若向100 mL原溶液中加入1mo/L 的Ba(OH)2溶液,当生成的沉淀质量刚好最大时,则加入的Ba(OH)2溶液体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G 的浓溶液中发生钝化, F 的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。请讨论以下两种情况(注:两种情况下各字母代表的物质可能不同)

(1)第一种情况:A为气体;用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
① B与甲反应的化学方程式为________________________________________ 。
② D与乙反应的离子方程式为_______________________________________ 。
(2)第二种情况:A为黄色固体;甲可由两种单质直接化合得到; D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
① 工业上,反应 I 在___________________ (填设备名称)中进行。
② 甲的化学式为______________ 。
③ D和乙反应的离子方程式为________________________________________ 。
④ 请简述检验G溶液中阴离子的方法____________________________________
⑤ 若A的相对分子质量为M,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=_______ (列出计算式即可)。

(1)第一种情况:A为气体;用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
① B与甲反应的化学方程式为
② D与乙反应的离子方程式为
(2)第二种情况:A为黄色固体;甲可由两种单质直接化合得到; D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
① 工业上,反应 I 在
② 甲的化学式为
③ D和乙反应的离子方程式为
④ 请简述检验G溶液中阴离子的方法
⑤ 若A的相对分子质量为M,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=
您最近一年使用:0次



