下表是生活生产中常见的物质:
(1)请你对表中①-⑥的物质进行分类(填序号):属于电解质的是____ ;属于非电解质的是__ ;________ 属于盐;
(2)写出电离方程式:
②的电离方程式是________ ;
③的电离方程式是________ ;
(3)写出下列物质在水溶液中反应的离子方程式:
②与③反应的离子方程式:________ ;
③与⑤反应的离子方程式:__________ ;
③与⑥反应的离子方程式:________ 。
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 名称 | Na | NaOH | H2SO4 | 酒精 | BaCl2 | Na2CO3 |
(1)请你对表中①-⑥的物质进行分类(填序号):属于电解质的是
(2)写出电离方程式:
②的电离方程式是
③的电离方程式是
(3)写出下列物质在水溶液中反应的离子方程式:
②与③反应的离子方程式:
③与⑤反应的离子方程式:
③与⑥反应的离子方程式:
更新时间:2020-11-24 14:02:14
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】无机化合物可根据其组成和性质进行分类。
(1)如图所示的物质分类方法的名称是______________ 。

(2)
以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥后面。
(3)写出⑦转化为⑤的化学方程式_______ 。
(1)如图所示的物质分类方法的名称是

(2)
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(3)写出⑦转化为⑤的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】二氧化硫是形成酸雨的“罪魁祸首”,为了保护环境,应减少SO2在大气中的排放。请回答下列问题:
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?___ 。
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:___ ;
②NaHSO3:___ 。
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
SO3与NaOH溶液反应可生成NaHSO4。已知:NaHSO4=Na++H++SO42-,则NaHSO4是酸类物质吗?__ 。
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:
②NaHSO3:
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
SO3与NaOH溶液反应可生成NaHSO4。已知:NaHSO4=Na++H++SO42-,则NaHSO4是酸类物质吗?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有下列十种物质:①O2;②Fe;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁胶体;⑧硫酸钠溶液;⑨稀硝酸;⑩Cu2(OH)2CO3。
(1)按物质的树状分类法填写表格的空白处:
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学反应方程式为_________ 。
(3)③与⑨发生反应的离子方程式为____________ 。
(4)②与⑨发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原剂是____________ 、氧化剂是____________ (填化学式)。
(1)按物质的树状分类法填写表格的空白处:
| 分类标准 | 氧化物 | 电解质 | |||
| 属于该类的物质 | ② | ⑧⑨ | ⑦ |
(3)③与⑨发生反应的离子方程式为
(4)②与⑨发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)化工生产中常用到“三酸两碱”,其中“两碱”指烧碱和纯碱,从物质的分类角度看,不恰当的一种物质是___________ (填名称)。
(2)下列几种物质的电离方程式如下: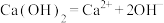 ;
;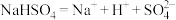 ;
; ;属于酸的物质为
;属于酸的物质为________ (填化学式),写出该酸与小苏打反应的离子方程式:________ 。
(3)在如图所示的串联装置中,打开电源后,发现灯泡不亮。

①上述装置A~D中物质,属于电解质的是___________ ,若保持装置不变,要使灯泡变亮,可进行的操作是___________ 。
②进行①中操作后,向烧杯B中逐渐滴入 溶液,灯泡的亮度变化为
溶液,灯泡的亮度变化为___________ 。
③ 是三元酸,能生成
是三元酸,能生成 、
、 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸(
一种正盐。磷还有一种含氧酸叫亚磷酸( ),若
),若 与NaOH反应生成的
与NaOH反应生成的 为正盐,
为正盐, 属于
属于______ (填字母)。
a.一元酸 b.二元酸 c.三元酸
(1)化工生产中常用到“三酸两碱”,其中“两碱”指烧碱和纯碱,从物质的分类角度看,不恰当的一种物质是
(2)下列几种物质的电离方程式如下:
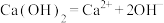 ;
;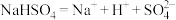 ;
; ;属于酸的物质为
;属于酸的物质为(3)在如图所示的串联装置中,打开电源后,发现灯泡不亮。

①上述装置A~D中物质,属于电解质的是
②进行①中操作后,向烧杯B中逐渐滴入
 溶液,灯泡的亮度变化为
溶液,灯泡的亮度变化为③
 是三元酸,能生成
是三元酸,能生成 、
、 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸(
一种正盐。磷还有一种含氧酸叫亚磷酸( ),若
),若 与NaOH反应生成的
与NaOH反应生成的 为正盐,
为正盐, 属于
属于a.一元酸 b.二元酸 c.三元酸
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】根据所学知识填空:
(1)下列几种物质:①CO2 ②CaO ③酒精 ④KOH ⑤BaSO4 ⑥Cu ⑦NH3 ⑧熔融NaCl ⑨氨水 ⑩食盐水。其中属于电解质的是:_______ (填序号,以下均是);属于非电解质的是:_______ ;上述状态下能导电的是:_______ 。
(2)①标准状况下11.2 L H2S气体的质量为_______ ;
②与0.1 molOH-含有相同电子数的NH3在标准状况下的体积为_______ ;
③同温同压下,同体积的NH3和H2S气体的质量比为_______ ;
④同质量的NH3和H2S中氢原子的个数比为_______ 。
⑤在同温同压下,CO和CO2两种气体,密度比为_______ ,若两者质量相等,其体积比为_______ 。
(3)常温下将10.0 mL 2.0 mol·L-1的硝酸溶液加水稀释到400 mL。
①所得硝酸溶液的物质的量浓度为_______ ;
②若从稀释后的溶液中取出100 mL溶液,则溶液中含有硝酸的质量为_______ ,中和这100 mL 硝酸溶液需要0.08 mol·L-1 KOH溶液的体积是_______ 。之后若要获得KNO3晶体,需进行的实验操作是_______ (填操作名称)。
(1)下列几种物质:①CO2 ②CaO ③酒精 ④KOH ⑤BaSO4 ⑥Cu ⑦NH3 ⑧熔融NaCl ⑨氨水 ⑩食盐水。其中属于电解质的是:
(2)①标准状况下11.2 L H2S气体的质量为
②与0.1 molOH-含有相同电子数的NH3在标准状况下的体积为
③同温同压下,同体积的NH3和H2S气体的质量比为
④同质量的NH3和H2S中氢原子的个数比为
⑤在同温同压下,CO和CO2两种气体,密度比为
(3)常温下将10.0 mL 2.0 mol·L-1的硝酸溶液加水稀释到400 mL。
①所得硝酸溶液的物质的量浓度为
②若从稀释后的溶液中取出100 mL溶液,则溶液中含有硝酸的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.现有以下物质:①NaOH溶液;②蔗糖;③Ba(OH)2固体;④熔融KHSO4;⑤Fe(OH)3胶体:⑥NaHCO3;⑦CO2;⑧CH3COOH;⑨石墨
(1)以上物质中属于电解质的是___________ (填序号,下同);属于非电解质的是___________ ;
(2)以上物质属于纯净物且能导电的是___________ 。
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向Ba(OH)2溶液中滴加盐酸,测定导电率的变化如图所示,回答下列问题:
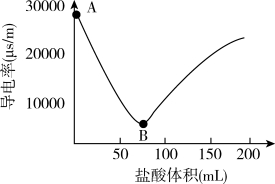
(3)Ba(OH)2在水中以离子形式存在的图示依据是___________ 。
(4)A-B段,发生的离子反应方程式是___________ 。
(5)B点恰好完全反应,此时溶液中存在的微粒主要有H2O、___________ 。
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是___________ 。
A.Ba(OH)2和H2SO4 B.NaOH 和H2SO4 C.Ba(OH)2与HNO3
(1)以上物质中属于电解质的是
(2)以上物质属于纯净物且能导电的是
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向Ba(OH)2溶液中滴加盐酸,测定导电率的变化如图所示,回答下列问题:

(3)Ba(OH)2在水中以离子形式存在的图示依据是
(4)A-B段,发生的离子反应方程式是
(5)B点恰好完全反应,此时溶液中存在的微粒主要有H2O、
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是
A.Ba(OH)2和H2SO4 B.NaOH 和H2SO4 C.Ba(OH)2与HNO3
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】①石墨 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤ 溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜
溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜
(1)其中能导电的是____ (填写符号,下同);属于电解质的是______ ;属于非电解质的是______ .
(2)写出物质⑤在水中的电离方程式:________ .
(3)写出物质⑥和⑨在水中发生反应的离子方程式:__________________ .
 溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜
溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜(1)其中能导电的是
(2)写出物质⑤在水中的电离方程式:
(3)写出物质⑥和⑨在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)下列都是中学化学常见的物质:A.Cu、B.CO2、C.NaHSO4、D.NaOH、E.H2SO4、F.C2H5OH(酒精)、G.BaSO4。请按下列分类标准回答:
①属于电解质的是________ (填序号,下同)。
②溶于水能电离出H+的是________ ,属于酸的是________ 。
(2)写出下列物质在水溶液中的电离方程式:
①Ba(OH)2________ 。
②(NH4)2SO4________ 。
③KHCO3________ 。
(3)写出下列反应的离子方程式:
①Zn与稀硫酸反应________ 。
②实验室制取CO2________ 。
③向Ba(OH)2溶液中加入稀硫酸________ 。
④Fe2O3体现碱性氧化物的性质________ 。
(1)下列都是中学化学常见的物质:A.Cu、B.CO2、C.NaHSO4、D.NaOH、E.H2SO4、F.C2H5OH(酒精)、G.BaSO4。请按下列分类标准回答:
①属于电解质的是
②溶于水能电离出H+的是
(2)写出下列物质在水溶液中的电离方程式:
①Ba(OH)2
②(NH4)2SO4
③KHCO3
(3)写出下列反应的离子方程式:
①Zn与稀硫酸反应
②实验室制取CO2
③向Ba(OH)2溶液中加入稀硫酸
④Fe2O3体现碱性氧化物的性质
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】酸碱盐是化学工业中的重要原料。回答下列问题:
(1)纯碱是重要的化工原料之一,写出其在水中的电离方程式_______ 。
(2)明矾 是常见的净水剂,属于
是常见的净水剂,属于_______ (填“酸”、“碱”或“盐”),实验室可以利用明矾和氨水制备 沉淀,其离子方程式为
沉淀,其离子方程式为_______ 。
(3)向两份相同的滴有酚酞的 溶液中,分别滴入导电能力大致相同的
溶液中,分别滴入导电能力大致相同的 、
、 溶液,混合溶液的导电能力随滴入溶液体积的变化曲线如下图所示。
溶液,混合溶液的导电能力随滴入溶液体积的变化曲线如下图所示。

①从开始至 点,除电导变化外,还观察到烧杯中的实验现象有
点,除电导变化外,还观察到烧杯中的实验现象有_______ 。
② 点溶液中大量存在的离子有
点溶液中大量存在的离子有_______ 。
③ 点溶液中发生中和的
点溶液中发生中和的 与未反应的
与未反应的 之比为
之比为_______ 。
(1)纯碱是重要的化工原料之一,写出其在水中的电离方程式
(2)明矾
 是常见的净水剂,属于
是常见的净水剂,属于 沉淀,其离子方程式为
沉淀,其离子方程式为(3)向两份相同的滴有酚酞的
 溶液中,分别滴入导电能力大致相同的
溶液中,分别滴入导电能力大致相同的 、
、 溶液,混合溶液的导电能力随滴入溶液体积的变化曲线如下图所示。
溶液,混合溶液的导电能力随滴入溶液体积的变化曲线如下图所示。
①从开始至
 点,除电导变化外,还观察到烧杯中的实验现象有
点,除电导变化外,还观察到烧杯中的实验现象有②
 点溶液中大量存在的离子有
点溶液中大量存在的离子有③
 点溶液中发生中和的
点溶液中发生中和的 与未反应的
与未反应的 之比为
之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】根据所学知识,回答下列问题
(1)以Na、K、H、O、C、S、N中任意两种或三种元素组成合适的物质,分别填在下表中。
(2)写出⑦转化为⑤的化学方程式:_____________________ 。
(3)写出①和④反应的相关化学方程式_____________ 。
(4)在化学学习中,我们经常用到一些指示剂用于检验某些溶液的酸碱性,例如,我们可以用酚酞检验④的溶液,当我们向待测液中滴入酚酞时,溶液变为__________ 色,再滴加稀硫酸至过量,写出相关的离子方程式___________ 。
(1)以Na、K、H、O、C、S、N中任意两种或三种元素组成合适的物质,分别填在下表中。
| 物质 类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(2)写出⑦转化为⑤的化学方程式:
(3)写出①和④反应的相关化学方程式
(4)在化学学习中,我们经常用到一些指示剂用于检验某些溶液的酸碱性,例如,我们可以用酚酞检验④的溶液,当我们向待测液中滴入酚酞时,溶液变为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】对于下列氧化还原反应,请按要求填空。
Cu + 4HNO3(浓)=== Cu(NO3)2+ 2NO2↑ + 2H2O
①用双线桥法标出电子转移的方向和数目_____________ ;
②氧化剂________ ,氧化产物__________ ;
③被还原的HNO3与参加反应的HNO3物质的量之比是_______ ;若有1molCu被氧化,则被还原的硝酸质量为 _____ g;若参加反应的硝酸为1.6mol,则放出气体的体积(在标准状况下)为___ L;
④离子方程式:_______ 。
Cu + 4HNO3(浓)=== Cu(NO3)2+ 2NO2↑ + 2H2O
①用双线桥法标出电子转移的方向和数目
②氧化剂
③被还原的HNO3与参加反应的HNO3物质的量之比是
④离子方程式:
您最近一年使用:0次



