下列说法不正确的是
| A.强电解质溶液的导电性不一定比弱电解质溶液的导电性强 |
| B.氯水能导电,但Cl2不是电解质 |
| C.SO2的水溶液可以导电,但SO2是非电解质 |
D.NaHSO4无论在水溶液里还是在熔融状态下都可以电离出Na+、H+和SO |
更新时间:2020-12-20 15:04:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
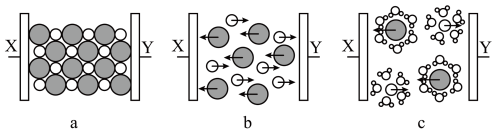
【推荐1】图a、b、c分别为氯化钠在不同状态下的导电实验的微观示意图(X、Y均表示石墨电极,且三个图中X、Y与直流电源连接方式均相同, 表示水分子),下列说法
表示水分子),下列说法不正确 的是
 表示水分子),下列说法
表示水分子),下列说法
A. 半径大于 半径大于 ,所以“●”代表 ,所以“●”代表 |
| B.图a为氯化钠固体,在通电情况下不导电说明NaCl不是电解质 |
| C.图b为熔融氯化钠,图c为氯化钠水溶液 |
| D.由图c可判断水合离子中H和O原子的朝向受到离子所带电荷种类的影响 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.液态 HCl、固态 AgCl 均不导电,所以 HCl、AgCl 是非电解质 |
| B.NH3、CO2 的水溶液均能导电,所 以 NH3、CO2 均是电解质 |
| C.金刚石、石墨、C60 是碳元素的同素异形体 |
| D.金属氧化物一定是碱性氧化物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关物质性质、结构的表述均正确,且存在因果关系的是:
表述Ⅰ | 表述Ⅱ | |
| A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中Cl—与Na+间的作用力大于碘晶体中分子间的作用力 |
| B | 通常条件下,CH4分子比SiH4分子稳定性高 | Si的原子半径比C的大,Si与H之间的键能比C与H间的小 |
| C | 在形成化合物时,同一主族元素的化合价相同 | 同一主族元素原子的最外层电子数相同 |
| D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】向100 mL 0.01 mol/LBa(OH)2溶液中滴加0.1 mol/L NaHCO3溶液,测得溶液的电导率变化如图。下列说法正确的是
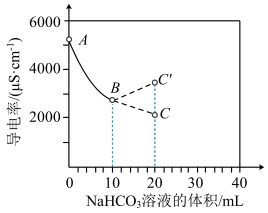

A.NaHCO3在水中的电离方程式为 |
| B.A→B的过程中,溶液中阳离子物质的量逐渐减小 |
| C.B点之后电导率变化为B→C |
D.B点之后发生的反应为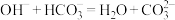 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法错误的是
①水是非电解质
②金属原子失电子越多,还原性越强
③固态氯化氢不导电,液态氯化氢可以导电
④硫酸氢钠在水中电离出的阳离子有氢离子,故硫酸氢钠是酸
⑤电解质溶于水形成的溶液一定能导电,非电解质溶于水形成的溶液一定不能导电
①水是非电解质
②金属原子失电子越多,还原性越强
③固态氯化氢不导电,液态氯化氢可以导电
④硫酸氢钠在水中电离出的阳离子有氢离子,故硫酸氢钠是酸
⑤电解质溶于水形成的溶液一定能导电,非电解质溶于水形成的溶液一定不能导电
| A.仅①④ | B.仅①④⑤ | C.仅②③ | D.①②③④⑤ |
您最近半年使用:0次



