按要求填空
(1)向CuCl2溶液中滴加NaOH溶液,现象:_________ ,离子方程式:_____ ,
(2)向NaHCO3溶液中滴加稀硫酸,现象:_____ ,离子方程式:_______ ;
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂_____ ,离子方程式;_____ 。
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂________ ,离子方程式__________ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀硫酸,现象:
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂
更新时间:2021-01-09 08:11:26
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有下列物质:①CO2 ②铜 ③硫酸 ④Na2CO3·10H2O晶体 ⑤石墨 ⑥Ba(OH)2固体 ⑦Al2(SO4)3固体 ⑧氨水 ⑨稀硝酸⑩C60按要求填空:
(1)上述物质中互为同素异形体的是______________________
(2)上述物质中属于电解质的有________ (填数字序号);能导电的是________ (填数字序号);
(3)写出⑦溶于水后形成溶液时的电离方程式:______________________
(4)上述物质中有两种物质之间可发生离子反应:H++OH-===H2O,写出该离子反应对应的化学方程式__________________________________ 。
(5)写出④和⑨反应的离子方程式:___________________________________ 。
(6)硫酸(H2SO4)、硝酸(HNO3)、磷酸(H3PO4)、氢硫酸(H2S)等都属于酸,从电离角度认识,其本质原因是:电离出的______________________
(1)上述物质中互为同素异形体的是
(2)上述物质中属于电解质的有
(3)写出⑦溶于水后形成溶液时的电离方程式:
(4)上述物质中有两种物质之间可发生离子反应:H++OH-===H2O,写出该离子反应对应的化学方程式
(5)写出④和⑨反应的离子方程式:
(6)硫酸(H2SO4)、硝酸(HNO3)、磷酸(H3PO4)、氢硫酸(H2S)等都属于酸,从电离角度认识,其本质原因是:电离出的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有化学中常见的一些物质:①空气 ②氯气 ③氢氧化钠 ④熔融状态的硝酸钾 ⑤铁 ⑥葡萄糖 ⑦硫酸 ⑧氯化铁溶液⑨碳酸氢钠⑩氨气。在以上物质中:
(1)属于单质的是_______ ,属于混合物的是_______ ;
(2)属于电解质的是_______ ,属于非电解质的是_______ ;
(3)属于酸的是_______ ,属于碱的是_______ ,属于盐(包括盐溶液)的是_______ ;
(4)上述物质在该状态下能导电的是_______
(5)写出⑨在水中的电离方程式:_______
(6)写出下列离子方程式
i.③和⑧反应:_______
ii.用⑨治疗胃酸(主要成分为盐酸)过多:_______ 。
(1)属于单质的是
(2)属于电解质的是
(3)属于酸的是
(4)上述物质在该状态下能导电的是
(5)写出⑨在水中的电离方程式:
(6)写出下列离子方程式
i.③和⑧反应:
ii.用⑨治疗胃酸(主要成分为盐酸)过多:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】无土栽培是一种在营养液中培育植物的高新技术,有良好的发展前景
Ⅰ.表为某“水培绿叶营养液的成分
(1)上述各成分均属于___________(填字母)
(2) 该营养液中,
该营养液中, 的物质的量浓度为
的物质的量浓度为_____  。
。
①需要用托盘天平称取 固体的质量为
固体的质量为______  。
。
②在配制过程中,下列操作会使所配溶液浓度偏低的是______ (填字母)
A.定容时,俯视刻度线 B.摇匀后液面低于刻度线,加水至刻度线
C.容量瓶中事先含有少量蒸馏水 D.未将烧杯的洗涤液转移至容量瓶中
Ⅱ.某水培営养液中可能含有 和
和 ,为确定其成分,进行如下实验:
,为确定其成分,进行如下实验:
①加入过量 溶液,无明显现象;
溶液,无明显现象;
②向①所得溶液中加足量 溶液,产生白色沉淀,再加入足量
溶液,产生白色沉淀,再加入足量 ,白色沉淀部分溶解;
,白色沉淀部分溶解;
③过滤,向滤液中滴加足量 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
(3)溶液中一定存在的离子有________ 。
(4)实验②中沉淀溶解发生反应的离子方程式为_________ 。
(5)有同学认为实验③不能达到目的,原因是________ 。
Ⅰ.表为某“水培绿叶营养液的成分
| 成分 | 含量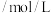 |
 | 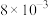 |
 |  |
 | 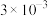 |
 | 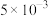 |
(1)上述各成分均属于___________(填字母)
| A.酸 | B.盐 | C.氯化物 | D.电解质 |
(2)
 该营养液中,
该营养液中, 的物质的量浓度为
的物质的量浓度为 。
。①需要用托盘天平称取
 固体的质量为
固体的质量为 。
。②在配制过程中,下列操作会使所配溶液浓度偏低的是
A.定容时,俯视刻度线 B.摇匀后液面低于刻度线,加水至刻度线
C.容量瓶中事先含有少量蒸馏水 D.未将烧杯的洗涤液转移至容量瓶中
Ⅱ.某水培営养液中可能含有
 和
和 ,为确定其成分,进行如下实验:
,为确定其成分,进行如下实验:①加入过量
 溶液,无明显现象;
溶液,无明显现象;②向①所得溶液中加足量
 溶液,产生白色沉淀,再加入足量
溶液,产生白色沉淀,再加入足量 ,白色沉淀部分溶解;
,白色沉淀部分溶解;③过滤,向滤液中滴加足量
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。(3)溶液中一定存在的离子有
(4)实验②中沉淀溶解发生反应的离子方程式为
(5)有同学认为实验③不能达到目的,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】除杂和离子的检验是中学化学的重要内容。回答下列问题:
(1)欲除去粗盐水中的 、
、 、
、 ,设计如下工艺流程(所加试剂均过量)。
,设计如下工艺流程(所加试剂均过量)。_______ (语言叙述)。
②试剂a、试剂b、试剂c依次为_______ (填字母)。
A. 溶液、
溶液、 溶液、稀盐酸 B.
溶液、稀盐酸 B. 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸
C. 溶液、NaOH溶液、稀盐酸 D.
溶液、NaOH溶液、稀盐酸 D. 溶液、NaOH溶液、稀盐酸
溶液、NaOH溶液、稀盐酸
③实验室中进行操作x需用到的玻璃仪器有烧杯、玻璃棒和_______ 。
(2)某无色透明溶液可能存在大量 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,进行如下实验:
中的一种或几种,进行如下实验:
Ⅰ.取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失;
Ⅱ.取Ⅰ的滤液加过量的NaOH溶液,出现白色沉淀。
①由操作Ⅰ确定原溶液中肯定存在的阳离子是_______ 。
②由操作Ⅱ产生沉淀的离子方程式为_______ 。
③通过以上操作肯定不存在的离子是_______ 。
(1)欲除去粗盐水中的
 、
、 、
、 ,设计如下工艺流程(所加试剂均过量)。
,设计如下工艺流程(所加试剂均过量)。
②试剂a、试剂b、试剂c依次为
A.
 溶液、
溶液、 溶液、稀盐酸 B.
溶液、稀盐酸 B. 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸C.
 溶液、NaOH溶液、稀盐酸 D.
溶液、NaOH溶液、稀盐酸 D. 溶液、NaOH溶液、稀盐酸
溶液、NaOH溶液、稀盐酸③实验室中进行操作x需用到的玻璃仪器有烧杯、玻璃棒和
(2)某无色透明溶液可能存在大量
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,进行如下实验:
中的一种或几种,进行如下实验:Ⅰ.取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失;
Ⅱ.取Ⅰ的滤液加过量的NaOH溶液,出现白色沉淀。
①由操作Ⅰ确定原溶液中肯定存在的阳离子是
②由操作Ⅱ产生沉淀的离子方程式为
③通过以上操作肯定不存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】重金属离子会污染水体。某化学兴趣小组设计如图流程除去工业废水(含有K+、Fe3+、Ag+ )中的重金属离子:

回答下列问题:
(1)操作①是_______ 。
(2)滤渣2的化学式为_______ 。
(3)检验工业废水是否含有K+的方法是_______ 。

回答下列问题:
(1)操作①是
(2)滤渣2的化学式为
(3)检验工业废水是否含有K+的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。
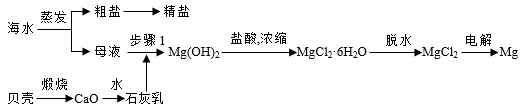
(1)步骤1中分离操作的名称是___________ ,发生反应的化学方程式是:___________
(2)粗盐中含Ca2+、Mg2+、SO 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是___________ (填写序号字母)。
a.⑥⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(3)操作步骤④调节溶液pH时,应加入___________ ,写出一个有关的化学方程式是___________ 。
(4)操作⑤溶解;⑥过滤;⑦蒸发都用到一种玻璃仪器是___________ ,简述以上⑥过滤操作中如何洗涤沉淀。___________

(1)步骤1中分离操作的名称是
(2)粗盐中含Ca2+、Mg2+、SO
 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是a.⑥⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(3)操作步骤④调节溶液pH时,应加入
(4)操作⑤溶解;⑥过滤;⑦蒸发都用到一种玻璃仪器是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】为除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):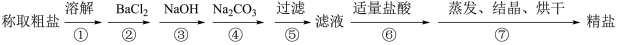
(1)判断BaCl2已过量的方法是___________ 。
(2)第④步中,相关的化学方程式是___________ 。
(3)过滤操作中,需要用到的玻璃仪器有___________ 。
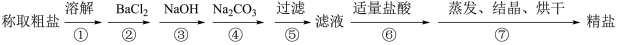
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的化学方程式是
(3)过滤操作中,需要用到的玻璃仪器有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)已知NaCl的熔点为801℃,而 (可简写为
(可简写为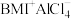 )的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么
)的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么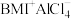 熔点远低于NaCl。
熔点远低于NaCl。_______ 。
(2)实验室中常用氨水吸收过量的 。现有一瓶500ml已经吸收
。现有一瓶500ml已经吸收 的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
a.向A中加入足量的NaOH溶液并加热,将生成的气体先通过碱石灰,再通入盛有过量无水 的装置C中,测量得反应前后装置C增重6.80g。
的装置C中,测量得反应前后装置C增重6.80g。
b.向B中加入足量稀硫酸并加热,将生成的气体先通过浓硫酸,再通入盛有过量碱石灰的装置D中,测量得反应前后装置D增重19.2g。
试回答以下问题:
①原溶液中亚硫酸铵与亚硫酸氢铵物质的量的之比是_______
②用来吸收 的氨水原物质的量浓度为
的氨水原物质的量浓度为_______
(1)已知NaCl的熔点为801℃,而
 (可简写为
(可简写为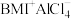 )的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么
)的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么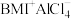 熔点远低于NaCl。
熔点远低于NaCl。(2)实验室中常用氨水吸收过量的
 。现有一瓶500ml已经吸收
。现有一瓶500ml已经吸收 的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);a.向A中加入足量的NaOH溶液并加热,将生成的气体先通过碱石灰,再通入盛有过量无水
 的装置C中,测量得反应前后装置C增重6.80g。
的装置C中,测量得反应前后装置C增重6.80g。b.向B中加入足量稀硫酸并加热,将生成的气体先通过浓硫酸,再通入盛有过量碱石灰的装置D中,测量得反应前后装置D增重19.2g。
试回答以下问题:
①原溶液中亚硫酸铵与亚硫酸氢铵物质的量的之比是
②用来吸收
 的氨水原物质的量浓度为
的氨水原物质的量浓度为
您最近一年使用:0次



