下列现象或事实、解释都正确的是
| 选项 | 现象或事实 | 解释 |
| A | 向 溶液中滴入盐酸,产生臭鸡蛋气味的气体 溶液中滴入盐酸,产生臭鸡蛋气味的气体 | 氯的非金属性比硫强 |
| B |  用于自来水的消毒和净化 用于自来水的消毒和净化 |  具有强氧化性可杀菌消毒,其还原产物 具有强氧化性可杀菌消毒,其还原产物 水解得到的胶状物能净水 水解得到的胶状物能净水 |
| C |  样品溶于水,加入硝酸酸化的 样品溶于水,加入硝酸酸化的 溶液,有白色沉淀产生 溶液,有白色沉淀产生 |  样品中含有 样品中含有 |
| D | 常温下,将铁片浸入足量的浓硫酸中,铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
| A.A | B.B | C.C | D.D |
更新时间:2021-01-06 20:13:54
|
相似题推荐
【推荐1】2023年10月4日,瑞典皇家科学院宣布将2023年诺贝尔化学奖授予美国科学家蒙吉·巴文迪、路易斯·布鲁斯和俄罗斯科学家阿列克谢·叶基莫夫,以表彰他们在发现和合成量子点方面所作出的贡献。碳量子点是一类具有显著荧光性能的零维碳纳米材料,直径低于10nm。碳量子点通常是由无定型和晶态的碳核组成,在碳核表面含有多个不同的含氧官能团,例如羟基、羧基等。下列说法错误的是
| A.由碳量子点形成的溶液具有丁达尔效应 |
| B.碳量子点直径比碳原子大 |
| C.碳量子点在水中具有优异的溶解性 |
| D.碳量子点与金刚石属于同素异形体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是( )
| A.由同种元素组成的物质一定是纯净物 |
| B.氨水导电,所以氨水是电解质 |
| C.能电离出H+的化合物都是酸 |
| D.在豆浆中加入硫酸钙制豆腐,是利用了胶体的聚沉性质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列溶液中各组离子一定能够大量共存的是
A.澄清透明的溶液:K+、H+、 、 、 |
B.0.lmol·L-1NaAlO2溶液:K+、 、Al3+、 、Al3+、 |
C.0.1 mol·L−1 FeCl3溶液: 、H+、I-、 、H+、I-、 |
D.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、 、Cl- 、Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.用石灰石—石膏法对燃煤烟气进行脱硫,同时可得到石膏 |
| B.浓硝酸与铁在常温下能反应,但可用铁质容器贮运浓硝酸 |
| C.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用 |
| D.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验的现象及对应的结论均正确的是
| 实验操作 | 实验现象 | 结论 | |
| A | 将铜片与稀硝酸混合 | 试管口有红棕色气体 | 铜片与稀硝酸反应产生NO2 |
| B | Ba(OH)2·8H2O与NH4Cl固体混合搅拌 | 有刺激性气味的气体产生 | 该反应是吸热反应 |
| C | Al和浓硝酸在常温下混合 | Al片完全溶解 | 常温下Al被浓硝酸完全溶解 |
| D | 紫色石蕊溶液中分别加入浓硝酸和稀硝酸中 | 浓硝酸中先变红后褪色,稀硝酸中只变红不褪色 | 浓硝酸氧化性比稀硝酸强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列对浓硫酸的叙述中,正确的是
| A.常温下不能用铁、铝容器盛放浓硫酸,因为铁、铝是活泼金属 |
| B.浓硫酸和碳单质加热反应,表现出强氧化性 |
| C.浓硫酸具有吸水性,可以使蔗糖脱水炭化 |
| D.滴加浓硫酸使胆矾由蓝色晶体变为无色粉末,属于物理变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用如图所示装置检验乙烯时不需要除杂的是( )
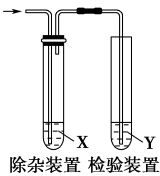
| 选项 | 乙烯的制备 | 试剂X | 试剂Y |
| A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
| C | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
| D | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | 溴水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】原子核的人工转变是利用 粒子(即氦核
粒子(即氦核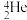 )撞击原子核,使原子核转变为另一种原子核的过程。1919年,卢瑟福利用
)撞击原子核,使原子核转变为另一种原子核的过程。1919年,卢瑟福利用 粒子轰击短周期非金属原子
粒子轰击短周期非金属原子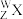 ,发现了质子,使人类对原子核的认识更进一步,其核反应原理为
,发现了质子,使人类对原子核的认识更进一步,其核反应原理为 ,其中元素X的最高价氧化物对应的水化物能与其气态氢化物反应生成盐,下列说法正确的是
,其中元素X的最高价氧化物对应的水化物能与其气态氢化物反应生成盐,下列说法正确的是
 粒子(即氦核
粒子(即氦核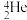 )撞击原子核,使原子核转变为另一种原子核的过程。1919年,卢瑟福利用
)撞击原子核,使原子核转变为另一种原子核的过程。1919年,卢瑟福利用 粒子轰击短周期非金属原子
粒子轰击短周期非金属原子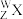 ,发现了质子,使人类对原子核的认识更进一步,其核反应原理为
,发现了质子,使人类对原子核的认识更进一步,其核反应原理为 ,其中元素X的最高价氧化物对应的水化物能与其气态氢化物反应生成盐,下列说法正确的是
,其中元素X的最高价氧化物对应的水化物能与其气态氢化物反应生成盐,下列说法正确的是| A.X、Y均可形成既含极性键又含非极性键的化合物 |
B.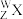 的中子数为8 的中子数为8 |
| C.原子半径:X<Y |
| D.X的简单气态氢化物的热稳定性比Y的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据元素周期表和元素周期律,判断下列叙述不 正确的是( )
| A.气态氢化物的稳定性:HCl>HI |
| B.氢元素与其他元素可形成共价化合物或离子化合物 |
C.如图所示实验可证明元素的非金属性:Cl>C>Si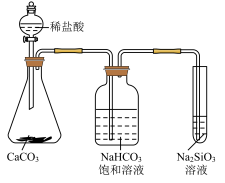 |
D.用中文“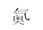 ” ”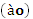 命名的第118号元素在周期表中位于第七周期 命名的第118号元素在周期表中位于第七周期 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】短周期元素X、Y、Z、W在元素周期表中的位置如下表所示,它们的最外层电子数之和为23。则下列判断正确的是
| X | Y | ||
| Z | W |
| A.简单气态氢化物稳定性:X>Y |
| B.四种元素中原子半径最大的是W |
| C.Z元素的最高价氧化物对应水化物的化学式为H2ZO3 |
| D.XW4分子中每个原子最外电子层都具有8电子稳定结构 |
您最近一年使用:0次

 浊液中加入浓
浊液中加入浓 溶液,沉淀由淡黄色逐渐变为白色
溶液,沉淀由淡黄色逐渐变为白色
 ,加热几分钟,冷却后加入过量的氢氧化钠溶液,然后滴加碘水,溶液未变蓝
,加热几分钟,冷却后加入过量的氢氧化钠溶液,然后滴加碘水,溶液未变蓝


