下列反应的离子方程式正确的是
A.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸: 3Fe2++4H++NO =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
B.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
C.NH4HCO3溶液与足量的NaOH溶液混合加热:NH +OH- +OH- NH3↑+H2O NH3↑+H2O |
D.等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合:Ca2++HCO +OH- =CaCO3↓+H2O +OH- =CaCO3↓+H2O |
更新时间:2021-01-07 14:46:15
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | NH | 少量Ba(OH)2溶液 | 2NH +SO +SO +Ba2++2OH-=2NH3·H2O+BaSO4↓ +Ba2++2OH-=2NH3·H2O+BaSO4↓ |
B | Mg2+、Cl-、HCO | 过量NaOH溶液 | Mg2++2HCO +4OH-=2H2O+Mg(OH)2↓+2CO +4OH-=2H2O+Mg(OH)2↓+2CO |
C | K+、CO | 通入少量CO2 | 2OH-+CO2=CO +H2O +H2O |
D | Fe2+、Cl-、HSO | NaHSO4溶液 | SO +2H+=SO2↑+H2O +2H+=SO2↑+H2O |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列化学反应对应的离子方程式表示正确的是
A.KAl(SO4)2中滴加Ba(OH)2使 恰好完全沉淀:2Al3++3 恰好完全沉淀:2Al3++3 +3Ba2++6OH-=2Al(OH)3↓ +3BaSO4↓ +3Ba2++6OH-=2Al(OH)3↓ +3BaSO4↓ |
B.NH4HCO3溶于过量的NaOH溶液中: |
| C.向Ca(ClO)2溶液中通入少量SO2 : Ca2++ClO-+H2O+SO2=Cl-+CaSO4↓+2H+ |
D. 溶液与等物质的量的 溶液与等物质的量的 反应: 反应: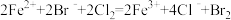 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】铁与不同浓度硝酸反应时各种还原产物的相对含量与硝酸溶液浓度的关系如图所示,下列说法错误的是


| A.硝酸的浓度越小,其还原产物氮的价态越低的成分越多 |
| B.硝酸与铁反应往往同时生成多种还原产物 |
| C.当硝酸浓度为9.75mol·L-1时,氧化剂与还原剂的物质的量之比可为15∶13 |
| D.铁能与大于12.2 mol·L-1HNO3溶液反应说明不存在“钝化”现象 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列有关实验的说法正确的是
| A.测定中和反应反应热实验中,为了充分反应,应将NaOH溶液缓缓倒入盐酸中 |
| B.配制FeCl3溶液时,将FeCl3晶体溶解在较浓的盐酸中,再加蒸馏水稀释到所需浓度 |
| C.用盐酸滴定NaOH溶液时,左手控制酸式滴定管活塞,右手振荡锥形瓶,眼睛注视滴定管内液面 |
| D.检验Fe(NOs)2晶体是否变质时,将Fe(NO3)2样品溶于稀H2SO4后,再滴加KSCN溶液 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某100mL无色溶液中可能含有 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出),下列说法不正确的是
中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出),下列说法不正确的是

 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出),下列说法不正确的是
中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出),下列说法不正确的是
A.原溶液一定存在 和 和 |
B.原溶液中 |
C.原溶液一定不存在 ,一定存在 ,一定存在 |
D.原溶液中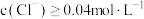 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】工业接触法制硫酸的吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到58.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果如下表;
试计算:该铵盐中氮元素的质量分数是
部分测定结果如下表;
| 不同质量铵盐/g | 25.00 | 50.00 | 75.00 | 100.00 |
| 浓硫酸增加的质量/g | 相同 | 相同 | 1.70 | 0 |
试计算:该铵盐中氮元素的质量分数是
| A.12.15% | B.21.50% | C.14.56% | D.无法确定 |
您最近半年使用:0次

 +H2O
+H2O






