向200 mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法正确的是


| A.a点时溶液中的阳离子仅为Cu2+和Fe2+ |
| B.b点时溶液中发生的反应为2Fe+3Cu2+=Cu+2Fe3+ |
| C.c点时溶液中溶质的物质的量浓度为0.2mol·L-1 |
| D.原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为1:2 |
更新时间:2021-03-04 23:34:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向10 mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。下列说法错误的是


| A.a点时溶液中金属阳离子有Fe3+、Cu2+和Fe2+ |
| B.b点时溶液中的离子反应有两种 |
| C.原溶液中n(Fe3+):n(Cu2+)=1:1 |
| D.原溶液中Fe2(SO4)3的物质的量浓度为1 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1 mol的混合溶液中加入0.1 molFe,充分搅拌后Fe溶解,溶液中不存在Fe3+,同时析出0.1 mol Ag。下列结论错误的是
| A.氧化性:Zn2+>Cu2+>Fe3+>Ag+ | B.Fe3+的氧化性大于Cu2+ |
| C.溶液中Cu2+与Fe2+的物质的量比为1∶2 | D.1 mol Fe可还原2 mol Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】为将含FeCl3、FeCl2、CuCl2的废液中的Cu2+还原回收,某同学在含有ag铁粉的容器中加入废液,探究了加入废液体积与完全反应后体系中固体质量的关系,部分实验数据如下表所示。已知:废液中c(Cu2+)=0.7mol·L-1;废液体积大于0.5L,充分反应后才能检测出Cu2+。
下列说法不正确 的是
| 废液体积/L | ≤0.5 | 1 | 2 | 3 | ≥4 |
| 固体质量/g | a | 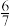 a a | 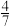 a a | 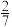 a a | 0 |
| A.当铁粉与0.25L废液反应完全后,固体成分为Fe与Cu |
| B.废液中c(Fe3+)=0.2mol·L-1 |
| C.要将1L废液中的Cu2+全部还原,则至少需要铁粉44.8g |
| D.当铁粉与1L废液反应完全后,再加入废液时发生的离子反应为:Fe+2Fe3+=3Fe2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某同学进行下列实验:在加热条件下将24g CuO、Fe2O3的混合物与充足的CO完全反应,并将反应后的气体全部通入到足量的澄清石灰水中,得到白色沉淀40g。下列有关叙述中不正确的是
| A.原混合物中CuO与Fe2O3物质的量比为1:1 |
| B.反应后所得CO2的物质的量为0.4mol |
| C.实验过程中需要的CO 质量为11.2g |
| D.原混合物中CuO与Fe2O3的质量比为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是
| A.若无固体剩余,则溶液中一定有Fe3+ |
| B.若有固体存在,则溶液中一定有Fe2+ |
| C.若溶液中有Cu2+,则一定没有固体析出 |
| D.若溶液中有Fe2+,则一定有Cu析出 |
您最近一年使用:0次

 和
和 的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量关系如图所示。忽略反应过程中溶液体积的变化,下列说法正确的是
的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量关系如图所示。忽略反应过程中溶液体积的变化,下列说法正确的是

 、
、 和
和
 的物质的量浓度为
的物质的量浓度为


