已知溴原子的原子结构示意图为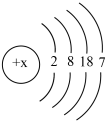
(1)溴元素在元素周期表中位置是___________ 。
(2)溴元素的最低化合价为___________ ,溴元素的最高价氧化物的水化物的化学式为___________ 。
(3)溴元素的非金属性比氯元素的非金属性___________ (选填“强”或“弱”)。
(4)向 溶液中滴加少量溴水,反应的离子方程式为
溶液中滴加少量溴水,反应的离子方程式为___________ 。继续加入少量苯,充分振荡,静置后观察到实验现象为___________ 。

(1)溴元素在元素周期表中位置是
(2)溴元素的最低化合价为
(3)溴元素的非金属性比氯元素的非金属性
(4)向
 溶液中滴加少量溴水,反应的离子方程式为
溶液中滴加少量溴水,反应的离子方程式为
20-21高一上·江苏苏州·阶段练习 查看更多[2]
更新时间:2021-03-07 20:50:55
|
【知识点】 同主族元素性质递变规律理解及应用解读
相似题推荐
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为_______ 。
(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。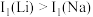 ,原因是
,原因是_______ 。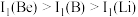 ,原因是
,原因是_______ 。
(1)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。
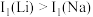 ,原因是
,原因是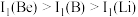 ,原因是
,原因是 | ||
 520 |  900 | B 801 |
 496 |  738 |  578 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期律反映了元素性质随原子序数递增的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是___________ (填碱的化学式)。
(2)碱金属元素中,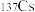 和
和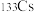 之间的关系是互为
之间的关系是互为___________ ,金属钾的氧化物有多种,写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性___________ HI的稳定性(填“大于”或“小于”),AgAt___________ 溶于水(填“易”或“难”)。
(4)某实验小组欲通过化学实验证明元素的非金属性:Br>S。
供选择的试剂:氯水、溴水、溴化钠溶液、新制 溶液、四氯化碳、酚酞。
溶液、四氯化碳、酚酞。
①完成该实验需要选用的最合适的试剂为___________ 。
②简述实验操作和实验现象:___________ 。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是
(2)碱金属元素中,
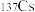 和
和 之间的关系是互为
之间的关系是互为 与
与 反应的化学方程式:
反应的化学方程式:(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性
(4)某实验小组欲通过化学实验证明元素的非金属性:Br>S。
供选择的试剂:氯水、溴水、溴化钠溶液、新制
 溶液、四氯化碳、酚酞。
溶液、四氯化碳、酚酞。①完成该实验需要选用的最合适的试剂为
②简述实验操作和实验现象:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。回答下列问题
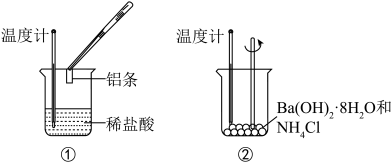
(1)装置①中反应物的总能量比生成物的总能量________ (填标号)。
a.高 b.低 c.相等
(2)装置②中反应后溶液的温度__________ (填标号)。
a.升高 b.降低 c.不变
(3)已知断裂1mol共价键需要吸收的能量分别为 H —H :436kJ,I —I :151kJ,H— I :299kJ。则反应 H2+I2 = 2HI的能量变化为______ (填标号)。
a.无能量变化 b.吸热 c.放热
(4)碱金属单质在空气中燃烧的产物与碱金属的活动性有关。锂单质在空气中燃烧得到的产物的化学式为__________ 。

(1)装置①中反应物的总能量比生成物的总能量
a.高 b.低 c.相等
(2)装置②中反应后溶液的温度
a.升高 b.降低 c.不变
(3)已知断裂1mol共价键需要吸收的能量分别为 H —H :436kJ,I —I :151kJ,H— I :299kJ。则反应 H2+I2 = 2HI的能量变化为
a.无能量变化 b.吸热 c.放热
(4)碱金属单质在空气中燃烧的产物与碱金属的活动性有关。锂单质在空气中燃烧得到的产物的化学式为
您最近一年使用:0次



