(1)①实验室制备氨气,下列方法中适宜选用的是_______ 。
A.固态氯化铵加热分解
B.氢氧化钠溶液中滴加稀氨水
C.氯化铵溶液与氢氧化钠溶液共热
D.固态氯化铵与氢氧化钙混合加热
②检验氨气是否已经收集满的方法是_______ 。
③为了得到干燥的NH3,用_______ 干燥剂。
A.碱石灰 B.浓H2SO4 C.无水CaCl2 D.P2O5
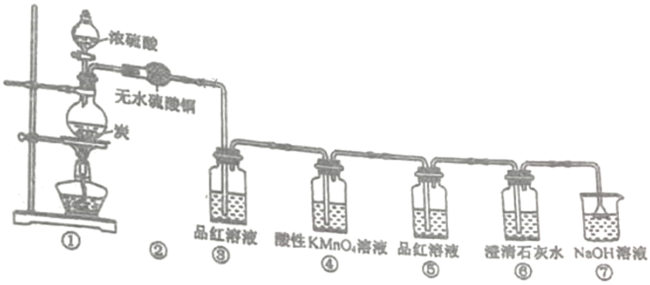
(2)为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置。
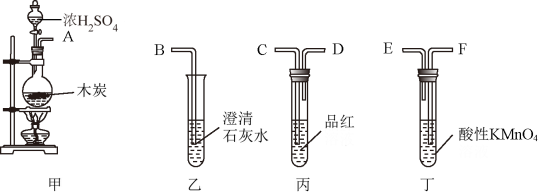
①如按气流由左向右流向,连接上述装置(各装置只用一次)的正确顺序是(填各接口字母):A→____ 。
②什么样的实验现象才表明已检验出CO2?_______ 。
③写出甲中反应的化学方程式_______ 。
A.固态氯化铵加热分解
B.氢氧化钠溶液中滴加稀氨水
C.氯化铵溶液与氢氧化钠溶液共热
D.固态氯化铵与氢氧化钙混合加热
②检验氨气是否已经收集满的方法是
③为了得到干燥的NH3,用
A.碱石灰 B.浓H2SO4 C.无水CaCl2 D.P2O5
(2)为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置。

①如按气流由左向右流向,连接上述装置(各装置只用一次)的正确顺序是(填各接口字母):A→
②什么样的实验现象才表明已检验出CO2?
③写出甲中反应的化学方程式
更新时间:2021-03-15 18:42:57
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
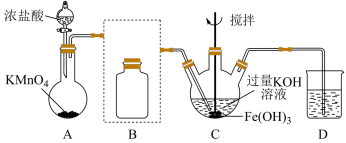
【推荐1】某课外小组利用如图装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置, C为纯净、干燥的氯气与氨气反应的装置。
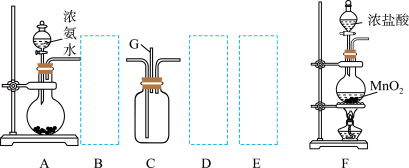
请回答下列问题:
(1)装置A中的烧瓶内固体不宜选用_________ (选填以下选项的代号,多选或者错选均不给分)。
A. 碱石灰 B. 生石灰 C. 二氧化硅 D. 烧碱
(2)虚线框内应添加必要的除杂装置, 请从图中的备选装置中选择。
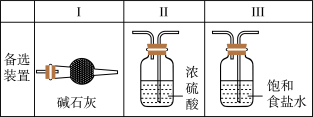
将编号填入下列空格:B_________ 、D_________ 、E_________ 。
(3)氯气和氨气在常温下相混合就会反应生成氯化铵和氮气,该反应的化学方程式为:________ 。
(4)若从装置C和G处逸出的尾气只含有N2和少量Cl2,应如何处理才能不污染环境?________ 。

请回答下列问题:
(1)装置A中的烧瓶内固体不宜选用
A. 碱石灰 B. 生石灰 C. 二氧化硅 D. 烧碱
(2)虚线框内应添加必要的除杂装置, 请从图中的备选装置中选择。

将编号填入下列空格:B
(3)氯气和氨气在常温下相混合就会反应生成氯化铵和氮气,该反应的化学方程式为:
(4)若从装置C和G处逸出的尾气只含有N2和少量Cl2,应如何处理才能不污染环境?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】利用元素的化合价推测物质的性质是化学研究的重要方法。位于元素周期表中第二周期的某元素,其常见化合价与对应物质类别的部分关系如图所示。
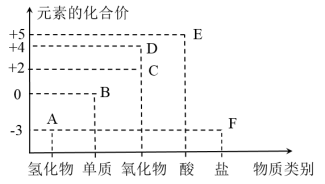
(1)该元素是__ ,它位于元素周期表中第二周期、第__ 族。
(2)根据元素的化合价,从氧化还原角度分析,单质B具有的性质是__ 。
(3)B、C、D、E4种物质中,属于有毒气体的是__ (填化学式),欲吸收有毒气体,可选用氧气和__ (填序号)。
a.氢氧化钠溶液 b.稀硫酸 c.蒸馏水
(4)组装如图装置制取并收集一瓶干燥的A。

①A的化学式是___ 。
②实验室制取A的化学方程式是___ 。
③各装置的接口顺序是a→__ (填序号)。
④X中的药品是__ ,其作用是___ 。
⑤检验是否收集满A的方法是__ 。

(1)该元素是
(2)根据元素的化合价,从氧化还原角度分析,单质B具有的性质是
(3)B、C、D、E4种物质中,属于有毒气体的是
a.氢氧化钠溶液 b.稀硫酸 c.蒸馏水
(4)组装如图装置制取并收集一瓶干燥的A。

①A的化学式是
②实验室制取A的化学方程式是
③各装置的接口顺序是a→
④X中的药品是
⑤检验是否收集满A的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】合成氨可以融入工业制硝酸形成联合制硝酸法,流程如图所示。

回答下列问题:
(1)气体X为_______ (填化学式),“液化分离”是利用空气中各组分_______ 不同分离出 与气体X。
与气体X。
(2)“合成氨”是在高温高压和催化剂条件下进行的,该反应的化学方程式为_______ ,为加快反应速率,还可以采取的措施有_______ 。
(3)“催化氧化”反应的化学方程式为_______ 。
(4)“吸收”过程的总反应可以表示为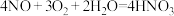 ,该反应属于
,该反应属于_______ (填基本反应类型)反应,吸收过程采用“喷淋法”使气液逆流的目的是_______ 。

回答下列问题:
(1)气体X为
 与气体X。
与气体X。(2)“合成氨”是在高温高压和催化剂条件下进行的,该反应的化学方程式为
(3)“催化氧化”反应的化学方程式为
(4)“吸收”过程的总反应可以表示为
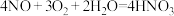 ,该反应属于
,该反应属于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
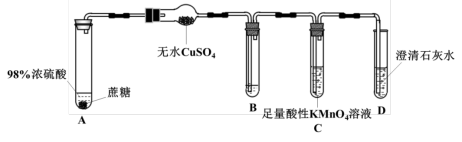
【推荐1】实验室中利用下图装置进行浓硫酸与蔗糖的微型化反应,并对所有产物进行检验。
请回答:
(1)装置A中的现象为产生大量气体,生成的黑色物质体积膨胀,呈疏松多孔状。体现出浓硫酸具有___________ (填性质),写出产生气体的反应的化学方程式___________ ;
(2)装置B中的溶液为品红溶液,作用是___________ ;
(3)装置C的作用是___________ ,现象为___________ ;
(4)装置D中反应的离子方程式___________ 。

请回答:
(1)装置A中的现象为产生大量气体,生成的黑色物质体积膨胀,呈疏松多孔状。体现出浓硫酸具有
(2)装置B中的溶液为品红溶液,作用是
(3)装置C的作用是
(4)装置D中反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】I.用下图所示各装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应所产生的各种产物。这些装置的连接顺序(按产物气体从左至右的流向)是__________________ 。




(1)实验时可观察到上图装置①中A瓶的溶液褪色,C瓶的溶液不褪色,A瓶溶液的作用是___________ 。
(2)装置②中实验现象是白色固体变蓝色,所加的固体药品是____________ (填名称)。
(3)装置③中所盛溶液是澄清石灰水,可验证的产物是________________ (填化学式)。
II.实验室可用如下装置(略去部分夹持仪器)制取SO2并验证其性质:

(1)盛装70%H2SO4溶液的仪器名称为__________________________ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择_________ (填字母)
a.蒸馏水 b.饱和Na2CO3溶液 c.饱和NaOH溶液 d.饱和NaHSO3溶液
(3)装置E的作用是_________________ 。




(1)实验时可观察到上图装置①中A瓶的溶液褪色,C瓶的溶液不褪色,A瓶溶液的作用是
(2)装置②中实验现象是白色固体变蓝色,所加的固体药品是
(3)装置③中所盛溶液是澄清石灰水,可验证的产物是
II.实验室可用如下装置(略去部分夹持仪器)制取SO2并验证其性质:

(1)盛装70%H2SO4溶液的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和Na2CO3溶液 c.饱和NaOH溶液 d.饱和NaHSO3溶液
(3)装置E的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验小组制备高铁酸钾( )并探究其性质。
)并探究其性质。
资料:
① 为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降与水反应放出氯气。
为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降与水反应放出氯气。
② 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③ 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。
胶体,可除去水中细微的悬浮物,有净水作用。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)A中发生反应的化学方程式为:___________ ,实验室还可以用二氧化锰和浓盐酸制备氯气,请写出其反应的离子方程式:___________ ,当 参与反应时,被氧化的
参与反应时,被氧化的 的质量为
的质量为___________ ,生成的 在标准状况下的体积约为
在标准状况下的体积约为___________ 。
(3)装置B是为了除去 中混有的
中混有的 杂质,将除杂装置B补充完整并标明所用试剂
杂质,将除杂装置B补充完整并标明所用试剂___________ 。
(4)D中可选用的试剂是___________。
(5)C中通 制得
制得 的化学方程式
的化学方程式___________ ,同时还发生了另一个反应的离子方程式是___________ 。
(6)下列关于 的说法中,正确的是
的说法中,正确的是___________ 。
A.是强氧化性的盐 B.固体保存需要防潮 C.其消毒和净化水的原理相同
 )并探究其性质。
)并探究其性质。资料:
①
 为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降与水反应放出氯气。
为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降与水反应放出氯气。②
 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。③
 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。
胶体,可除去水中细微的悬浮物,有净水作用。
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)A中发生反应的化学方程式为:
 参与反应时,被氧化的
参与反应时,被氧化的 的质量为
的质量为 在标准状况下的体积约为
在标准状况下的体积约为(3)装置B是为了除去
 中混有的
中混有的 杂质,将除杂装置B补充完整并标明所用试剂
杂质,将除杂装置B补充完整并标明所用试剂(4)D中可选用的试剂是___________。
| A.KOH溶液 | B.NaCl溶液 | C.稀硫酸 | D.NaI溶液 |
 制得
制得 的化学方程式
的化学方程式(6)下列关于
 的说法中,正确的是
的说法中,正确的是A.是强氧化性的盐 B.固体保存需要防潮 C.其消毒和净化水的原理相同
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某校化学研究性小组,利用下列提供的实验装置和试剂对某种燃煤所含元素进行定性和定量检测,试回答:
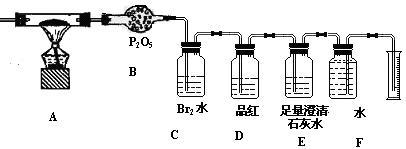
(1)将燃煤充分燃烧,产生气体经化学分析主要含有CO2、H2O、SO2、N2四种气体
(2)称取该燃煤样品Wg,通入纯氧使其充分燃烧,检测该燃煤中所含上述元素的质量分数。利用下列装置进行实验:
①指出上述装置中D、E的作用
D____________ , E_____________
为了测得相应数据,进行如下操作(忽略CO2在C、D中的溶解)
a.实验前用托盘天平称得B、C、D、E的质量分别为W1、W2、W3、W4
b.实验完成后称得B、C、D、E的质量分别为m1、m2、m3、m4
c.通过正确实验操作,用F装置测得收集气体体积为V L
②为了准确测量F中收集到的气体体积,正确的实验操作是___________
③测定燃煤中的硫的质量分数,当观察到溴水不完全褪色,品红不褪色时,燃煤中含硫元素的质量分数的表达式为___________________ 。当观察到___________
现象时,无法测定燃煤中硫元素的质量分数。

(1)将燃煤充分燃烧,产生气体经化学分析主要含有CO2、H2O、SO2、N2四种气体
(2)称取该燃煤样品Wg,通入纯氧使其充分燃烧,检测该燃煤中所含上述元素的质量分数。利用下列装置进行实验:
①指出上述装置中D、E的作用
D
为了测得相应数据,进行如下操作(忽略CO2在C、D中的溶解)
a.实验前用托盘天平称得B、C、D、E的质量分别为W1、W2、W3、W4
b.实验完成后称得B、C、D、E的质量分别为m1、m2、m3、m4
c.通过正确实验操作,用F装置测得收集气体体积为V L
②为了准确测量F中收集到的气体体积,正确的实验操作是
③测定燃煤中的硫的质量分数,当观察到溴水不完全褪色,品红不褪色时,燃煤中含硫元素的质量分数的表达式为
现象时,无法测定燃煤中硫元素的质量分数。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯化亚铁是重要的还原剂,常用于检测硒、生产聚合氯化铝铁絮凝剂。制备FeCl2的方法有多种。请回答下列问题:
Ⅰ.结晶法制取FeCl2
在一定浓度的盐酸中,逐渐加入过量的铁屑,充分反应后,蒸发至出现晶膜,____ ,______ ,固液分离,洗涤,快速干燥制得。
Ⅱ.氯苯还原无水FeC13制取FeC12
无水FeCl3与氯苯反应的化学方程式为:2FeCl3+C6H5Cl 2FeCl2+C6H4Cl2+HCl↑
2FeCl2+C6H4Cl2+HCl↑
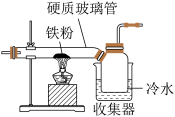
(1)如图是用干燥的C12和铁粉制取无水FeC13的装置。硬质玻璃管和收集器用大口管连接的原因是________ 。
(2)利用如图装置制备无水FeC12,并检测FeC13的转化率。已知相关物质的部分性质如下:
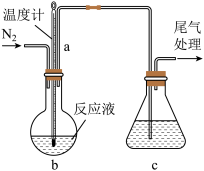
将162.5 g无水氯化铁和200 g氯苯加入到圆底烧瓶中,在锥形瓶中加入200 g滴有酚酞的9.5%的NaOH溶液。先通入N2一段时间,再加热,控制温度在132 ℃左右发生反应。实验完成后冷却,分离提纯得到粗产品。
①先通入N2的目的是_______ ;导管a的作用是______ 。
②当锥形瓶内溶液颜色由红色变为无色时,停止加热,则氯化铁转化率理论上达到或超过______ %。
③实验结束后,回收过量氯苯的操作名称为______ 。
④指出装置c可能存在的缺点______ 。
Ⅰ.结晶法制取FeCl2
在一定浓度的盐酸中,逐渐加入过量的铁屑,充分反应后,蒸发至出现晶膜,
Ⅱ.氯苯还原无水FeC13制取FeC12
无水FeCl3与氯苯反应的化学方程式为:2FeCl3+C6H5Cl
 2FeCl2+C6H4Cl2+HCl↑
2FeCl2+C6H4Cl2+HCl↑(1)如图是用干燥的C12和铁粉制取无水FeC13的装置。硬质玻璃管和收集器用大口管连接的原因是

(2)利用如图装置制备无水FeC12,并检测FeC13的转化率。已知相关物质的部分性质如下:

| C6H5C1(氯苯) | C6H4C12 | FeC13 | FeC12 | |
| 相对分子质量 | 112.5 | 147 | 162.5 | 127 |
| 熔点/℃ | -45 | 53 | 306 | 670~674 |
| 沸点/℃ | 132 | 173 | 315 | 1023 |
将162.5 g无水氯化铁和200 g氯苯加入到圆底烧瓶中,在锥形瓶中加入200 g滴有酚酞的9.5%的NaOH溶液。先通入N2一段时间,再加热,控制温度在132 ℃左右发生反应。实验完成后冷却,分离提纯得到粗产品。
①先通入N2的目的是
②当锥形瓶内溶液颜色由红色变为无色时,停止加热,则氯化铁转化率理论上达到或超过
③实验结束后,回收过量氯苯的操作名称为
④指出装置c可能存在的缺点
您最近一年使用:0次