A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了54克。常温下各烧杯中溶液的pH与电解时间t的关系图如下。据此回答下列问题:
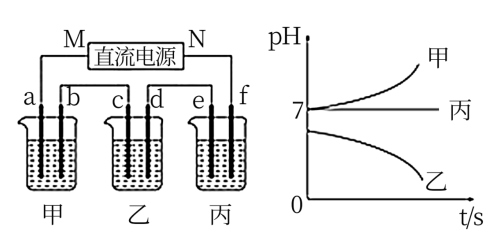
(1)甲中电解质为_______ (填写化学式);
(2)要使丙恢复到原来的状态,应加入_______ g _______ (填写化学式)。
| 阳离子 | Ag+、Na+ |
| 阴离子 |  、 、 、Cl- 、Cl- |

(1)甲中电解质为
(2)要使丙恢复到原来的状态,应加入
更新时间:2021-03-16 22:51:20
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是_______________________ 。
(2)铝与氢氧化钾溶液反应的离子方程式是______________ 。
(3)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。

①该电解槽的阳极反应式是______________________ 。
②通电开始后,阴极附近溶液pH会增大,请简述原因______________________ 。
③除去杂质后的氢氧化钾溶液从液体出口___________ (填写“A”或“B”)导出。
(1)工业冶炼铝的化学方程式是
(2)铝与氢氧化钾溶液反应的离子方程式是
(3)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。

①该电解槽的阳极反应式是
②通电开始后,阴极附近溶液pH会增大,请简述原因
③除去杂质后的氢氧化钾溶液从液体出口
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。
(1)如图是一个电化学过程示意图。

①铂片上发生的电极反应式是___________________________ 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气_____ L(假设空气中氧气体积含量为20%)。
③若把铜电极改换成铂电极电解1L0.5mol·L-1CuSO4溶液,则和电源正极相连的电极上的电极反应式为________ ,若此电极产生4.48L(标准状况)气体,则所得溶液的氢离子浓度:c(H+)=________ (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入________ (填字母)。
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
(2)肼—空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时,负极的电极反应式是________________________
(1)如图是一个电化学过程示意图。

①铂片上发生的电极反应式是
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气
③若把铜电极改换成铂电极电解1L0.5mol·L-1CuSO4溶液,则和电源正极相连的电极上的电极反应式为
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
(2)肼—空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时,负极的电极反应式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】N2O5是一种新型硝化剂,其性质和制备备受人们的关注。
(1)一定温度下,在2L恒容密闭的容器中充入2.0molN2O5发生反应:2N2O5(g) 4NO2(g)+O2(g)。在三种不同的条件下进行实验,N2O5的浓度随时间的变化如图所示。
4NO2(g)+O2(g)。在三种不同的条件下进行实验,N2O5的浓度随时间的变化如图所示。

①已知:2N2O5(g)===2N2O4(g)+O2(g) △H1=-4.4kJ/mol
2NO2(g)===N2O4(g) △H2=-55.3 kJ/mol
则反应2N2O5(g)===4NO2(g)+O2(g)的△H=________ 。
②下列不能说明该反应已达平衡状态的是___ (填序号)。
A.v正(N2O5)=2v逆(O2)
B.混合气体密度不变
C.混合体平均摩尔质量
D.NO2的体积分数不变
③该反应自发进行的条件是____ (填“高温”或“低温”),实验Ⅲ中:a点v逆(O2)____ (填“<”或“>”)b点v逆(O2)。
④实验Ⅱ从反应开始至平衡时,v(O2)=____ mol/(L·min)。
⑤列式并计算该反应在800℃时的平衡常数K=_______ 。
(2)1840年Devil用干燥的氯气通过干燥的硝酸银,反应得到N2O5。该反应的氧化产物是一种气体,该反应的化学方程式为_______ 。
(3)N2O5也可采用“电解法”制备,装置如图所示。

则N2O5在电解池的____ (填“阴极”或“阳极”)室生成,其电极反应式为_____ 。
(1)一定温度下,在2L恒容密闭的容器中充入2.0molN2O5发生反应:2N2O5(g)
 4NO2(g)+O2(g)。在三种不同的条件下进行实验,N2O5的浓度随时间的变化如图所示。
4NO2(g)+O2(g)。在三种不同的条件下进行实验,N2O5的浓度随时间的变化如图所示。
①已知:2N2O5(g)===2N2O4(g)+O2(g) △H1=-4.4kJ/mol
2NO2(g)===N2O4(g) △H2=-55.3 kJ/mol
则反应2N2O5(g)===4NO2(g)+O2(g)的△H=
②下列不能说明该反应已达平衡状态的是
A.v正(N2O5)=2v逆(O2)
B.混合气体密度不变
C.混合体平均摩尔质量
D.NO2的体积分数不变
③该反应自发进行的条件是
④实验Ⅱ从反应开始至平衡时,v(O2)=
⑤列式并计算该反应在800℃时的平衡常数K=
(2)1840年Devil用干燥的氯气通过干燥的硝酸银,反应得到N2O5。该反应的氧化产物是一种气体,该反应的化学方程式为
(3)N2O5也可采用“电解法”制备,装置如图所示。

则N2O5在电解池的
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】下图为人工肾脏采用间接电化学方法除去代谢产物中的尿素【CO(NH2)2】的原理。请回答下列问题:

(1)电源的负极为____ (选填“A”或“B”)。
(2)阳极室中发生的反应依次为________________ 、_________________________ 。
(3)电解结束后,阴极室溶液的pH与电解前相比将___ (选填“降低”、“增大”或“不变”)。
(4)若两极共收集到标准状况下气体6.72 L,则除去的尿素为__ g(忽略气体的溶解)。

(1)电源的负极为
(2)阳极室中发生的反应依次为
(3)电解结束后,阴极室溶液的pH与电解前相比将
(4)若两极共收集到标准状况下气体6.72 L,则除去的尿素为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、 时,
时,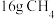 完全燃烧生成液态水时放出的热量是
完全燃烧生成液态水时放出的热量是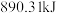 ,则
,则 燃烧的热化学方程式为
燃烧的热化学方程式为_______ 。
(2)已知:
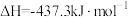

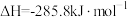
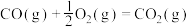
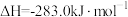
则煤气化反应 的焓变
的焓变
_______  。
。
(3)如图所示组成闭合回路,其中,甲装置中 为负极,
为负极, 和
和 的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出,
的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出, 溶液的体积为
溶液的体积为 。
。

①装置中气体A为_______ (填“ ”或“
”或“ 和
和 ”),d极上的电极反应式为
”),d极上的电极反应式为_______ 。
②乙装置中a极上的电极反应式为_______ 。若在a极产生 (标准状况)气体,则甲装置中消耗
(标准状况)气体,则甲装置中消耗
_______ mL(标准状况),乙装置中所得溶液的
_______ (忽略电解前后溶液体积变化)。
③如果乙中电极不变,将溶液换成饱和 溶液,当阴极上有
溶液,当阴极上有 气体生成时,同时有
气体生成时,同时有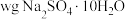 晶体析出,若温度不变,剩余溶液中溶质的质量分数应为
晶体析出,若温度不变,剩余溶液中溶质的质量分数应为_______ (用含w、a的表达式表示,不必化简)。
(1)在25℃、
 时,
时,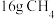 完全燃烧生成液态水时放出的热量是
完全燃烧生成液态水时放出的热量是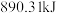 ,则
,则 燃烧的热化学方程式为
燃烧的热化学方程式为(2)已知:

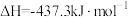

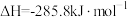
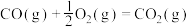
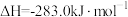
则煤气化反应
 的焓变
的焓变
 。
。(3)如图所示组成闭合回路,其中,甲装置中
 为负极,
为负极, 和
和 的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出,
的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出, 溶液的体积为
溶液的体积为 。
。
①装置中气体A为
 ”或“
”或“ 和
和 ”),d极上的电极反应式为
”),d极上的电极反应式为②乙装置中a极上的电极反应式为
 (标准状况)气体,则甲装置中消耗
(标准状况)气体,则甲装置中消耗

③如果乙中电极不变,将溶液换成饱和
 溶液,当阴极上有
溶液,当阴极上有 气体生成时,同时有
气体生成时,同时有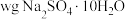 晶体析出,若温度不变,剩余溶液中溶质的质量分数应为
晶体析出,若温度不变,剩余溶液中溶质的质量分数应为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】利用所学电化学反应原理,解决以下问题:
Ⅰ.如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴 溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。
溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。
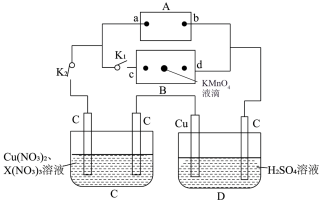
(1)闭合 ,断开
,断开 ,通电后,d端显红色,则电源b端为
,通电后,d端显红色,则电源b端为___________ 极,若c、d为惰性电极,检验c端产物的方法为___________ 。滤纸中央 溶液处发生的现象为
溶液处发生的现象为___________ 。
(2)已知C装置中溶液的溶质为 和
和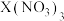 。且均为
。且均为 ,打开
,打开 ,关闭
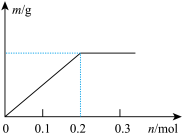
,关闭 ,通电一段时间后,阴极析出固体质量
,通电一段时间后,阴极析出固体质量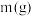 与通过电子的物质的量
与通过电子的物质的量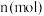 关系如图所示,则
关系如图所示,则 、
、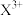 、
、 氧化能力由大到小的顺序是
氧化能力由大到小的顺序是___________ 。
(3)D装置中溶液是 溶液,则电极C端从开始至一段时间后的实验现象是
溶液,则电极C端从开始至一段时间后的实验现象是___________ 。
Ⅱ.铀(U)可用作核燃料,核废料中 价的铀
价的铀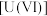 可以通过电化学还原法处理。
可以通过电化学还原法处理。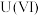 还原为
还原为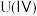 的电化学装置如图所示:
的电化学装置如图所示:

阴极上发生反应: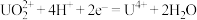 、
、
阴极区溶液中发生反应: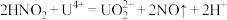
(4)反应 中,每生成
中,每生成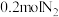 转移电子
转移电子___________  。
。
(5)阴极区溶液中加入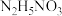 的目的是
的目的是___________ 。
(6)以恒定电流进行电解,测得阴极区溶液中部分离子的物质的量浓度随时间变化如图所示:
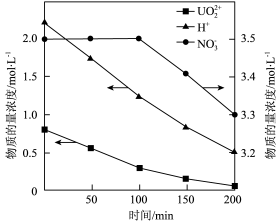
ⅰ.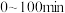 ,电路中每转移
,电路中每转移 ,阴极区
,阴极区 减少
减少___________  。
。
ⅱ.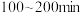 ,
,  下降速率低于
下降速率低于 前,原因是
前,原因是___________ 。
Ⅰ.如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴
 溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。
溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。

(1)闭合
 ,断开
,断开 ,通电后,d端显红色,则电源b端为
,通电后,d端显红色,则电源b端为 溶液处发生的现象为
溶液处发生的现象为(2)已知C装置中溶液的溶质为
 和
和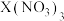 。且均为
。且均为 ,打开
,打开 ,关闭
,关闭 ,通电一段时间后,阴极析出固体质量
,通电一段时间后,阴极析出固体质量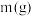 与通过电子的物质的量
与通过电子的物质的量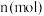 关系如图所示,则
关系如图所示,则 、
、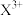 、
、 氧化能力由大到小的顺序是
氧化能力由大到小的顺序是(3)D装置中溶液是
 溶液,则电极C端从开始至一段时间后的实验现象是
溶液,则电极C端从开始至一段时间后的实验现象是Ⅱ.铀(U)可用作核燃料,核废料中
 价的铀
价的铀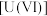 可以通过电化学还原法处理。
可以通过电化学还原法处理。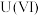 还原为
还原为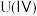 的电化学装置如图所示:
的电化学装置如图所示:
阴极上发生反应:
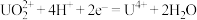 、
、
阴极区溶液中发生反应:
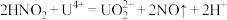
(4)反应
 中,每生成
中,每生成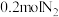 转移电子
转移电子 。
。(5)阴极区溶液中加入
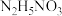 的目的是
的目的是(6)以恒定电流进行电解,测得阴极区溶液中部分离子的物质的量浓度随时间变化如图所示:

ⅰ.
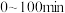 ,电路中每转移
,电路中每转移 ,阴极区
,阴极区 减少
减少 。
。ⅱ.
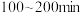 ,
,  下降速率低于
下降速率低于 前,原因是
前,原因是
您最近一年使用:0次



