取W g NaHCO3固体加热使其完全分解,将生成的CO2通入足量澄清石灰水中全部吸收,生成5.0 g CaCO3沉淀。试计算:
(1)CaCO3的物质的量为_______ mol。
(2)NaHCO3固体的质量w=_______ 。
(1)CaCO3的物质的量为
(2)NaHCO3固体的质量w=
20-21高一·浙江·阶段练习 查看更多[1]
(已下线)【浙江新东方】高中化学20210304-026
更新时间:2021-03-23 10:14:06
|
相似题推荐
【推荐1】(1)把一定质量的镁、铝混合物投入到1mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入1mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。则:
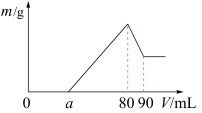
①金属铝的质量为________ g
②a的取值范围是________ mL。
(2)浓度分别为1mol /L的硫酸、氢氧化钠溶液各200mL分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为8:9,则甲、乙两烧杯中加入的铝的物质的为______ 。

①金属铝的质量为
②a的取值范围是
(2)浓度分别为1mol /L的硫酸、氢氧化钠溶液各200mL分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为8:9,则甲、乙两烧杯中加入的铝的物质的为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】现有300mLH2SO4和Al2(SO4)3的混合溶液,将其分成三等份,向第一份中加入1.00mol•L-1BaCl2溶液,至恰好不再产生沉淀,消耗100mL,将沉淀过滤、洗涤、干燥,称其质量为mg;向第二份溶液中加入铁片,充分反应后,溶液质量增加了0.54g;向第三份溶液加入2.00mol•L-1的NaOH溶液,当沉淀量达最大时,所加入NaOH溶液的体积为VmL。试计算:
(1)m=________ 。
(2)原混合液中c(H+)=________ 。
(3)V=________ 。
(1)m=
(2)原混合液中c(H+)=
(3)V=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室中有一瓶碳酸氢钾固体,因受热而部分变质(杂质为K2CO3,假设杂质分布均匀)。为测定其组成,称取12.76 g样品溶于水,配成500 mL溶液。取出25.00 mL该溶液,加入0.1000 mol/LBa(OH)2 溶液至60.00mL时沉淀量达到最大。回答下列问题:
(1)写出碳酸氢钾固体受热分解的化学方程式:_______ 。
(2)写出样品溶液与Ba(OH)2溶液反应的离子方程式:_______ 。
(3)12.76g样品中碳酸氢钾物质的量为_______ ,碳酸钾物质的量为_______ 。
(1)写出碳酸氢钾固体受热分解的化学方程式:
(2)写出样品溶液与Ba(OH)2溶液反应的离子方程式:
(3)12.76g样品中碳酸氢钾物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】将Na2CO3和NaHCO3的混合物充分加热,生成的气体(假设无损耗)全部通入足量的石灰水中,得到20.0g白色沉淀,加热后的残留物加入200mL盐酸恰好完全反应,生成5.60LCO2气体(标准状况下)。试回答下列问题:
(1)所加盐酸的物质的量浓度为_______ mol/L。
(2)原混合物中碳酸钠的质量是_______ g。
(1)所加盐酸的物质的量浓度为
(2)原混合物中碳酸钠的质量是
您最近一年使用:0次

 的物质的量是
的物质的量是

