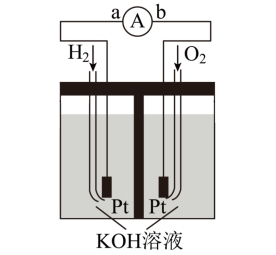
如图所示,甲是甲烷燃料电池,乙槽是给铁表面镀铜的装置,丙槽中C、D是碳棒。回答下列问题
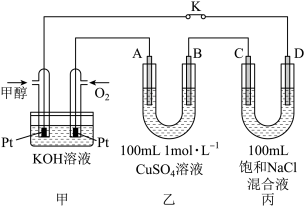
(1)①甲中通入甲烷的一极为___________ 极(用“正”、“负”、“阴”或“阳”),连接乙、丙槽线路中,电子流动的方向是B___________ C(用“→”或“←”填空)。
②乙槽中,A电极的材料为___________ 。
(2)①写出B极上反应的电极反应式:___________ 。
②写出丙槽中总反应的化学方程式:___________
③写出甲中通入O2极上反应的电极反应式:___________
④写出甲中通入甲烷极上反应的电极反应式:___________
(3)若将乙槽中的A、B电极换成惰性电极进行电解,一段时间后,在相同条件下A、B两极收集到相同体积的气体,停止电解。欲将电解后的溶液恢复如初,则应加入的一种物质为___________ ,质量为___________ g。

(1)①甲中通入甲烷的一极为
②乙槽中,A电极的材料为
(2)①写出B极上反应的电极反应式:
②写出丙槽中总反应的化学方程式:
③写出甲中通入O2极上反应的电极反应式:
④写出甲中通入甲烷极上反应的电极反应式:
(3)若将乙槽中的A、B电极换成惰性电极进行电解,一段时间后,在相同条件下A、B两极收集到相同体积的气体,停止电解。欲将电解后的溶液恢复如初,则应加入的一种物质为
更新时间:2021-04-15 12:32:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为:___________ 。
(2) FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu =2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:___________ 。当线路中转移0.2mol电子时,则被腐蚀铜的质量为:___________ g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为___________ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,下图是电解质为稀硫酸溶液的甲烷燃料电池工作原理示意图,a、b均为惰性电极。
回答下列问题:
②使用时,空气从___________ (填“A”或“B”)口通入。
②a极的电极反应式为___________ 。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为:
(2) FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu =2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,下图是电解质为稀硫酸溶液的甲烷燃料电池工作原理示意图,a、b均为惰性电极。

回答下列问题:
②使用时,空气从
②a极的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义。图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
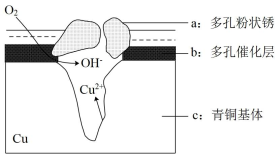
①腐蚀过程中,负极是_____ (填图中字母“a”或“b”或“c”)
②环境中的Clˉ̄扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈Cu2(OH)3Cl,其离子方程式为_____ ;
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为_____ L(标准状况)。

①腐蚀过程中,负极是
②环境中的Clˉ̄扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈Cu2(OH)3Cl,其离子方程式为
③若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是一个化学过程的示意图

(1)图中甲池是_____ 装置(填“电解池”或“原电池”)。
(2)写出通入CH4的电极的电极反应式:_____ 。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为_____ 极(填“A”或“B”),并写出此电极的反应式:_____ 。
(4)乙池中总反应的离子方程式_____ 。
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的氢离子浓度是_____ (若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是_____ 。
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3

(1)图中甲池是
(2)写出通入CH4的电极的电极反应式:
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为
(4)乙池中总反应的离子方程式
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的氢离子浓度是
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
您最近半年使用:0次
【推荐1】纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
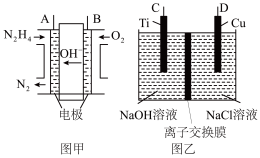
(1)上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”),该电解池中离子交换膜为________ 离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为________________________________________ ,
肼燃料电池中A极发生的电极反应为____________________________ 。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。

(1)上述装置中D电极应连接肼燃料电池的
(2)该电解池的阳极反应式为
肼燃料电池中A极发生的电极反应为
(3)当反应生成14.4 g Cu2O时,至少需要肼
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
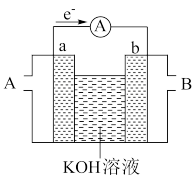
【推荐2】某课外活动小组用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应式为______________ 。
(2)若开始时开关K与b连接,则B极的电极反应式为__________ ,总反应的离子方程式为____________ 。
(3)若开始时开关K与b连接.下列说法正确的是_______ 。
A.溶液中Na+向A极移动
B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为________ 。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)________ 导出。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因_________________________ 。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b连接,则B极的电极反应式为
(3)若开始时开关K与b连接.下列说法正确的是
A.溶液中Na+向A极移动
B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】电化学与能源、材料、化工等领域紧密联系,应用广泛.利用N2H4燃料电池电解AgNO3溶液并制备 ,装置如图所示(
,装置如图所示( 均为石墨电极,假设各装置在工作过程中溶液体积不变).
均为石墨电极,假设各装置在工作过程中溶液体积不变).
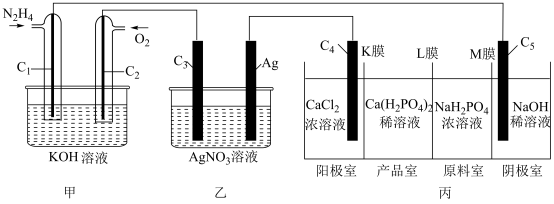
(1)工作时,甲装置 电极为
电极为________ (填“正”“负”“阳”或“阴”)极,电极反应式为________ 。
(2)工作时,乙装置中 向
向________ (填“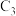 ”或“Ag”)极移动.
”或“Ag”)极移动.
(3)若乙装置中溶液体积为400mL,当电极质量增加4.32g时,溶液pH约为________ 。若将乙装置中两电极调换,一段时间后, 溶液浓度将
溶液浓度将________ (填“增大”“减小”或“不变”).
(4)丙装置中K、M、L为离子交换膜,其中M膜是________ (填“阳离子”“阴离子”或“质子”)交换膜.
(5)若甲装置 电极上消耗标准状况下2.24L的
电极上消耗标准状况下2.24L的 ,理论上丙装置阳极室溶液质量减少
,理论上丙装置阳极室溶液质量减少________ g.
 ,装置如图所示(
,装置如图所示( 均为石墨电极,假设各装置在工作过程中溶液体积不变).
均为石墨电极,假设各装置在工作过程中溶液体积不变).
(1)工作时,甲装置
 电极为
电极为(2)工作时,乙装置中
 向
向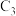 ”或“Ag”)极移动.
”或“Ag”)极移动.(3)若乙装置中溶液体积为400mL,当电极质量增加4.32g时,溶液pH约为
 溶液浓度将
溶液浓度将(4)丙装置中K、M、L为离子交换膜,其中M膜是
(5)若甲装置
 电极上消耗标准状况下2.24L的
电极上消耗标准状况下2.24L的 ,理论上丙装置阳极室溶液质量减少
,理论上丙装置阳极室溶液质量减少
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是一个化学过程的示意图。

请回答:
(1)甲池是________ 池,该电池的总反应方程式为______________ 。
(2)乙池中A电极名称为________ 极,电极反应式为__________________ 。一段时间后溶液的pH________ (填“增大”、“减小”或“不变”)。
(3)当乙池中B(Ag)极的质量增加5.40g时,丙池CuSO4溶液中理论上生成O2________ mL(标准状况下)。

请回答:
(1)甲池是
(2)乙池中A电极名称为
(3)当乙池中B(Ag)极的质量增加5.40g时,丙池CuSO4溶液中理论上生成O2
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
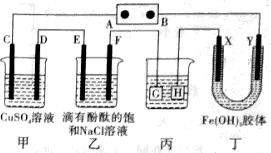
【推荐3】如图装置,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答下列问题:
(1)B极是电源的_____________ ,一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明_____________ ,在电场作用下向Y极移动,这是胶体的_____________ 现象。
(2)若甲、乙装置中的D、C、E、F电极均只有一种单质生成时,对应单质的物质的量之比为_____________ 。
(3)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_____________ .
(4)现用丙装置给铜件镀银,则H应该是_____________ (填“镀层金属”或“镀件”),当乙中溶液的pH=13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为_____________ g。

请回答下列问题:
(1)B极是电源的
(2)若甲、乙装置中的D、C、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是
(4)现用丙装置给铜件镀银,则H应该是
您最近半年使用:0次