某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)反应最剧烈的烧杯中金属是_______ (填字母序号);
A.钠 B.镁 C.铝 D.钾
(2)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法_______ (填字母序号)。
A.把烧杯中的冷水换成热水
B.把烧杯中的冷水换成盐酸
C.把烧杯中的冷水换成浓硝酸
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题实验装置:(已知酸性强弱:亚硫酸>碳酸)

(3)铜与浓硫酸反应的化学方程式是_______ ;
(4)能说明碳元素的非金属性比硅元素非金属性强的实验现象是_______ ;试管F中发生反应的离子方程式为_______ 。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)反应最剧烈的烧杯中金属是
A.钠 B.镁 C.铝 D.钾
(2)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法
A.把烧杯中的冷水换成热水
B.把烧杯中的冷水换成盐酸
C.把烧杯中的冷水换成浓硝酸
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题实验装置:(已知酸性强弱:亚硫酸>碳酸)

(3)铜与浓硫酸反应的化学方程式是
(4)能说明碳元素的非金属性比硅元素非金属性强的实验现象是
更新时间:2021-04-29 15:14:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】根据下图所示实验,回答问题:
(1)实验①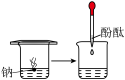 观察到的现象是
观察到的现象是________________________ 。实验②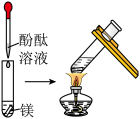 观察到的现象是
观察到的现象是________________________ 。
(2)实验③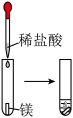 观察到的现象是
观察到的现象是________________________ 。实验④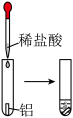 观察到的现象是
观察到的现象是________________________ 。
(3)由上述实验,你能得出的结论是________________________ 。
(4)请总结同周期元素金属性的变化规律__________ ,并用原子结构解释其原因_________ 。
(1)实验①
 观察到的现象是
观察到的现象是 观察到的现象是
观察到的现象是(2)实验③
 观察到的现象是
观察到的现象是 观察到的现象是
观察到的现象是(3)由上述实验,你能得出的结论是
(4)请总结同周期元素金属性的变化规律
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】利用如图装置可验证同主族元素非金属性的变化规律。

(1)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液___ 的现象,即可证明。从环保角度考虑,此装置缺少尾气处理装置,可用___ 溶液吸收尾气。请写出一种制氯气的化学反应方程式:___ 。
(2)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液___ 的现象,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有___ 溶液的洗气瓶。

(1)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(2)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】1.航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置。它可直接将化学能转化为电能,氢氧燃料电池以KOH溶液为电解质,其总反应的化学方程式为2H2+O2=2H2O。
(1)负极上的电极反应为______ 。
(2)消耗标准状况下的5.6LO2时,有____ mol电子发生转移。
(3)工作过程中时,溶液的c(OH-)____ (填“增大”、“减小”或“不变”)。
2.证明卤族元素的非金属性强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检查)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是________ 。
(2)B中溶液发生反应的离子方程式是________ 。
(3)为验证溴的氧化性强于碘,过程 Ⅳ 的操作和现象是______ 。
(4)过程Ⅲ实验的目的是________ 。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐___ ,得电子能力逐渐____ 。
(1)负极上的电极反应为
(2)消耗标准状况下的5.6LO2时,有
(3)工作过程中时,溶液的c(OH-)
2.证明卤族元素的非金属性强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检查)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是
(2)B中溶液发生反应的离子方程式是
(3)为验证溴的氧化性强于碘,过程 Ⅳ 的操作和现象是
(4)过程Ⅲ实验的目的是
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。

I.将 NaOH溶液与 NH4Cl 溶液混合生成 NH3·H2O,从而验证 NaOH的碱性大于 NH3·H2O,继而可以验证 Na 的金属性大于 N,你认为此设计是否合理? 并说明理由:_____________________ 。
II.根据下图所示装置图回答以下问题。
(1)利用如图装置可以验证元素的非金属性的变化规律。图中 A 装置名称是____________ ,干燥管 D的作用是______________ 。
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为_____________________ 。
(3)若要用此装置证明酸性: HNO3>H2CO3>H2SiO3 进而证明非金属性: N>C>Si,从以下所 给物质中选出甲同学设计的实验所用到物质:
①稀 HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置 A、C中所选试剂分别为______________ (填序号);能说明酸性 H2CO3>H2SiO3的实验现象是________________________________________________________________________ 。

I.将 NaOH溶液与 NH4Cl 溶液混合生成 NH3·H2O,从而验证 NaOH的碱性大于 NH3·H2O,继而可以验证 Na 的金属性大于 N,你认为此设计是否合理? 并说明理由:
II.根据下图所示装置图回答以下问题。
(1)利用如图装置可以验证元素的非金属性的变化规律。图中 A 装置名称是
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为
(3)若要用此装置证明酸性: HNO3>H2CO3>H2SiO3 进而证明非金属性: N>C>Si,从以下所 给物质中选出甲同学设计的实验所用到物质:
①稀 HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置 A、C中所选试剂分别为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】利用如图装置可验证同主族元素非金属性的变化规律。

(1)仪器A的名称为______ ,干燥管D的作用为______ 。
(2)若要证明非金属性: ,C中为淀粉
,C中为淀粉 碘化钾混合溶液,B中装有
碘化钾混合溶液,B中装有 固体,则A中试剂为
固体,则A中试剂为______ ,观察到C中溶液______  填现象
填现象 ,即可证明。从环境保护的观点考虑,此装置缺点
,即可证明。从环境保护的观点考虑,此装置缺点______ 。
(3)若要证明非金属性: ,则在A中
,则在A中______ B中加______ 、C中加______ ,写出C中反应的化学方程式______

(1)仪器A的名称为
(2)若要证明非金属性:
 ,C中为淀粉
,C中为淀粉 碘化钾混合溶液,B中装有
碘化钾混合溶液,B中装有 固体,则A中试剂为
固体,则A中试剂为 填现象
填现象 ,即可证明。从环境保护的观点考虑,此装置缺点
,即可证明。从环境保护的观点考虑,此装置缺点(3)若要证明非金属性:
 ,则在A中
,则在A中
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学设计如图装置,研究非金属元素性质变化规律。

(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,强酸一般能制取弱酸。现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如图装置来证明酸性:HNO3>H2CO3>H2SiO3。(不考虑硝酸的挥发性)
A、B、C中盛装的试剂分别为________ 、________ 、________ 。C中实验现象为_____________________________________________________ ;
写出C中发生反应的离子方程式:__________________________________ 。
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用图中装置证明氯气氧化性强于碘单质的氧化性。A中盛装浓盐酸,B中装入高锰酸钾粉末,实验时C中溶液变成蓝色,则C中盛装的试剂为________ ;写出C中离子方程式____________________________________________________________________ 。
该实验该装置有明显不足,请指出改进方法:______________________________________________ 。
(3)如果C中盛装饱和氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀。写出该反应的化学方程式:______________________________________ ;
如果将SO2气体通入饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2________ (填字母)。
A.漂白性 B.氧化性
C.还原性 D.酸性

(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,强酸一般能制取弱酸。现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如图装置来证明酸性:HNO3>H2CO3>H2SiO3。(不考虑硝酸的挥发性)
A、B、C中盛装的试剂分别为
写出C中发生反应的离子方程式:
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用图中装置证明氯气氧化性强于碘单质的氧化性。A中盛装浓盐酸,B中装入高锰酸钾粉末,实验时C中溶液变成蓝色,则C中盛装的试剂为
该实验该装置有明显不足,请指出改进方法:
(3)如果C中盛装饱和氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀。写出该反应的化学方程式:
如果将SO2气体通入饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2
A.漂白性 B.氧化性
C.还原性 D.酸性
您最近一年使用:0次



