几种短周期元素的原子半径及主要化合价如下表
下列有关这几种元素的叙述中,正确的是
| 元素代号 | X | Y | Z | W |
| 原子半径/nm | 0.160 | 0.143 | 0.070 | 0.066 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A.元素的金属性:X<Y |
| B.Z原子的最外层电子数为7 |
| C.元素的简单离子半径:r(X2+)>r(W2-) |
| D.元素Y的最高价氧化物能溶于氢氧化钠溶液 |
更新时间:2021-05-07 18:12:50
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列判断错误的是
| A.稳定性:H2O>H2S>H2Se | B.半径:Na+>Mg2+>F- |
| C.酸性:HClO4>H2SO4>H3PO4 | D.碱性:NaOH>Mg(OH)2>Al(OH)3 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列“最值”描述情况正确的是
| A.第二周期所有元素的第一电离能:最大的是F,最小的是 Li |
| B.第三周期主族元素离子半径:最大的是Clˉ,最小的是Al3+ |
| C.第三周期元素最高价氧化物的水化物:酸性最强的是HClO,碱性最强的是 NaOH |
| D.第VIA族元素的最简单氢化物的沸点,最高的是H2O,最低的是H2S |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】联合国将2019年定为“国际化学元素周期表年”,以纪念门捷列夫发现元素周期律150周年。元素周期律把元素及其化合物纳入一个统一的理论体系,为系统研究元素及其化合物提供了科学方法,为发现和探索斯元素、斯物质提供了有效思路。短周期主族元素X、Y、Z的原子序数依次增大,X原子的最外层电子数是次外层电子数的2倍,Y是地壳中含量最多的元素,Z是同周期金属性最强的元素。下列说法正确的是
| A.X元素位于第二周期VIA族 | B.简单气态氢化物的热稳定性:X>Y |
| C.Y与Z形成的化合物只有一种 | D.原子半径:r(Z)>r(X)>r(Y) |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】有A、B两种原子,A原子的第三电子层比B原子的第三电子层少3个电子,B原子的第二电子层电子数恰好为A原子第二电子层电子数的2倍.A和B分别是
| A.硅原子和钠原子 | B.硼原子和氦原子 | C.氯原子和碳原子 | D.碳原子和铝原子 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】甲元素原子的核电荷数为11,乙元素的质子数为8,甲和乙化合形成化合物丙,下列说法中错误的是( )
| A.甲形成+1价阳离子 | B.丙一定与水反应 |
| C.丙一定是MO型离子化合物 | D.丙中含有离子键 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】A、B、C、D均为短周期元素,它们在周期表中的位置如下图。若A原子的最外层电子数是次外层电子数的2倍。下列说法中正确的是
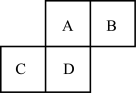

| A.D的单质常用做半导体材料 |
| B.最简单气态氢化物的热稳定性:A>B |
| C.B的最低负化合价:-2价 |
| D.原子半径大小:r(C)>r(B)>r(A) |
您最近半年使用:0次





