在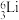 、
、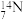 、
、 、
、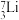 、
、 、
、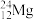 中
中
(1)互为同位素的是_______ 和_______ 。
(2)质量数相等,但不能互称同位素的是_______ 和_______ 。
(3)中子数相等,但质子数不相等的是_______ 和_______ 。
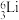 、
、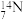 、
、 、
、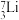 、
、 、
、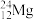 中
中(1)互为同位素的是
(2)质量数相等,但不能互称同位素的是
(3)中子数相等,但质子数不相等的是
20-21高一下·河北石家庄·期中 查看更多[2]
更新时间:2021-06-09 21:12:50
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.根据下列6种符号回答问题:
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)共有_____ 种核素,属于______ 种元素。
(2)互为同位素的是________ 。(填序号,下同)
(3)质量数相等的是______ ,中子数相等的是________ 。
II.现有6种物质: ①MgCl2 ②Cl2 ③SO2 ④K2CO3 ⑤Na2O2 ⑥NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物的是_________ 。
(2)只含离子键的化合物是_________ 。
(3)含非极性共价键的离子化合物是_________ 。
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)共有
(2)互为同位素的是
(3)质量数相等的是
II.现有6种物质: ①MgCl2 ②Cl2 ③SO2 ④K2CO3 ⑤Na2O2 ⑥NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物的是
(2)只含离子键的化合物是
(3)含非极性共价键的离子化合物是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有X、Y、Z三种元素:
(1)X元素原子的核电荷数为8,其原子核内的质子数为_______ ,该元素的二价阴离子中,核外电子数为_______ ,中子数为9的核素表示为_______ 。
(2)Y元素的一价阳离子核外有18个电子,质量数为40,该元素原子的原子核内中子数为_______ 。
(3)2gZO 中电子数比质子数多3.01×1022个,则Z的相对原子质量为
中电子数比质子数多3.01×1022个,则Z的相对原子质量为_______ 。
(1)X元素原子的核电荷数为8,其原子核内的质子数为
(2)Y元素的一价阳离子核外有18个电子,质量数为40,该元素原子的原子核内中子数为
(3)2gZO
 中电子数比质子数多3.01×1022个,则Z的相对原子质量为
中电子数比质子数多3.01×1022个,则Z的相对原子质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】I.下列7种化学符号:18O;14C;23Na;14N;32S; 16O; 1H2
(1)表示核素的符号共______ 种。
(2)互为同位素的是______ 和______ 。
(3)质量数相等,但不能互为同位素的是______ 和______ 。
(4)中子数相等,但质子数不相等的是______ 和______ 。
II.(1)写出下列物质的电子式: NH3_____________ , CO2______ 。
(2)2.2g铵根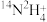 的中子数是
的中子数是___ ,核外电子数是____ ,某微粒含有一个原子核,核中有 17个质子,20个中子,核外有18个电子,该粒子的化学符号是____ 。
(3)已知断开 1mol H—H 键、1mol I—I 键、1mol H—I 键分别需要吸收的能量为 436kJ、151kJ、299kJ,则由 1mol H2和 1mol I2生成 2mol HI会_____ (“放出”或“吸收”)_____ kJ 的热量。
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S,只由离子键构成的物质是_____ (填序号,下同),由离子键和非极性共价键构成的物质是________ ,属于共价化合物的是_____ 。
(1)表示核素的符号共
(2)互为同位素的是
(3)质量数相等,但不能互为同位素的是
(4)中子数相等,但质子数不相等的是
II.(1)写出下列物质的电子式: NH3
(2)2.2g铵根
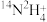 的中子数是
的中子数是(3)已知断开 1mol H—H 键、1mol I—I 键、1mol H—I 键分别需要吸收的能量为 436kJ、151kJ、299kJ,则由 1mol H2和 1mol I2生成 2mol HI会
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S,只由离子键构成的物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】有下列四种微粒:① ②
② ③
③ ④
④ 。(只填序号,下同)。
。(只填序号,下同)。
(1)按原子半径由大到小的顺序排列为_______ ;微粒中质子数小于中子数的是_______ 。
(2)能形成 型化合物的是
型化合物的是_______ ;通常情况下,化合价有零价、正价和负价的是_______ 。
 ②
② ③
③ ④
④ 。(只填序号,下同)。
。(只填序号,下同)。(1)按原子半径由大到小的顺序排列为
(2)能形成
 型化合物的是
型化合物的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】钋(PO)是一种低熔点金属,极其稀有,毒性和放射性极强。回答下列问题:
(1) 具有放射性,经
具有放射性,经 衰变成稳定的Pb原子,在衰变过程中释放一个
衰变成稳定的Pb原子,在衰变过程中释放一个 。生成的Pb的原子核中质子数为
。生成的Pb的原子核中质子数为___________ ,中子数为___________ 。Po元素能形成较稳定的+4价离子, 含有的电子的物质的量为
含有的电子的物质的量为___________ 。
(2)下列有关的说法正确的是___________ 。
a.由 衰变为铅的变化是化学变化
衰变为铅的变化是化学变化
b.钋元素的相对原子质量为210
c.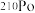 比
比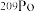 原子核多一个中子
原子核多一个中子
d.研究表明,烟草中含有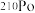 和
和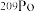 等,它们互为同位素
等,它们互为同位素
(3)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间。已知 的半衰期为138天,质量为64克的
的半衰期为138天,质量为64克的 ,经276天后,得到铅的质量为
,经276天后,得到铅的质量为___________ 。
(1)
 具有放射性,经
具有放射性,经 衰变成稳定的Pb原子,在衰变过程中释放一个
衰变成稳定的Pb原子,在衰变过程中释放一个 。生成的Pb的原子核中质子数为
。生成的Pb的原子核中质子数为 含有的电子的物质的量为
含有的电子的物质的量为(2)下列有关的说法正确的是
a.由
 衰变为铅的变化是化学变化
衰变为铅的变化是化学变化b.钋元素的相对原子质量为210
c.
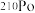 比
比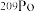 原子核多一个中子
原子核多一个中子d.研究表明,烟草中含有
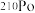 和
和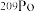 等,它们互为同位素
等,它们互为同位素(3)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间。已知
 的半衰期为138天,质量为64克的
的半衰期为138天,质量为64克的 ,经276天后,得到铅的质量为
,经276天后,得到铅的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求回答下列问题。
(1)28.5g某金属氯化物MCl2中含有0.6molCl-,M的相对原子质量为_______ 。
(2)标准状况下CO和CO2混合气体6.72L,其质量为10g,则此混合气体中,CO和CO2的物质的量之比为_______ 。
(3)中子数为20的钙原子,其微粒符号可表示为_______ 。
(4)质量数为23、中子数为12的原子,其结构示意图可表示为_______ 。
(5)核内中子数为N的R2+,质量数为A,则该离子的核外电子数为_______ 。
(1)28.5g某金属氯化物MCl2中含有0.6molCl-,M的相对原子质量为
(2)标准状况下CO和CO2混合气体6.72L,其质量为10g,则此混合气体中,CO和CO2的物质的量之比为
(3)中子数为20的钙原子,其微粒符号可表示为
(4)质量数为23、中子数为12的原子,其结构示意图可表示为
(5)核内中子数为N的R2+,质量数为A,则该离子的核外电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】开发利用核能可以减少对化石能源的依赖。UO2是一种常用的核燃料,其铀元素中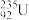 需达到5%。该核燃料的一种制备流程如下:
需达到5%。该核燃料的一种制备流程如下:
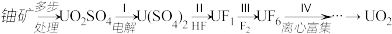
(1)天然铀主要含99.3% 和0.7%
和0.7%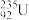 ,
, 和
和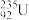 互为
互为_______ 。
(2)I中,将含有硫酸的UO2SO4溶液通入电解槽,如下图所示。

①A电极是_______ (填“阴极”或“阳极”),其电极反应式是_______ 。
②U4+有较强的还原性。用质子交换膜隔开两极区溶液可以_______ ,从而提高U4+的产率。
(3)III中使用的F2可通过电解熔融KF、HF混合物制备,不能直接电解液态HF的理由是HF属于___ 化合物,液态HF几乎不电离。
(4)IV中利用了相对分子质量对气体物理性质的影响。铀的氟化物的熔沸点如下:
①离心富集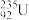 时,采用UF6的优点:
时,采用UF6的优点:
a.F只有一种核素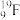 ,且能与U形成稳定的氟化物;
,且能与U形成稳定的氟化物;
b._______ 。
②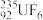 和
和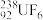 的相对分子质量之比约为
的相对分子质量之比约为_______ (列出计算表达式)。
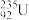 需达到5%。该核燃料的一种制备流程如下:
需达到5%。该核燃料的一种制备流程如下: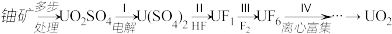
(1)天然铀主要含99.3%
 和0.7%
和0.7%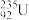 ,
, 和
和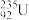 互为
互为(2)I中,将含有硫酸的UO2SO4溶液通入电解槽,如下图所示。

①A电极是
②U4+有较强的还原性。用质子交换膜隔开两极区溶液可以
(3)III中使用的F2可通过电解熔融KF、HF混合物制备,不能直接电解液态HF的理由是HF属于
(4)IV中利用了相对分子质量对气体物理性质的影响。铀的氟化物的熔沸点如下:
| UF4 | UF6 | |
| 熔点/℃ | 1036 | 64(150kPa) |
| 沸点/℃ | 1417 | 56.5升华 |
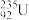 时,采用UF6的优点:
时,采用UF6的优点:a.F只有一种核素
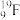 ,且能与U形成稳定的氟化物;
,且能与U形成稳定的氟化物;b.
②
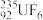 和
和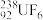 的相对分子质量之比约为
的相对分子质量之比约为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】各题中的物质均由核电荷数为1~10的元素组成,按要求填写化学式:
(1)只有两个原子核和两个电子组成的分子是___________ ;
(2)最外层分别为4个和6个电子的原子形成的化合物是___________ ;
(3)最外层有5个电子的原子所形成的氢化物___________ ;
(4)由3个原子组成的电子总数为10的化合物是___________ ;
(5)离子化合物AB中阴阳离子的电子层结构相同,则化合物AB是___________ 。
(1)只有两个原子核和两个电子组成的分子是
(2)最外层分别为4个和6个电子的原子形成的化合物是
(3)最外层有5个电子的原子所形成的氢化物
(4)由3个原子组成的电子总数为10的化合物是
(5)离子化合物AB中阴阳离子的电子层结构相同,则化合物AB是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】 有下列各组微粒、物质:①金刚石、石墨 ② CH3-O-CH3、CH3-CH2-OH ③16O、18O ④ CH3-CH2-CH =CH2、CH3-CH=CH-CH3 ⑤ O2、O3 ⑥12C、13C。其中组内互为同素异形体的是(选填编号,下同):_______ ,互为同位素的是_______ ,互为同分异构体的是_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氯元素有两种核素 Cl、
Cl、 Cl。
Cl。
(1)关于 Cl原子说法正确的是
Cl原子说法正确的是_______ 。
(2) Cl、
Cl、 Cl具有
Cl具有_______ 。
(3) Cl、
Cl、 Cl都属于氯元素,由此可知:
Cl都属于氯元素,由此可知:_______ 决定元素种类,_______ 决定核素种类。
(4) Cl、
Cl、 Cl互为何种关系
Cl互为何种关系_______ ?
(5)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:_______ 、_______ 、_______ 。
(6)Br、Cl都属于卤族元素。某教材中有下面一段话:
For many years chemists were unsuccessfully tried to prepare the perbromateion,BrO 。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing:
。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing: SeO
SeO →
→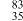 BrO
BrO +e-。以下说法正确的是
+e-。以下说法正确的是_______ 。
(7)已知:氯元素的近似相对原子质量为35.5。STP下,11.2LHCl气体中含H35Cl_______ mol。
 Cl、
Cl、 Cl。
Cl。(1)关于
 Cl原子说法正确的是
Cl原子说法正确的是| A.中子数等于质子数 | B.质子数等于电子数 |
| C.质子数等于质量数 | D.电子数等于中子数 |
 Cl、
Cl、 Cl具有
Cl具有| A.相同质量数 | B.不同质子数 | C.相同中子数 | D.相同电子数 |
 Cl、
Cl、 Cl都属于氯元素,由此可知:
Cl都属于氯元素,由此可知:(4)
 Cl、
Cl、 Cl互为何种关系
Cl互为何种关系(5)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:
(6)Br、Cl都属于卤族元素。某教材中有下面一段话:
For many years chemists were unsuccessfully tried to prepare the perbromateion,BrO
 。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing:
。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing: SeO
SeO →
→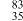 BrO
BrO +e-。以下说法正确的是
+e-。以下说法正确的是| A.该过程发生了化学变化 | B.Br元素的质量数为83 |
C. SeO SeO 中含有68个电子 中含有68个电子 | D. Se与 Se与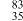 Br互为同位素 Br互为同位素 |
您最近一年使用:0次

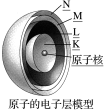
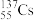 进行“无损探伤”,该原子___________
进行“无损探伤”,该原子___________

