实验室中需要用氢氧化钠固体配制480mL0.10mol•L-1的NaOH溶液,就该实验回答下列问题:
(1)请写出该实验的实验步骤。
①计算,②___ ,③溶解冷却,④转移,⑤洗涤振荡,⑥___ ,⑦摇匀,⑧装瓶贴签。
(2)用天平称量NaOH固体的质量为___ 。实验所需要的仪器除托盘天平、烧杯、药匙外,还有___ 、___ 、___ 。
(3)试分析下列操作对所配溶液的浓度有何影响。(填偏大或偏小或不变)
①定容时,俯视容量瓶刻度线进行定容。对所配溶液浓度的影响:___ 。
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线。对所配溶液浓度的影响:___ 。
③容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水。对所配溶液浓度的影响:___ 。
(4)从该溶液中取出50mL,其中所取NaOH的物质的量浓度为___ ,将取出的50mL溶液加水稀释到了___ mL,稀释后溶液中NaOH的物质的量浓度为0.025mol/L。
(1)请写出该实验的实验步骤。
①计算,②
(2)用天平称量NaOH固体的质量为
(3)试分析下列操作对所配溶液的浓度有何影响。(填偏大或偏小或不变)
①定容时,俯视容量瓶刻度线进行定容。对所配溶液浓度的影响:
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线。对所配溶液浓度的影响:
③容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水。对所配溶液浓度的影响:
(4)从该溶液中取出50mL,其中所取NaOH的物质的量浓度为
更新时间:2021-06-09 15:46:13
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
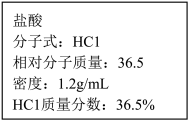
(1)该浓盐酸的物质的量浓度为___________ mol/L。
(2)某学生现需450 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取___________ mL上述浓盐酸进行配制。
②配制时正确的操作顺序是(用字母表示)___________ ;
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中, 用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”)。
I、用量筒量取浓盐酸时俯视观察凹液面___________ ;
II、用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶___________ ;
III、溶液注入容量瓶前没有恢复到室温就进行定容___________ 。
(3)若在标准状况下,将V LHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为___________mol/L。(填字母)
(4)现将100mL 0.5mol/L的盐酸(密度为d1g/cm3)与200mL 0.1mol/LCuCl 溶液(密度为d2g/cm3)混合,所得密度为d3g/cm3的混合溶液中Cl
溶液(密度为d2g/cm3)混合,所得密度为d3g/cm3的混合溶液中Cl 的物质的量浓度是
的物质的量浓度是___________ 。(用含d1、d2、d3的式子表示)

(1)该浓盐酸的物质的量浓度为
(2)某学生现需450 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取
②配制时正确的操作顺序是(用字母表示)
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中, 用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”)。
I、用量筒量取浓盐酸时俯视观察凹液面
II、用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶
III、溶液注入容量瓶前没有恢复到室温就进行定容
(3)若在标准状况下,将V LHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为___________mol/L。(填字母)
A.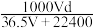 | B.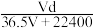 | C.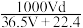 | D.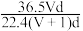 |
 溶液(密度为d2g/cm3)混合,所得密度为d3g/cm3的混合溶液中Cl
溶液(密度为d2g/cm3)混合,所得密度为d3g/cm3的混合溶液中Cl 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常稀释100倍(体积之比)后使用请回答下列问题:
(1)该“84”消毒液的物质的量浓度约_______ mol·L-1(小数点后保留一位)。
(2)某同学取100 mL该“84”消毒液,稀释后用于消毒,稀释后的溶液中c(Na+) =_______ mol·L-1下列为打乱了的操作示意图,其正确排序为 _______ 。

(3)配制过程中下列各操作对消毒液物质的量浓度有何影响(填“偏小”、“偏大”或“无影响”)
①用托盘天平称量NaClO固体时,砝码生锈_______ 。
②容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水_______ 。
③定容时,俯视容量瓶刻度线进行定容_______ 。
| 品名:84消毒液 有效成分:NaClO 规格:1000 mL 质量分数:25% 密度:1.19 g·cm-3 |
(2)某同学取100 mL该“84”消毒液,稀释后用于消毒,稀释后的溶液中c(Na+) =

(3)配制过程中下列各操作对消毒液物质的量浓度有何影响(填“偏小”、“偏大”或“无影响”)
①用托盘天平称量NaClO固体时,砝码生锈
②容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
③定容时,俯视容量瓶刻度线进行定容
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
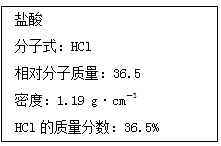
【推荐3】如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为______ mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________ 。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸加蒸馏水稀释至500 mL,得到物质的量浓度为0.400 mol·L-1的稀盐酸。该学生需要量取________ mL上述浓盐酸进行配制。
(4)假设该同学用0.400 mol·L-1的盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸加蒸馏水稀释至500 mL,得到物质的量浓度为0.400 mol·L-1的稀盐酸。该学生需要量取
(4)假设该同学用0.400 mol·L-1的盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.某同学在实验室配制了一瓶500 浓度约为0.1
浓度约为0.1 的
的 溶液。现欲测定其准确浓度,用20.00
溶液。现欲测定其准确浓度,用20.00 浓度为0.1010
浓度为0.1010 的邻苯二甲酸氢钾(
的邻苯二甲酸氢钾(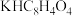 )标准溶液与该
)标准溶液与该 溶液反应,测得恰好完全反应时平均消耗该
溶液反应,测得恰好完全反应时平均消耗该 溶液的体积为18.50
溶液的体积为18.50 。(已知:
。(已知: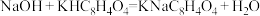 )
)
(1) 溶液需要经过标准溶液测定后方可确定其准确浓度(排除操作因素),原因可能是
溶液需要经过标准溶液测定后方可确定其准确浓度(排除操作因素),原因可能是_______
(2)经测定,该 溶液的浓度为
溶液的浓度为_____ (保留4位有效数字)。
(3)该实验大约需要80 0.1010
0.1010 的
的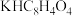 标准溶液。
标准溶液。
①配制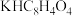 溶液时,不需要用到的仪器为
溶液时,不需要用到的仪器为_______ 、_______ (选填序号)。

②配制该溶液过程中,下列操作可能引起所配溶液浓度偏高的是_______ (填序号)。
a.容量瓶未干燥,含有少量蒸馏水 b.转移溶液时不慎有少量液体洒到容量瓶外面
c.溶液从烧杯转移到容量瓶后没有洗涤烧杯 d.定容时俯视刻度线
Ⅱ.欲配制250 0.1
0.1 的稀盐酸,实验室的浓盐酸密度为1.25
的稀盐酸,实验室的浓盐酸密度为1.25 ,质量分数为36.5%。请回答下列问题:
,质量分数为36.5%。请回答下列问题:
(4)需要量取浓盐酸的体积为_______  。
。
(5)配制该溶液的操作顺序是:D→_______ →B(用字母符号表示,每个字母符号只用一次)。
A.用30 蒸馏水洗涤烧杯和玻璃棒各2~3次,将洗涤液全部注入容量瓶中并轻轻摇动
蒸馏水洗涤烧杯和玻璃棒各2~3次,将洗涤液全部注入容量瓶中并轻轻摇动
B.将容量瓶盖紧,振满,摇匀
C.将已恢复至室温的盐酸沿玻璃棒注入所选用的容量瓶中
D.用量筒准确量取所需体积的浓盐酸,将其沿玻璃棒注入烧杯中,再向烧杯中加入少量蒸馏水(约30 ),用玻璃棒慢慢搅动,使其混合均匀
),用玻璃棒慢慢搅动,使其混合均匀
E.改用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶的刻度线相切
F.继续往容量瓶中小心地滴加蒸馏水,直到液面接近刻度线1~2 处
处
 浓度约为0.1
浓度约为0.1 的
的 溶液。现欲测定其准确浓度,用20.00
溶液。现欲测定其准确浓度,用20.00 浓度为0.1010
浓度为0.1010 的邻苯二甲酸氢钾(
的邻苯二甲酸氢钾(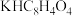 )标准溶液与该
)标准溶液与该 溶液反应,测得恰好完全反应时平均消耗该
溶液反应,测得恰好完全反应时平均消耗该 溶液的体积为18.50
溶液的体积为18.50 。(已知:
。(已知: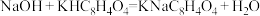 )
)(1)
 溶液需要经过标准溶液测定后方可确定其准确浓度(排除操作因素),原因可能是
溶液需要经过标准溶液测定后方可确定其准确浓度(排除操作因素),原因可能是(2)经测定,该
 溶液的浓度为
溶液的浓度为(3)该实验大约需要80
 0.1010
0.1010 的
的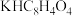 标准溶液。
标准溶液。①配制
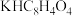 溶液时,不需要用到的仪器为
溶液时,不需要用到的仪器为
②配制该溶液过程中,下列操作可能引起所配溶液浓度偏高的是
a.容量瓶未干燥,含有少量蒸馏水 b.转移溶液时不慎有少量液体洒到容量瓶外面
c.溶液从烧杯转移到容量瓶后没有洗涤烧杯 d.定容时俯视刻度线
Ⅱ.欲配制250
 0.1
0.1 的稀盐酸,实验室的浓盐酸密度为1.25
的稀盐酸,实验室的浓盐酸密度为1.25 ,质量分数为36.5%。请回答下列问题:
,质量分数为36.5%。请回答下列问题:(4)需要量取浓盐酸的体积为
 。
。(5)配制该溶液的操作顺序是:D→
A.用30
 蒸馏水洗涤烧杯和玻璃棒各2~3次,将洗涤液全部注入容量瓶中并轻轻摇动
蒸馏水洗涤烧杯和玻璃棒各2~3次,将洗涤液全部注入容量瓶中并轻轻摇动B.将容量瓶盖紧,振满,摇匀
C.将已恢复至室温的盐酸沿玻璃棒注入所选用的容量瓶中
D.用量筒准确量取所需体积的浓盐酸,将其沿玻璃棒注入烧杯中,再向烧杯中加入少量蒸馏水(约30
 ),用玻璃棒慢慢搅动,使其混合均匀
),用玻璃棒慢慢搅动,使其混合均匀E.改用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶的刻度线相切
F.继续往容量瓶中小心地滴加蒸馏水,直到液面接近刻度线1~2
 处
处
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】现需配制0.1mol·L-1NaOH溶液480mL,根据此,回答下列问题:
(1)配制氢氧化钠溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、和___________________________________________ 。
(2)实验时需要托盘天平称量氢氧化钠____________ g;
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)__________ 。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液冷却室温后,沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,上下颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)配制0.1 mol· L-1NaOH溶液的实验中,如果出现以下操作,会导致配制溶液的浓度偏大的有___________ (填写字母)。
A.称量时用了生锈的砝码
B.未洗涤溶解NaOH的烧杯
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.容量瓶未干燥即用来配制溶液
E.定容时仰视刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(1)配制氢氧化钠溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、和
(2)实验时需要托盘天平称量氢氧化钠
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液冷却室温后,沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,上下颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)配制0.1 mol· L-1NaOH溶液的实验中,如果出现以下操作,会导致配制溶液的浓度偏大的有
A.称量时用了生锈的砝码
B.未洗涤溶解NaOH的烧杯
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.容量瓶未干燥即用来配制溶液
E.定容时仰视刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

(1)加入A试剂,是为了除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子。A代表的是多种试剂,按滴加顺序依次为:iNaOH,ⅱ__________ ,ⅲ_________ (填化学式)。
(2)请写出下列试剂加入试剂i时发生主要反应的离子反应方程式:_________
(3)右下图是某学生的过滤操作示意图,其操作不规范的是________ (填标号)。

a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)操作III的名称是__________
(5)mg粗盐提纯后得到ng纯净的NaCl固体,则m与n的大小关系为_________ .
A.m>n B. m=n C. m<n D. 无法确定.
(6)实验室需配制480 mL0.400mol/L盐酸,现用如图所示浓盐酸配制,回答下列问题:
①配制需要的玻璃仪器有玻璃棒、量筒、烧杯、________ (填仪器名称)
②需量取浓盐酸的体积为:__________ mL。(结果保留1位小数)

(1)加入A试剂,是为了除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子。A代表的是多种试剂,按滴加顺序依次为:iNaOH,ⅱ
(2)请写出下列试剂加入试剂i时发生主要反应的离子反应方程式:
(3)右下图是某学生的过滤操作示意图,其操作不规范的是

a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)操作III的名称是
(5)mg粗盐提纯后得到ng纯净的NaCl固体,则m与n的大小关系为
A.m>n B. m=n C. m<n D. 无法确定.
(6)实验室需配制480 mL0.400mol/L盐酸,现用如图所示浓盐酸配制,回答下列问题:
| 盐酸 分子式: HCl 相对分子质量: 36.5 密度: 1.2g/cm3 HCl的质量分数为: 36.5% |
①配制需要的玻璃仪器有玻璃棒、量筒、烧杯、
②需量取浓盐酸的体积为:
您最近一年使用:0次



