在两个锥形瓶内各盛有2g锌粒(颗粒大小基本相同),然后通过分液漏斗分别加入40mL1mol/L和40mL4mol/L的硫酸,装置如图。来比较以上两个反应的反应速率,下列说法正确的是
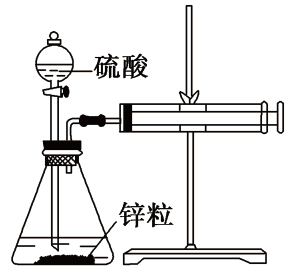

| A.锌粒和40mL1mol/L硫酸反应过程中,用Zn和H+表示该反应的反应速率的关系为v(Zn):v(H+)=1:2 |
| B.可以通过比较二者收集相同体积的H2所用的时间来比较两个反应的速率 |
| C.在相同条件下,1mol/L的硫酸与锌的反应速率更快 |
| D.该实验所需要的主要仪器就是以上装置中的仪器,不需要其它仪器 |
20-21高一下·湖北·阶段练习 查看更多[3]
湖北省重点高中智学联盟2020-2021学年高一下学期5月联考化学试题(已下线)第26练 化学反应速率-2023年高考化学一轮复习小题多维练(全国通用)第二章 化学反应速率与化学平衡 第一节 化学反应速率 第1课时 化学反应速率
更新时间:2021-06-07 15:18:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】工业上利用固体Ga与 高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol
高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol 时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
 高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol
高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol 时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
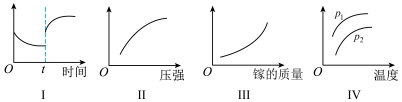
| A.I图像中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压 |
B.Ⅱ图像中纵坐标可以为 的百分含量 的百分含量 |
| C.Ⅲ图像中纵坐标可以为化学反应速率 |
D.Ⅳ图像中纵坐标可以为体系内混合气体平均相对分子质量,且 |
您最近一年使用:0次
【推荐2】下列实验设计可以达到目的是
| 实验目的 | 实验设计 | |
| A | 证明升温可以加快化学反应速率 | 两支试管(编号1、2)各盛 酸性 酸性 溶液,分别滴加 溶液,分别滴加 溶液,将1试管升温至 溶液,将1试管升温至 ,根据溶液褪色时间比较反应速率 ,根据溶液褪色时间比较反应速率 |
| B | 证明 和 和 之间的反应是可逆的 之间的反应是可逆的 | 向 溶液中加入 溶液中加入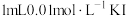 溶液,充分反应后,滴加 溶液,充分反应后,滴加 溶液,溶液变红色 溶液,溶液变红色 |
| C | 证明 比 比 更难溶 更难溶 | 向 浓度均为 浓度均为 的 的 与 与 混合溶液中滴加2滴 混合溶液中滴加2滴 的 的 溶液,只有黑色沉淀生成 溶液,只有黑色沉淀生成 |
| D | 证明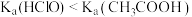 | 用 计分别测饱和 计分别测饱和 和 和 溶液的 溶液的 ,前者 ,前者 大 大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关实验的操作、现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向浓度均为0.10mol/L的KCl和KI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 向FeCl3+3KSCN Fe(SCN)3+3KCl的溶液平衡体系中加入少量KCl固体 Fe(SCN)3+3KCl的溶液平衡体系中加入少量KCl固体 | 溶液血红色变浅 | 增大生成物浓度,平衡逆向移动 |
| C | 分别向4mL 0.1mol/L、4mL 0.2mol/L的KMnO4酸性溶液中加入2mL 0.1mol/L H2C2O4溶液,记录溶液褪色所需时间 | 0.2mol/L的KMnO4酸性溶液褪色更快 | 反应物的浓度越大,反应速率越快 |
| D | 测定等物质的量浓度的Na2CO3和NaClO的pH | Na2CO3>NaClO | 酸性:H2CO3<HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】为比较 Fe3+和 Cu2+对 H2O2分解反应的催化效果, 甲、乙两位同学分别设计了如图甲、乙所示的实验。下列说法不正确的是( )


| A.图甲所示实验可通过观察气泡产生的快慢来比较反应速率的大小 |
| B.若图甲实验中反应速率① > ②,则可说明Fe3+比Cu2+对 H2O2分解反应的催化效果好 |
| C.用图乙所示装置测定反应速率,放置药品前需检验装置气密性。具体操作为:关闭活塞 A, 然后拉动注射器活塞。一段时间后松开活塞,观察其是否能够恢复原位 |
| D.用图乙所示装置测定反应速率,可在锥形瓶中放置 H2O2溶液,分液漏斗中 Fe3+或 Cu2+溶液。测定并记录反应产生一定气体体积所需的时间 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A.可逆反应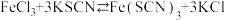 达到平衡后,加入 达到平衡后,加入 固体,逆反应速率加快 固体,逆反应速率加快 |
B.工业上合成 常选择500℃时进行而不是常温,是基于勒夏特列原理考虑的 常选择500℃时进行而不是常温,是基于勒夏特列原理考虑的 |
C.反应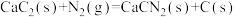 能自发进行,是因为 能自发进行,是因为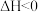 |
D.在装有2mL和1mL0.1mol/L 溶液的二支试管中,分别添加足量稀硫酸,观察浑浊产生的时间或产生气体的多少即可判断反应的快慢 溶液的二支试管中,分别添加足量稀硫酸,观察浑浊产生的时间或产生气体的多少即可判断反应的快慢 |
您最近一年使用:0次

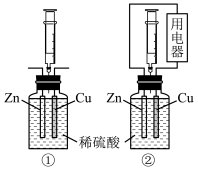


 均为负极,发生氧化反应
均为负极,发生氧化反应 内,生成气体的平均速率①>②
内,生成气体的平均速率①>②

