将硝酸表现出的性质填在下列各反应操作或现象后:
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)久置的浓硝酸变黄色___ 。
(2)用硝酸浸洗附有银的试管___ 。
(3)常温下用铁制或铝制容器贮存、运输浓HNO3___ 。
(4)用稀HNO3浸洗久置石灰水试剂瓶上的固体___ 。
(5)用Cu和稀HNO3制NO气体___ 。
(6)浓HNO3中滴入石蕊溶液并微热,石蕊溶液先变红后褪色___ 。
A.氧化性 B.酸性 C.还原性 D.不稳定性
(1)久置的浓硝酸变黄色
(2)用硝酸浸洗附有银的试管
(3)常温下用铁制或铝制容器贮存、运输浓HNO3
(4)用稀HNO3浸洗久置石灰水试剂瓶上的固体
(5)用Cu和稀HNO3制NO气体
(6)浓HNO3中滴入石蕊溶液并微热,石蕊溶液先变红后褪色
更新时间:2021-06-10 13:28:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室必备的重要试剂
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有___________ 性;硝酸应保存在棕色瓶中,这是因为硝酸具有___________ 性。
(2)如图是硫酸试剂瓶标签上的部分内容,该硫酸的浓度是___________ ;实验人员操作时不必需穿戴的安全用具是___________ 。
A.防护手套 B.实验服 C.防毒面具 D.护目镜
(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式___________ 。
(4)某同学向浸泡铜片的稀盐酸中加入 后,铜片溶解。写出该反应的化学方程式
后,铜片溶解。写出该反应的化学方程式___________ 。
实验室中向烧杯内加入约20g蔗糖,向其中插入玻璃棒,消加几滴蒸馏水,再加入适量浓硫酸。试回答下列问题:
(5)该实验除有刺激性气味的气体产生外,还可能有___________ 现象;
(6)将产生的气体通入品红溶液,红色褪去,判断该气体中含有___________ (写化学式),将产生气体先通过足量酸性高锰酸钾溶液,再通过澄清石灰水,石灰水变浑浊,判断该气体中还含有___________ (写化学式)
(7)实验结束吸收尾气应该选用的装置是___________ ,烧杯中盛放的试剂是___________ 。
A、 B、
B、 C、
C、
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
(2)如图是硫酸试剂瓶标签上的部分内容,该硫酸的浓度是
| 化学纯(CP)(500mL) 品名:硫酸 化学式:  相对分子质量:98 密度:  质量分数:98.9% |
A.防护手套 B.实验服 C.防毒面具 D.护目镜
(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式
(4)某同学向浸泡铜片的稀盐酸中加入
 后,铜片溶解。写出该反应的化学方程式
后,铜片溶解。写出该反应的化学方程式实验室中向烧杯内加入约20g蔗糖,向其中插入玻璃棒,消加几滴蒸馏水,再加入适量浓硫酸。试回答下列问题:
(5)该实验除有刺激性气味的气体产生外,还可能有
(6)将产生的气体通入品红溶液,红色褪去,判断该气体中含有
(7)实验结束吸收尾气应该选用的装置是
A、
 B、
B、 C、
C、
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列说法不正确的是____________________ 。
A.用100mL的容量瓶准确量取100mL液体
B.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
C.用托盘天平称量NaCl时,NaCl放在纸上;称量NaOH时,NaOH放在小烧杯里
D.用加热的方法提取NH4C1固体中含有的少量碘单质
E.浓硝酸与浓盐酸均易挥发,故都必须保存在棕色试剂瓶中,并置于阴凉处
A.用100mL的容量瓶准确量取100mL液体
B.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
C.用托盘天平称量NaCl时,NaCl放在纸上;称量NaOH时,NaOH放在小烧杯里
D.用加热的方法提取NH4C1固体中含有的少量碘单质
E.浓硝酸与浓盐酸均易挥发,故都必须保存在棕色试剂瓶中,并置于阴凉处
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式:______ 。
H2PO2-+Ag+=PO43-+Ag+。
由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下:

(2)关于除砷条件的说法合理的是_______ (填字母)。
a. 75℃使白磷熔化,并溶于水b.硝酸浓度不易过大,防止白磷反应
c.温度不宜过高,防止硝酸分解d.适当提高温度,加快化学反应速率
(3)硝酸氧化除砷时被还原为NO,氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越____ (填“多”或“少”)。
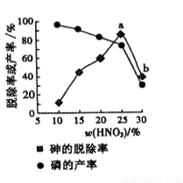
(4)某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是__________________ 。
(1)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式:
H2PO2-+Ag+=PO43-+Ag+。
由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下:

(2)关于除砷条件的说法合理的是
a. 75℃使白磷熔化,并溶于水b.硝酸浓度不易过大,防止白磷反应
c.温度不宜过高,防止硝酸分解d.适当提高温度,加快化学反应速率
(3)硝酸氧化除砷时被还原为NO,氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越
(4)某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式:______ 。
H2PO2-+Ag+=PO43-+Ag+。
由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下:

(2)关于除砷条件的说法合理的是_______ (填字母)。
a. 75℃使白磷熔化,并溶于水b.硝酸浓度不易过大,防止白磷反应
c.温度不宜过高,防止硝酸分解d.适当提高温度,加快化学反应速率
(3)硝酸氧化除砷时被还原为NO,氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越____ (填“多”或“少”)。
(4)某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是__________________ 。

(1)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式:
H2PO2-+Ag+=PO43-+Ag+。
由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下:

(2)关于除砷条件的说法合理的是
a. 75℃使白磷熔化,并溶于水b.硝酸浓度不易过大,防止白磷反应
c.温度不宜过高,防止硝酸分解d.适当提高温度,加快化学反应速率
(3)硝酸氧化除砷时被还原为NO,氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越
(4)某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁及其化合物在工业上用途广泛。部分含铁物质的分类与相应铁元素的化合价关系如图所示。回答下列问题:

(1)在高温条件下,Al粉可与a的粉末反应。写出该反应的一个用途______ 。
(2)电子工业中,人们常用b的溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。该反应的离子方程式为______ ,设计实验证明腐蚀后的废液中含有b的阳离子:______ 。
(3)工业上可以用c制造的容器盛放冷的浓硝酸,体现了浓硝酸的______ 性;在加热条件下二者可剧烈反应,c与足量浓硝酸在加热条件下反应的化学方程式为______ 。
(4)d为K2FeO4,是一种新型、高效的水处理剂。已知湿法制备它的体系中参加反应的六种微粒为:d的阴离子、e、H2O、 、
、 、
、 。该反应的离子方程式为
。该反应的离子方程式为______ 。若要制备0.2mol ,理论上需要
,理论上需要______ gNaClO。

(1)在高温条件下,Al粉可与a的粉末反应。写出该反应的一个用途
(2)电子工业中,人们常用b的溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。该反应的离子方程式为
(3)工业上可以用c制造的容器盛放冷的浓硝酸,体现了浓硝酸的
(4)d为K2FeO4,是一种新型、高效的水处理剂。已知湿法制备它的体系中参加反应的六种微粒为:d的阴离子、e、H2O、
 、
、 、
、 。该反应的离子方程式为
。该反应的离子方程式为 ,理论上需要
,理论上需要
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下图为氮及其化合物的类别与化合价对应的关系图。

(1)实验室制取氨气。
① 化学方程式是_______ 。
② 可用向下排空气法收集氨气的原因是_______ 。
③ 用水吸收多余的氨气时,如将导管直接插入水中,
会产生倒吸现象,产生该现象的原因是_______ 。
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:
a. 汽车尾气中产生的NO:N2 + O2 2NO。
2NO。
b. 氨的催化氧化:_________ 。
② 体现N元素的氧化性:_________ 。
(3)NO2 易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。

① NO2溶于水的化学方程式是_________ 。
② 使试管中NO2完全被水吸收的操作是________ 。

(1)实验室制取氨气。
① 化学方程式是
② 可用向下排空气法收集氨气的原因是
③ 用水吸收多余的氨气时,如将导管直接插入水中,
会产生倒吸现象,产生该现象的原因是
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:
a. 汽车尾气中产生的NO:N2 + O2
 2NO。
2NO。b. 氨的催化氧化:
② 体现N元素的氧化性:
(3)NO2 易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。

① NO2溶于水的化学方程式是
② 使试管中NO2完全被水吸收的操作是
您最近一年使用:0次



