下图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号
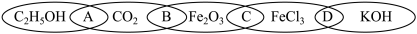
(1)相连的两种物质都是电解质的是___________ (填分类标准代号,下同)都是氧化物的是___________
(2)图中相连的两种物质能够相互反应的是___________ ,所属基本反应类型的是___________ 反应。
(3)用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,得到的分散系称为___________ ,证明该分散系生成的实验原理是___________ (用离子方程式表示)。
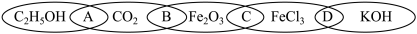
(1)相连的两种物质都是电解质的是
(2)图中相连的两种物质能够相互反应的是
(3)用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,得到的分散系称为
更新时间:2021-09-07 00:12:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】古代道家炼制外丹常用的八种石质原料如下:丹砂(HgS)、雄黄(As4S4)、云母[KAl2(AISi3O10)(OH)2]、空青[Cu2(OH)2CO3]、硫黄、戌盐(NaCl)、硝石(KNO3)、雌黄(As2S3)。回答下列问题:
(1)属于易溶于水的盐类是_______ (填化学式)。
(2)根据Mg2SiO4氧化物形式:2MgO·SiO2。写出云母的氧化物形式:_______ 。
(3)硫黄、硝石及木炭为黑火药成分,爆炸反应为2KNO3+S+3C K2S+N2↑+3CO2↑。该反应氧化剂为
K2S+N2↑+3CO2↑。该反应氧化剂为_______ ,每消耗1molKNO3该反应转移_______ 个电子。
(4)空青与硫酸反应可得胆矾,该反应的离子方程式为_______ 。
(1)属于易溶于水的盐类是
(2)根据Mg2SiO4氧化物形式:2MgO·SiO2。写出云母的氧化物形式:
(3)硫黄、硝石及木炭为黑火药成分,爆炸反应为2KNO3+S+3C
 K2S+N2↑+3CO2↑。该反应氧化剂为
K2S+N2↑+3CO2↑。该反应氧化剂为(4)空青与硫酸反应可得胆矾,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】次磷酸钙可用作阻燃剂,其化学式为 ,是一种正盐。实验室制备方法:在烧瓶中加入次磷酸钠溶液,水浴60℃中缓慢滴加氯化钙溶液,经过滤,再真空干燥可得次磷酸钙。
,是一种正盐。实验室制备方法:在烧瓶中加入次磷酸钠溶液,水浴60℃中缓慢滴加氯化钙溶液,经过滤,再真空干燥可得次磷酸钙。
 是
是___________ 元酸,推断理由:___________ 。上述制备次磷酸钙的化学方程式:___________ 。
 ,是一种正盐。实验室制备方法:在烧瓶中加入次磷酸钠溶液,水浴60℃中缓慢滴加氯化钙溶液,经过滤,再真空干燥可得次磷酸钙。
,是一种正盐。实验室制备方法:在烧瓶中加入次磷酸钠溶液,水浴60℃中缓慢滴加氯化钙溶液,经过滤,再真空干燥可得次磷酸钙。 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】分类法有助于人们发现和预测物质的性质,在化学学习中,科学的分类方法几乎是无可替代的。 下列物质:①稀硫酸;②硝酸钾溶液;③铜;④Na2O固体;⑤Ba(OH)2固体;⑥K2CO3固体;⑦二氧化碳;⑧熔融KHSO4;⑨NaCl固体;⑩氨气;
(1)能导电的是_______ (填序号,下同),属于电解质的是_______ ,属于非电解质的是_______ 。
(2)写出⑤、⑥在水溶液中的电离方程式:
⑤_______ ,⑥_______ 。
(3)从物质的组成看KNO3、K2CO3、KHSO4都属于钾盐,其分类标准是:_______ ;
检验⑨中阴离子的实验方法是_______ 。
(1)能导电的是
(2)写出⑤、⑥在水溶液中的电离方程式:
⑤
(3)从物质的组成看KNO3、K2CO3、KHSO4都属于钾盐,其分类标准是:
检验⑨中阴离子的实验方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)实验室中,制取Fe(OH)3胶体的操作是________ ,反应的化学方程式是_______ ,证明胶体已经制成的方法是_______ 。
(2)已知Fe(OH)3胶粒带正电荷。Al(OH)3胶粒也带正电荷,而H2SiO3胶粒带负电荷,则下列实验的现象分别是:
①Fe(OH)3胶体和Al(OH)3胶体混合:_______ ;
②Fe(OH)3胶体和H2SiO3胶体混合:_______ 。
(3)已知Al(OH)3胶体能够净水,则Fe(OH)3胶体_______ (填“能”或“不能”)净水。
(1)实验室中,制取Fe(OH)3胶体的操作是
(2)已知Fe(OH)3胶粒带正电荷。Al(OH)3胶粒也带正电荷,而H2SiO3胶粒带负电荷,则下列实验的现象分别是:
①Fe(OH)3胶体和Al(OH)3胶体混合:
②Fe(OH)3胶体和H2SiO3胶体混合:
(3)已知Al(OH)3胶体能够净水,则Fe(OH)3胶体
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)现有下列物质:①小苏打② 晶体③
晶体③ ④
④ 溶液⑤液态的
溶液⑤液态的 ⑥酒精(
⑥酒精( )⑦铜。上述物质中:能导电的是
)⑦铜。上述物质中:能导电的是_______ (填序号,下同);属于酸性氧化物的是_______ 。属于电解质的是_______ 。溶于水后形成的水溶液不能导电的是_______ 。
(2)同学们吃的食品包装袋中经常有一个小纸袋,上面写着“干燥剂”, 其主要成分是生石灰( )。
)。
①生石灰属于哪类氧化物:_______ 。
②生石灰可作干燥剂的理由是(用化学方程式表示)_______ 。
(3)某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。①现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,其中正确的是_______ (填序号)。
a.甲同学的操作:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
b.乙直接加热饱和氯化铁溶液;
c.丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
②制备氢氧化铁胶体的化学方程式是_______ 。
③证明有氢氧化铁胶体生成的实验操作是_______ 。
(1)现有下列物质:①小苏打②
 晶体③
晶体③ ④
④ 溶液⑤液态的
溶液⑤液态的 ⑥酒精(
⑥酒精( )⑦铜。上述物质中:能导电的是
)⑦铜。上述物质中:能导电的是(2)同学们吃的食品包装袋中经常有一个小纸袋,上面写着“干燥剂”, 其主要成分是生石灰(
 )。
)。①生石灰属于哪类氧化物:
②生石灰可作干燥剂的理由是(用化学方程式表示)
(3)某课外活动小组进行氢氧化铁胶体的制备实验并检验其性质。①现有甲、乙、丙三名同学进行氢氧化铁胶体的制备实验,其中正确的是
a.甲同学的操作:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至混合液呈红褐色,停止加热;
b.乙直接加热饱和氯化铁溶液;
c.丙向沸水中滴加饱和氯化铁溶液,为了使反应进行充分,煮沸10分钟;
②制备氢氧化铁胶体的化学方程式是
③证明有氢氧化铁胶体生成的实验操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物在生产、生活中有及其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是_________ ,分散剂是___________ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是_______
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果.由饱和FeCl3溶液制备Fe(OH)3胶体的方法是______________________ 。离子方程式是___________________________ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是__________ 。
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是_________
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠有多种方法,其中一种方法的原理可用离子方程式表示为
3ClO—+2Fe3++10OH—= 2 +3Cl—+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl—+5H2O,则Na2FeO4中铁元素的化合价为_______ ,该离子反应中氧化剂与还原剂的个数比为_____ ,生成1个高铁酸钠转移____ 个电子
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果.由饱和FeCl3溶液制备Fe(OH)3胶体的方法是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠有多种方法,其中一种方法的原理可用离子方程式表示为
3ClO—+2Fe3++10OH—= 2
 +3Cl—+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl—+5H2O,则Na2FeO4中铁元素的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有下列物质:
①烧碱固体;②铜丝;③NH3;④稀硫酸;⑤二氧化碳气体;⑥食盐水;⑦碳酸钠粉末;⑧酒精;⑨熔融氯化钠;⑩胆矾。
请用序号填空:
(1)属于电解质的是___________ ;
(2)属于非电解质的是___________ ;
(3)属于电解质,但在上述状态下不能导电的是___________ 。
(4)写出下列物质在水溶液中的电离方程式:
H2SO4:___________ ;
Ca(OH)2:___________ ;
NH4NO3:___________ ;
KAl(SO4)2:___________ 。
①烧碱固体;②铜丝;③NH3;④稀硫酸;⑤二氧化碳气体;⑥食盐水;⑦碳酸钠粉末;⑧酒精;⑨熔融氯化钠;⑩胆矾。
请用序号填空:
(1)属于电解质的是
(2)属于非电解质的是
(3)属于电解质,但在上述状态下不能导电的是
(4)写出下列物质在水溶液中的电离方程式:
H2SO4:
Ca(OH)2:
NH4NO3:
KAl(SO4)2:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)现有以下物质①NaCl溶液 ②CO2 ③铜 ④BaSO4固体 ⑤蔗糖 ⑥酒精⑦熔融的KNO3,其中属于电解质的是 _____ (填上序号), 属于电解且能够导电的是 _____ (填上序号)。
(2)写出下列电解质在水中的电离方程式:①硝酸铜_______________ ;② H2SO4_____________________________ 。
(3)你想过复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合。如反应“BaCl2+Na2SO4=BaSO4↓+2NaCl”中,实际参加反应的离子是Ba2+和SO42-,而Cl-、Na+则是“旁观者”,并没有参加反应。请你分析:反应“K2CO3+2HCl=2KCl+CO2↑+H2O”中实际参加反应的离子是:_________________ 。
(4)写出一个与离子方程式2H++CaCO3 =Ca2+ +CO2↑+H2O 相对应的反应化学方程式:_____________ 。
(2)写出下列电解质在水中的电离方程式:①硝酸铜
(3)你想过复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合。如反应“BaCl2+Na2SO4=BaSO4↓+2NaCl”中,实际参加反应的离子是Ba2+和SO42-,而Cl-、Na+则是“旁观者”,并没有参加反应。请你分析:反应“K2CO3+2HCl=2KCl+CO2↑+H2O”中实际参加反应的离子是:
(4)写出一个与离子方程式2H++CaCO3 =Ca2+ +CO2↑+H2O 相对应的反应化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学上用分类法学习化学物质的共性,用比较法学习化学物质的特性,物质的氧化性与还原性尤为重要,回答下列问题:
(1)磷元素的含氧酸有H3PO4、H3PO3(亚磷酸)、H3PO2(次磷酸)等多种,其中已知H3PO3+2NaOH(过量)=Na2HPO3+2H2O。
H3PO3属于________ (选填“一”“二”或“三”)元酸。
NaH2PO3属于_______ (填“正盐”或“酸式盐”)。
H3PO2可将溶液中的Ag+转化为银,自身变为H3PO4,可用于化学镀银。
利用H3PO2进行化学镀银的反应中,氧化剂与还原剂的个数比为________ 。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:_______ 。
_______Fe(OH)3+______CH4+______H+ _____Fe2++______HCO
_____Fe2++______HCO +________。
+________。
(3)强酸反应体系中发生的一个离子反应中,反应物和生成物共六种微粒:Fe2+、NO 、Fe3+、NH
、Fe3+、NH 和H2O,写出该反应的离子方程式
和H2O,写出该反应的离子方程式_______ 。
(4)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1个NaBH4的还原能力相当于_____ 个H2的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同)。
(1)磷元素的含氧酸有H3PO4、H3PO3(亚磷酸)、H3PO2(次磷酸)等多种,其中已知H3PO3+2NaOH(过量)=Na2HPO3+2H2O。
H3PO3属于
NaH2PO3属于
H3PO2可将溶液中的Ag+转化为银,自身变为H3PO4,可用于化学镀银。
利用H3PO2进行化学镀银的反应中,氧化剂与还原剂的个数比为
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:
_______Fe(OH)3+______CH4+______H+
 _____Fe2++______HCO
_____Fe2++______HCO +________。
+________。(3)强酸反应体系中发生的一个离子反应中,反应物和生成物共六种微粒:Fe2+、NO
 、Fe3+、NH
、Fe3+、NH 和H2O,写出该反应的离子方程式
和H2O,写出该反应的离子方程式(4)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1个NaBH4的还原能力相当于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】分类是化学学习与研究的常用方法。请回答下列问题:
(1)根据____________ 将分散系分为溶液、胶体和浊液;鉴别胶体和溶液的常用方法是____ ;向新制的Fe(OH)3胶体中滴加稀硫酸,现象为先出现棕红色沉淀,后沉淀消失,原因为_____ 。
(2)现有物质:①铁 ②氨气 ③熔融氯化钠 ④硫酸 ⑤醋酸 ⑥氢氧化钾 ⑦漂白粉⑧蔗糖 上述物质中属于非电解质的是_________ (填序号);既是电解质又是强电解质的是_____ (填序号)。
(3)熟练掌握不同类别物质间的相互转化具有重要意义。
①写出由碳酸钠转化为氢氧化钠的化学方程式______________ ;
②若用M表示金属活动顺序表中排在H前的金属,金属M与稀硫酸反应的离子方程式为_______ ;
③钠在空气中燃烧的化学方程式为___________ ;若46 g钠与0.8 mol O2恰好完全反应,则Na2O和Na2O2的物质的量之比为_______ 。
(1)根据
(2)现有物质:①铁 ②氨气 ③熔融氯化钠 ④硫酸 ⑤醋酸 ⑥氢氧化钾 ⑦漂白粉⑧蔗糖 上述物质中属于非电解质的是
(3)熟练掌握不同类别物质间的相互转化具有重要意义。
①写出由碳酸钠转化为氢氧化钠的化学方程式
②若用M表示金属活动顺序表中排在H前的金属,金属M与稀硫酸反应的离子方程式为
③钠在空气中燃烧的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C、D为四种可溶性的盐,它们的阳离子分别是 ,
, ,
, ,
, 中的一种,阴离子分别是
中的一种,阴离子分别是 ,
, 、
、 、
、 中的一种。(离子在物质中不能重复出现)
中的一种。(离子在物质中不能重复出现)
a.若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
b.若向a的四支试管中分别加入盐酸,B盐的溶液有无色无味的气体逸出,D盐的溶液有沉淀生成。
根据a、b实验事实可推断:
(1)写出下列物质的化学式:A___________ ;D___________ 。
(2)写出上述可溶性盐C与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
 ,
, ,
, ,
, 中的一种,阴离子分别是
中的一种,阴离子分别是 ,
, 、
、 、
、 中的一种。(离子在物质中不能重复出现)
中的一种。(离子在物质中不能重复出现)a.若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
b.若向a的四支试管中分别加入盐酸,B盐的溶液有无色无味的气体逸出,D盐的溶液有沉淀生成。
根据a、b实验事实可推断:
(1)写出下列物质的化学式:A
(2)写出上述可溶性盐C与
 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次



