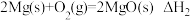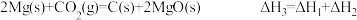燃烧1 g乙炔( C2H2)生成二氧化碳和液态水,放出热量50 kJ,则这一反应的热化学反应方程式为
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=+50 kJ·mol-1 |
| B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l) ΔH=-1 300 kJ |
| C.2C2H2+5O2=4CO2+2H2O ΔH=-2 600 kJ·mol-1 |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-2 600 kJ·mol-1 |
更新时间:2021-11-04 14:42:47
|
【知识点】 热化学方程式书写及正误判断解读
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列说法中正确的是( )
A.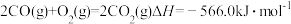 则 则 标准燃烧热为 标准燃烧热为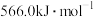 |
B.甲烷的燃烧热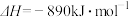 则在甲烷燃料电池中当有 则在甲烷燃料电池中当有 甲烷参与反应放出热量为 甲烷参与反应放出热量为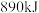 |
C.在一定条件下将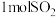 和 和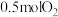 置于密闭容器中充分反应,放出热量 置于密闭容器中充分反应,放出热量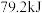 ,则反应的热化学方程式为 ,则反应的热化学方程式为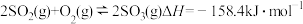 |
D.已知稀溶液中,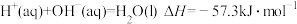 ,但稀醋酸与稀氢氧化钠溶液反应生成 ,但稀醋酸与稀氢氧化钠溶液反应生成 水时放出的热量小于 水时放出的热量小于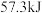 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知断开1molH2(g)中H-H键需要吸收436kJ能量,根据能量变化示意图,下列说法或热化学方程式不正确的是( )
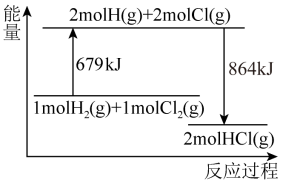

| A.断开1molHCl(g)中H-Cl键要吸收432kJ能量 |
| B.生成1molCl2(g)中的Cl-Cl键放出243kJ能量 |
| C.HCl(g)→1/2H2(g)+1/2Cl2(g)-92.5kJ |
| D.H2(g)+Cl2(g)→2HCl(g)+864kJ |
您最近一年使用:0次

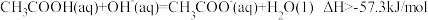

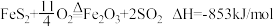
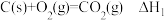 ,
,