现有以下物质:① 溶液;②液氨;③
溶液;②液氨;③ 固体;④
固体;④ ;⑤
;⑤ 胶体;⑥铜;⑦
胶体;⑥铜;⑦ ;⑧稀醋酸。
;⑧稀醋酸。
(1)物质中属于电解质的是_________________ 。(填序号)
(2)写出①和⑧的水溶液反应的离子方程式:__________________________ 。
(3)写出④在水溶液中的电离方程式:________________________ 。
(4)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为____________________ 。
(5)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈_______ 色,即制得 胶体。写出制备物质⑤的化学方程式:
胶体。写出制备物质⑤的化学方程式:_____________________________________ 。
 溶液;②液氨;③
溶液;②液氨;③ 固体;④
固体;④ ;⑤
;⑤ 胶体;⑥铜;⑦
胶体;⑥铜;⑦ ;⑧稀醋酸。
;⑧稀醋酸。(1)物质中属于电解质的是
(2)写出①和⑧的水溶液反应的离子方程式:
(3)写出④在水溶液中的电离方程式:
(4)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为
(5)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。写出制备物质⑤的化学方程式:
胶体。写出制备物质⑤的化学方程式:
更新时间:2021-11-12 10:28:23
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】FeCl3是实验室常见的药品,将少量FeCl3饱和溶液分别滴加到下列物质中,可得到三种分散系。

回答下列问题:
(1)可判断丙中成功制备胶体的是_________
(2)关于分散系的下列说法中,正确的是_________
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为___________ 。
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带___________ 电荷;将丁与丙混合,可观察到___________ 现象。
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是___________ 。

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从___________ (填a或b)口通入,该装置使用水浴加热的优点是___________ ,最后晶态碘在___________ 里聚集(填仪器名称)。


回答下列问题:
(1)可判断丙中成功制备胶体的是_________
| A.布朗运动 | B.丁达尔现象 |
| C.形成分散系 | D.形成澄清透明的液体 |
(2)关于分散系的下列说法中,正确的是_________
| A.分散系一定是混合物 | B.分散剂一定是液体 |
| C.一种分散系里只能有一种分散质 | D.胆矾、空气、有色玻璃都是分散系 |
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
| A.溴的四氯化碳溶液(分液) |
| B.淀粉和水(过滤) |
| C.KCl和MnO2(溶解过滤,再蒸发结晶) |
| D.碘和蒸馏水(萃取) |
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】定性和定量是中学化学研究物质性质、组成的常用方法。胶体是一种重要的分散系(三种分散系分散质粒子大小如图示)。
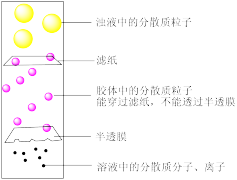
某兴趣小组按如下实验步骤制备Cu(OH)2胶体:用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中慢慢加入数滴浓CuCl2溶液,得到蓝色透明的液体。制备原理用化学方程式表示为:CuCl2+2H2O(沸水)=Cu(OH)2(胶体)+2HCl。
(1)Cu(OH)2胶体中分散质微粒直径范围是_____ 。
(2)Cu(OH)2浊液与Cu(OH)2胶体性质不同,本质原因是_____ 。
(3)下列哪种用于判断胶体制备成功的方法最简单_____ 。
(4)实验过程中,有一位同学向烧杯中一次性加入大量CuCl2溶液,结果没有制得胶体,反而出现了浑浊,请分析他实验失败的原因_____ 。

某兴趣小组按如下实验步骤制备Cu(OH)2胶体:用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中慢慢加入数滴浓CuCl2溶液,得到蓝色透明的液体。制备原理用化学方程式表示为:CuCl2+2H2O(沸水)=Cu(OH)2(胶体)+2HCl。
(1)Cu(OH)2胶体中分散质微粒直径范围是
| A.小于1nm | B.1~10nm | C.1~100 | D.大于100nm |
| A.分散剂的种类不同 | B.颜色和透明程度不同 |
| C.分散质粒子的大小不同 | D.分散质粒子所带电荷不同 |
| A.丁达尔现象 | B.半透膜实验 | C.聚沉 | D.电泳 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)①食盐晶体②乙醇③水银④蔗糖⑤KNO3溶液⑥熔融的氢氧化钠⑦SO2⑧液态氯化氢。以上物质能导电的是:_______ (填序号,下同)。以上物质属于电解质的是:_______ 。以上物质属于非电解质的是:_______ 。
(2)把淀粉溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是_______ 。
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:_______ ;继续滴加稀硫酸至过量可观察到的现象是_______ ,写出上述反应的化学方程式_______ 。
(1)①食盐晶体②乙醇③水银④蔗糖⑤KNO3溶液⑥熔融的氢氧化钠⑦SO2⑧液态氯化氢。以上物质能导电的是:
(2)把淀粉溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】现有物质:① ②
② ③
③ ④
④ 胶体 ⑤酒精 ⑥
胶体 ⑤酒精 ⑥ ⑦
⑦ 。回答下列问题:
。回答下列问题:
(1)其中属于非电解质的是___________ (填序号)。
(2)②与⑦的浓溶液反应会产生大量气体,气体的主要成分有___________ (填化学式)。
(3)写出③的电离方程式:___________ 。
(4)提纯④的方法为___________ (填名称)。
(5)在实验室中检验气体⑥常用的试剂是___________ 。
 ②
② ③
③ ④
④ 胶体 ⑤酒精 ⑥
胶体 ⑤酒精 ⑥ ⑦
⑦ 。回答下列问题:
。回答下列问题:(1)其中属于非电解质的是
(2)②与⑦的浓溶液反应会产生大量气体,气体的主要成分有
(3)写出③的电离方程式:
(4)提纯④的方法为
(5)在实验室中检验气体⑥常用的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有下列物质:①熔化的NaCl;②盐酸;③氯气;④冰醋酸;⑤铜;⑥酒精;⑦硫酸氢钠晶体;⑧液氨;⑨ 。请按要求回答下列问题。
。请按要求回答下列问题。
(1)属于强电解质的是_______ (填序号,下同)。
(2)在上述状态下能导电的是_______ 。
(3)属于非电解质,但溶于水后的水溶液能导电的是_______ 。
(4)可以证明④是弱酸的事实是_______(填标号)。
(5)有下列物质的溶液:a. ;b.
;b. ;c.
;c. ;d.
;d. 。若四种溶液的
。若四种溶液的 相同,则四种物质的物质的量浓度由大到小的顺序为
相同,则四种物质的物质的量浓度由大到小的顺序为_______ 。
(6)常温下,有 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图,正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图,正确的是_______ (填标号)。(其中①表示盐酸,②表示醋酸)
a.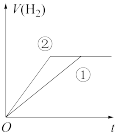 b.
b.
c. d.
d.
 。请按要求回答下列问题。
。请按要求回答下列问题。(1)属于强电解质的是
(2)在上述状态下能导电的是
(3)属于非电解质,但溶于水后的水溶液能导电的是
(4)可以证明④是弱酸的事实是_______(填标号)。
| A.乙酸和水能以任意比例混溶 |
| B.在乙酸水溶液中含有未电离的乙酸分子 |
C.乙酸与 溶液反应放出 溶液反应放出 气体 气体 |
| D.1mol/L的乙酸水溶液能使紫色石蕊溶液变红色 |
 ;b.
;b. ;c.
;c. ;d.
;d. 。若四种溶液的
。若四种溶液的 相同,则四种物质的物质的量浓度由大到小的顺序为
相同,则四种物质的物质的量浓度由大到小的顺序为(6)常温下,有
 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图,正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图,正确的是a.
 b.
b.
c.
 d.
d.
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】电离方程式的书写
(1)强电解质:书写强电解质的电离方程式时用“_______ ”,例如,氯化钠的电离方程式为_______ 。
(2)弱电解质:书写弱电解质的电离方程式时用“_______ ”,例如,醋酸和一水合氨的电离方程式分别为_______ 。
(1)强电解质:书写强电解质的电离方程式时用“
(2)弱电解质:书写弱电解质的电离方程式时用“
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)下列物质能导电且属于电解质的是_______(填序号)。
(2)写出下列物质在水溶液中的电离方程式:
① :
:_______ ;
② :
: _______ ;
③ :
:_______ ;
④NaHCO3 :_______ ;
(1)下列物质能导电且属于电解质的是_______(填序号)。
A.固态氯化镁( ) ) | B.熔融态氯化镁( ) ) |
| C.氯化钠溶液 | D.铝 |
①
 :
:②
 :
: ③
 :
:④NaHCO3 :
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出金属钠与硫酸铜溶液反应的离子方程式:______________________ .
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】通常用小苏打的悬浊液除去CO2中的HCl,反应的离子方程式为:_________ ,不能用NaOH溶液的原因是__________ (用离子方程式表示原因)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表
每组分类均有错误,其错误的物质分别是第一组___________ 、第二组___________ (填化学式)。
(2)一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
①该变化的基本反应类型是___________ 反应;
②物质Q在反应中可能起的作用是___________ 。
(3)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸(H3PO2)是___________ 元酸(填“一”、“二”或“三”)。
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO 恰好沉淀完全,请写出发生反应的离子方程式:
恰好沉淀完全,请写出发生反应的离子方程式:___________ 。
(5)已知反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,若该反应生成50个氯气分子,则转移的电子为___________ 个。
(1)下列是某同学对有关物质进行分类的列表
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | CO |
每组分类均有错误,其错误的物质分别是第一组
(2)一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
| 物质 | M | N | Q | P |
| 反应前质量/g | 50 | 1 | 3 | 12 |
| 反应后质量/g | x | 26 | 3 | 30 |
①该变化的基本反应类型是
②物质Q在反应中可能起的作用是
(3)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸(H3PO2)是
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO
 恰好沉淀完全,请写出发生反应的离子方程式:
恰好沉淀完全,请写出发生反应的离子方程式:(5)已知反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,若该反应生成50个氯气分子,则转移的电子为
您最近一年使用:0次



