能源是现代社会发展的支柱之一、
(1)下列反应中,属于放热反应的是___________ (填序号)。
a.Ba(OH)2•8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(2)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式___________ 。
(3)1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,此反应的热化学方程式为___________
(4)已知白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程式分别为:P4(s)+5O2(g)=P4O10(s);ΔH=-24.08kJ/g(表示1g白磷固体燃烧生成P4O10固体放热24.08kJ,下同);P(s)+5/4O2(g)=1/4P4O10(s);ΔH=-23.84kJ/g。1mol白磷转化为红磷时___________ (释放、吸收)___________ kJ的热量。
(1)下列反应中,属于放热反应的是
a.Ba(OH)2•8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(2)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式
(3)1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,此反应的热化学方程式为
(4)已知白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程式分别为:P4(s)+5O2(g)=P4O10(s);ΔH=-24.08kJ/g(表示1g白磷固体燃烧生成P4O10固体放热24.08kJ,下同);P(s)+5/4O2(g)=1/4P4O10(s);ΔH=-23.84kJ/g。1mol白磷转化为红磷时
21-22高二上·山西临汾·期中 查看更多[3]
山西省侯马市第一中学校2021-2022年高二上学期期中测试化学试题(已下线)1.1.2 热化学方程式 燃烧热-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)海南省海口嘉勋高级中学2022-2023学年高二上学期10月检测化学试题
更新时间:2021-12-03 20:44:23
|
相似题推荐
填空题
|
容易
(0.94)
名校
【推荐1】(1)3 mol 甲烷燃烧时,生成液态水和二氧化碳,同时放出 2670.9 kJ 的热量,写出该反应的热化学方程式_____________________________ 。
(2)H2SO4和 NaOH 的稀溶液反应生成 1mol 液态水时放出 57.3 kJ 的热量,写出该反应的热化学方程式_______________________ 。
(2)H2SO4和 NaOH 的稀溶液反应生成 1mol 液态水时放出 57.3 kJ 的热量,写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】根据下列叙述写出相应的热化学方程式:
(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应燃烧的热化学方程式是
____________________________________________________
(2)如图是298 K时N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为:_________________________________ 。
(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应燃烧的热化学方程式是
(2)如图是298 K时N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为:

您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】依据下列信息,完成填空:
(1)同温同压下, ,在光照和点燃条件下的
,在光照和点燃条件下的 (化学计量数相同)分别为
(化学计量数相同)分别为 、
、 ,则
,则
___________ (填“>”、“<”或“=”) 。
。
(2)已知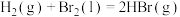
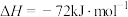 ,蒸发
,蒸发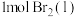 需要吸收的能量为
需要吸收的能量为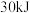 ,其他相关数据如表:
,其他相关数据如表:
则表中a=___________ 。
(3)已知稀溶液中, 与
与 恰好完全反应时,放出
恰好完全反应时,放出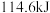 热量,写出表示
热量,写出表示 与
与 反应的中和热的热化学方程式
反应的中和热的热化学方程式___________ 。
(4)用如图所示的装置进行中和热的测定。烧杯间填满碎泡沬塑料的主要作用是___________ 。

(1)同温同压下,
 ,在光照和点燃条件下的
,在光照和点燃条件下的 (化学计量数相同)分别为
(化学计量数相同)分别为 、
、 ,则
,则
 。
。(2)已知
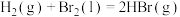
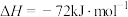 ,蒸发
,蒸发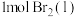 需要吸收的能量为
需要吸收的能量为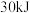 ,其他相关数据如表:
,其他相关数据如表:| 物质 |  |  | 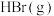 |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
(3)已知稀溶液中,
 与
与 恰好完全反应时,放出
恰好完全反应时,放出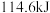 热量,写出表示
热量,写出表示 与
与 反应的中和热的热化学方程式
反应的中和热的热化学方程式(4)用如图所示的装置进行中和热的测定。烧杯间填满碎泡沬塑料的主要作用是

您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】中和热实验测定应当使用强酸、强碱的稀溶液,弱酸、弱碱在水溶液中不能完全电离,且电离过程是___________ 过程,(填“吸热”或“放热”,同下)使测得的反应热数值偏小;浓的强酸、强碱溶于水___________ ,使测得的反应热数值偏大。
您最近一年使用:0次
【推荐3】下列说法正确的是________ 。
①生成物能量一定低于反应物总能量
②放热反应的反应速率总是大于吸热反应的反应速率
③HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
④需要加热才能发生的反应一定是吸热反应
⑤1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
⑥依据盖斯定律,反应焓变的大小与反应的途径有关,无论是一步完成还是分几步完成,其总的热效应完全相同
⑦25 ℃、101kPa,1molS和2molS的燃烧热相等
⑧反应中旧键断裂需吸收能量,新键形成需放出能量,所以总能量不变
⑨化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
⑩由反应物X转化为Y和Z的能量变化 所示可知,由X→Z反应的ΔH<0
所示可知,由X→Z反应的ΔH<0
⑪由778 K时氮气与氢气合成氨反应过程中能量变化的曲线图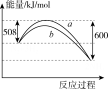 可知,b曲线是加入催化剂时的能量变化曲线
可知,b曲线是加入催化剂时的能量变化曲线
⑫1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
①生成物能量一定低于反应物总能量
②放热反应的反应速率总是大于吸热反应的反应速率
③HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
④需要加热才能发生的反应一定是吸热反应
⑤1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
⑥依据盖斯定律,反应焓变的大小与反应的途径有关,无论是一步完成还是分几步完成,其总的热效应完全相同
⑦25 ℃、101kPa,1molS和2molS的燃烧热相等
⑧反应中旧键断裂需吸收能量,新键形成需放出能量,所以总能量不变
⑨化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
⑩由反应物X转化为Y和Z的能量变化
 所示可知,由X→Z反应的ΔH<0
所示可知,由X→Z反应的ΔH<0⑪由778 K时氮气与氢气合成氨反应过程中能量变化的曲线图
 可知,b曲线是加入催化剂时的能量变化曲线
可知,b曲线是加入催化剂时的能量变化曲线⑫1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
您最近一年使用:0次

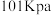 时,
时, 的燃烧热为
的燃烧热为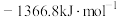 ,写出乙醇燃烧热的热化学方程式:
,写出乙醇燃烧热的热化学方程式:

