下表是元素周期表的一部分,请依据该表回答问题。
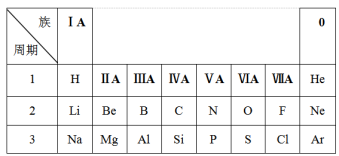
(1)第2周期VIIA族元素的原子结构示意图是___________ ,该元素与同周期IA族元素组成的化合物类型是___________ (填“离子化合物”或“共价化合物”)。
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是___________ (填化学式,下同);具有两性的是___________ 。加热时,碳单质能与S的最高价氧化物对应的水化物的浓溶液反应,写出该反应的化学方程式___________ 。
(3)下列判断正确的是___________(填标号)。

(1)第2周期VIIA族元素的原子结构示意图是
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是
(3)下列判断正确的是___________(填标号)。
| A.最低负化合价的绝对值:P>S |
| B.非金属性:P>N |
| C.离子半径:Mg2+>O2− |
| D.还原性:S2−>Cl− |
更新时间:2022-01-08 22:27:02
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,并回答下列问题:
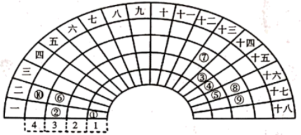
(1)元素②的名称为___________ ;元素⑩在常见周期表中的位置是___________ 。
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是___________ (填化学式,下同);元素④、⑧、⑨的最高价氧化物对应的水化物,酸性最强的是___________ 。
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应的化学方程式为___________ 。
(5)请设计简单实验,比较元素②、⑦的金属性强弱。

(1)元素②的名称为
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应的化学方程式为
(5)请设计简单实验,比较元素②、⑦的金属性强弱。
| 实验步骤 | 实验现象 | 实验结论 |
| 金属性:②>⑦ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)原子序数大于4的主族元素A和B的离子Am+和Bn-,它们的核外电子排布相同,则:
①A和B的质子数之差为_________________ (用m、n 表示)。
②B和A的族序数之差为_________________ (用含m、n的代数式表示)。
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为_____________________ ;
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为_____________ 。
①A和B的质子数之差为
②B和A的族序数之差为
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表短周期的一部分:
请按要求用化学用语回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为________________ ;
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:_____________________ ;
(3)用电子式表示元素④与元素⑥形成的化合物的形成过程____________ ;
(4)比元素⑦的原子序数多17的元素在周期表的位置为________________ ;
(5)写出由①④⑤三种元素组成的一种离子化合物的电子式_______________ ,若将其溶于水,破坏了其中的__________ (填“离子键”、“共价键”或“离子键和共价键”);
(6)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4 :1反应的离子方程式________ 。

请按要求用化学用语回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:
(3)用电子式表示元素④与元素⑥形成的化合物的形成过程
(4)比元素⑦的原子序数多17的元素在周期表的位置为
(5)写出由①④⑤三种元素组成的一种离子化合物的电子式
(6)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4 :1反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(8分)下表是元素周期表的一部分, 针对表中的①~⑥元素,填写下列空白:
(1)在这些元素中,化学性质最活泼的金属元素是:_______ (填具体元素符号)。
(2)元素②与⑥形成的BA型化合物所含的化学键类型为:______ 键。
(3)元素④的单质制造的器具不能盛装碱性溶液也不能盛装酸性溶液,请写出元素④的单质与氢氧化钠溶液反应的离子方程式:__________ 。
(4)设计实验证明:元素①比元素⑤的非金属性强:______ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 二 | ① | |||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ |
(1)在这些元素中,化学性质最活泼的金属元素是:
(2)元素②与⑥形成的BA型化合物所含的化学键类型为:
(3)元素④的单质制造的器具不能盛装碱性溶液也不能盛装酸性溶液,请写出元素④的单质与氢氧化钠溶液反应的离子方程式:
(4)设计实验证明:元素①比元素⑤的非金属性强:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下面是元素周期表的一部分,参照元素①~⑧在表中的位置,请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)___________ 。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)___________ 。
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:__________ 。
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:_____________ 。
(5)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为____________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(5)⑦单质与⑤的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:
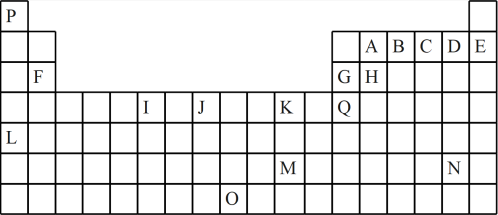
(1)I的最高化合价为____ ;K的元素名称为____ 。
(2)基态时G元素原子的电子排布式___ ,J元素原子的外围电子排布式___ 。
(3)下列对比正确的是___ 。
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是____ 。
a.L位于元素周期表中第5周期ⅠA族,属于s区元素
b. O位于元素周期表中第7周期ⅧB族,属于d区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
(5)元素B和C的气态氢化物热稳定性较强的是____ (填化学式)。

(1)I的最高化合价为
(2)基态时G元素原子的电子排布式
(3)下列对比正确的是
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是
a.L位于元素周期表中第5周期ⅠA族,属于s区元素
b. O位于元素周期表中第7周期ⅧB族,属于d区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
(5)元素B和C的气态氢化物热稳定性较强的是
您最近一年使用:0次



