铁盐与亚铁盐在工业生产和生活中具有重要应用。三氯化铁在水溶液中易形成氢氧化铁胶体,具有吸附作用,可用作净水剂。三氯化铁溶液可用作印刷电路板刻剂,反应化学方程式为2FeCl3+Cu=2FeCl2+CuCl2。硫酸亚铁溶液可用于脱除烟气中的二氧化硫等有害气体。下列离子能在印刷电路板的蚀刻废液中大量存在的是
| A.H+ | B. | C.OH- | D.Ag+ |
更新时间:2022-01-20 08:39:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温时,下列各环境下的离子组合一定能够大量共存的是
A.0.1 mol/LNa2CO3的溶液中:Ca2+、Fe3+、 、Cl- 、Cl- |
B.0.1 mol/LHCl的溶液中:Fe3+、K+、I-、 |
| C.0.1 mol/LNaOH的溶液中:K+、Ba2+、Cl-、ClO- |
| D.0.1 mol/LNaHCO3的溶液中:Na+、K+、Al3+、Cl- |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】与Al反应放出大量氢气的溶液中,下列离子可能大量共存的是
| A.Mg2+、Na+、Cl-、NO3- | B.K+、Na+、Cl-、HCO3- |
| C.Na+、NH4+、Cl-、CH3COO- | D.Fe2+、Ba2+、Cl-、I- |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各组离子在指定溶液中,一定能大量共存的是( )
A.无色溶液中:[Al(OH)4]-、K+、OH-、NO |
B.能与铝片反应产生氢气的溶液中:Al3+、Cl-、Fe2+、NO |
C.常温下,pH=2的溶液中:SO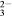 、Cl-、K+、SiO 、Cl-、K+、SiO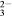 |
D.含有较多Fe3+的溶液中:Na+、SO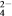 、SCN-、I- 、SCN-、I- |
您最近半年使用:0次
单选题
|
适中
(0.64)
【推荐2】常温下,下列各组离子在指定的水溶液中一定能大量共存的是
| A.使甲基橙变红的溶液:K+、Al3+、SO42-、NO3— |
| B.c(H+)=1×10—13mol·L—1的溶液:Na+、NH4+、SO42-、CO32- |
| C.c(Fe2+)=1.0 mol·L—1的溶液:H+、K+、Cl-、NO3— |
| D.含有大量Fe3+的溶液:Mg2+、Na+、SCN—、Cl— |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】实验测得pH=1.0的某溶液中还可能大量存在:Na+、Fe2+、Al3+、NH4+、SO42-、Cl-中的若干种离子,现进行了如下实验:
步骤I. 取该溶液10.0mL,加入过量1.0mol/LBa(NO3)2溶液,产生白色沉淀A和无色气体B,B遇空气立即变为红棕色:
步骤II. 向I所得的溶液中加入过量1.0mol/LNaOH溶液,有红褐色沉淀C和无色刺激性气体D生成。用铂丝蘸取所得溶液,在火焰上灼烧,火焰呈黄色;
步骤III. 向II所得的溶液中通入过量CO2有沉淀E生成。下列推断错误的是
步骤I. 取该溶液10.0mL,加入过量1.0mol/LBa(NO3)2溶液,产生白色沉淀A和无色气体B,B遇空气立即变为红棕色:
步骤II. 向I所得的溶液中加入过量1.0mol/LNaOH溶液,有红褐色沉淀C和无色刺激性气体D生成。用铂丝蘸取所得溶液,在火焰上灼烧,火焰呈黄色;
步骤III. 向II所得的溶液中通入过量CO2有沉淀E生成。下列推断错误的是
| A.步骤I中白色沉淀A的化学式为BaSO4 |
| B.步骤Ⅱ中产生沉淀C的反应:Fe3+ + 3OH-=Fe(OH)3↓ |
| C.CO2先后分别与 NaOH(aq)、NaAlO2(aq)反应 |
| D.原溶液一定含有:Na+、Fe2+、Al3+、SO42- |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式正确的是( )
| A.向溴化亚铁溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| B.向次氯酸钙溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| C.向硫酸氢钠溶液中滴加氢氧化钡至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D.将氢氧化铁粉末加入氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】在水溶液中能大量共存的一组离子是
A.NH 、Na+、Br-、SO 、Na+、Br-、SO | B.K+、Cu2+、OH-、NO |
C.Fe2+、H+、NO 、OH- 、OH- | D.Na+、H+、CO 、SO 、SO |
您最近半年使用:0次


 、OH-
、OH-


