有下列十种物质:①草木灰、②纯碱、③金刚石、④苛性钠、⑤生石灰、⑥硫酸、⑦碘酒、⑧氯化钠、⑨金属钠、⑩氧气和臭氧的混合气体,回答下列问题(填序号):
(1)只由一种元素组成的是____ ,只由两种元素组成的是____ 。
(2)属于混合物的是____ ,属于纯净物的是____ 。
(3)属于单质的是____ ,属于化合物的是____ 。
(4)属于酸的是____ ,属于碱的是_____ ,属于盐的是____ 。
(1)只由一种元素组成的是
(2)属于混合物的是
(3)属于单质的是
(4)属于酸的是
21-22高一·全国·假期作业 查看更多[2]
更新时间:2022-06-18 12:48:50
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】对于数以万计的化学物质和化学反应,分类法的作用几乎是无可替代的。
(1)现有下列5种物质:CuO、CO、MgO、Na2O、FeO,按照不同的分类标准,它们中有1种物质与其他4种物质有明显的不同,这种物质是_______ ,并写出两种依据:①_______ ②_______
(2)下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和Na2CO3五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:

①分类标准代号A表示_______ 。
a.两物质都是氧化物 b.两物质都可溶于水 c.两物质都是含碳化合物
②上述五种物质中的某一物质能与BaCl2反应,溶液中会有白色沉淀产生,该反应的化学方程式为:_______ 。
③上述五种物质中的某一物质能与澄清石灰水反应,且随着加入量的不同现象表现出差异,请写出相关现象_______ 以及与之相应的化学方程式:_______ 。
(1)现有下列5种物质:CuO、CO、MgO、Na2O、FeO,按照不同的分类标准,它们中有1种物质与其他4种物质有明显的不同,这种物质是
(2)下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和Na2CO3五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:

①分类标准代号A表示
a.两物质都是氧化物 b.两物质都可溶于水 c.两物质都是含碳化合物
②上述五种物质中的某一物质能与BaCl2反应,溶液中会有白色沉淀产生,该反应的化学方程式为:
③上述五种物质中的某一物质能与澄清石灰水反应,且随着加入量的不同现象表现出差异,请写出相关现象
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.下列每组中都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来写在横线上:
(1)NaCl、KCl、NaClO、MgCl2_______
(2)H3PO4 、H2SO3 、HCl、HNO3_______
(3)CO2、CaO、 SO3、SO2_______
(4)空气、盐酸、氨水、胆矾_______
(5)Mg、Al、Zn、S_______
II.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,不能形成Fe(OH)3胶体的是_______ 。
A.冷水 B.沸水 C.NaOH稀溶液 D.NaCl浓溶液
(2)区分Fe(OH)3胶体与FeCl3溶液的方法是_______ ,分离提纯Fe(OH)3胶体的方法是_______ 。
(3)氢氧化铁胶体能稳定存在的原因是_______ (选填序号)。
A.胶体微粒直径在1 nm -100nm之间 B.胶体微粒能透过滤纸
C.胶体微粒做布朗运动 D.胶体微粒带电荷
(1)NaCl、KCl、NaClO、MgCl2
(2)H3PO4 、H2SO3 、HCl、HNO3
(3)CO2、CaO、 SO3、SO2
(4)空气、盐酸、氨水、胆矾
(5)Mg、Al、Zn、S
II.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,不能形成Fe(OH)3胶体的是
A.冷水 B.沸水 C.NaOH稀溶液 D.NaCl浓溶液
(2)区分Fe(OH)3胶体与FeCl3溶液的方法是
(3)氢氧化铁胶体能稳定存在的原因是
A.胶体微粒直径在1 nm -100nm之间 B.胶体微粒能透过滤纸
C.胶体微粒做布朗运动 D.胶体微粒带电荷
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】Mg、H、O、S、Cl五种元素可组成下表所示各类物质:
回答下列问题:
(1)物质①、②、③的化学式分别为________ 、 ________ 、 ________ 。
(2)写出①与②反应的离子方程式:_______________________________________ 。
(3)写出由⑤制备 的化学方程式:
的化学方程式: __________________________________________ 。
(4)元素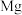 与Cl可形成
与Cl可形成 ,根据后面括号要求,各写出一种制备
,根据后面括号要求,各写出一种制备  的化学反应方程式:
的化学反应方程式: _________________________ (置换反应)、 _______________ (复分解反应)。
| 类别 | 强酸 | 碱 | 硫酸盐 | 氧化物 | 氢化物 |
| 化学式 | ① | ② | ③ | ④ | ⑤ |
(1)物质①、②、③的化学式分别为
(2)写出①与②反应的离子方程式:
(3)写出由⑤制备
 的化学方程式:
的化学方程式: (4)元素
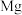 与Cl可形成
与Cl可形成 ,根据后面括号要求,各写出一种制备
,根据后面括号要求,各写出一种制备  的化学反应方程式:
的化学反应方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ.现有以下物质:①NaCl溶液 ②NH3③冰醋酸(纯净的醋酸) ④铜 ⑤K2SO4固体 ⑥蔗糖 ⑦酒精 ⑧熔融的MgO ⑨盐酸 ⑩铁
(1)其中能导电的是___________ (填序号,下同);属于电解质的是___________ ,属于非电解质的是___________ 。
(2)写出物质⑤溶于水的电离方程式___________ 。
(3)写出物质⑨和物质⑩反应的化学方程式___________ 。
Ⅱ.甘肃马家窑遗址出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,其化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。回答下列问题:
(4)CO2属于___________ 氧化物。(填“酸性”或“碱性”)
(5)从物质分类标准看,“铜绿”属于哪类物质___________。(填选项)
(6)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:
反应Ⅰ: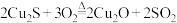 ,
,
反应Ⅱ: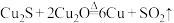 。
。
①反应Ⅰ中,氧化产物是___________ ,还原产物是___________ 。
②反应Ⅱ中,Cu2O的作用是___________ 。(填“氧化剂”“还原剂”或“氧化剂和还原剂”)
(1)其中能导电的是
(2)写出物质⑤溶于水的电离方程式
(3)写出物质⑨和物质⑩反应的化学方程式
Ⅱ.甘肃马家窑遗址出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,其化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。回答下列问题:
(4)CO2属于
(5)从物质分类标准看,“铜绿”属于哪类物质___________。(填选项)
| A.酸 | B.碱 | C.盐 | D.氧化物 |
反应Ⅰ:
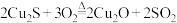 ,
,反应Ⅱ:
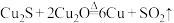 。
。①反应Ⅰ中,氧化产物是
②反应Ⅱ中,Cu2O的作用是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】硼酸晶体成片状,有滑腻感,可作润滑剂,硼酸分子结构可表示为 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
(1)根据以上所述可知硼酸应属于___________ 。
A.强酸 B.中强酸 C.弱酸
(2)研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有___________ 个。
(3)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸三甲酯,试写出硼酸完全酯化的化学方程式(注明反应条件)___________ 。
(4)已知硼酸0.01mol可被20mL 0.5mol·L-1 NaOH溶液恰好完全中和,据此推测:硼酸在水中显酸性的原因是(写电离方程式)___________ 。
 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面(1)根据以上所述可知硼酸应属于
A.强酸 B.中强酸 C.弱酸
(2)研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有
(3)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸三甲酯,试写出硼酸完全酯化的化学方程式(注明反应条件)
(4)已知硼酸0.01mol可被20mL 0.5mol·L-1 NaOH溶液恰好完全中和,据此推测:硼酸在水中显酸性的原因是(写电离方程式)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】现有①氧气;②空气;③碱式碳酸铜;④氯酸钾;⑤硫;⑥水;⑦氧化镁;⑧氯化钠等物质,其中属于单质的有(填序号)_________________________ ;属于化合物的有____________________ ,属于混合物的有_____________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下面的适当位置(填化学式)。
①金属单质_____ 。
②非金属单质_____ 。
③化合物:_____ 。
(2)从(1)中的四种物质中选出一种或几种为反应物,按下述反应类型,各写一个化学方程式。
①分解反应:____ ;
②化合反应:____ ;
③置换反应:_____ ;
④复分解反应:____ 。
(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下面的适当位置(填化学式)。
①金属单质
②非金属单质
③化合物:
(2)从(1)中的四种物质中选出一种或几种为反应物,按下述反应类型,各写一个化学方程式。
①分解反应:
②化合反应:
③置换反应:
④复分解反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】牙膏是常见的日用化学品。磨擦剂是牙膏的主体原料,在牙膏中最重要的作用就是去除牙垢,减轻牙结石。
I.按要求回答下列问题
(1)表中列出了牙膏中常见的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
(2)根据用途推测 SiO2在水中的溶解性:_______ (填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂氢氧化镁可以用菱镁矿(主要成分为MgCO3、CaCO3、FeCO3、SiO2)来制备,按要求回答下列问题。

①该方案中属于电解质的物质是_______ (填字母)

A.菱镁矿 B .CO2 C . NH4 Cl D .H2 O E.硫酸钙 F.氨
②方案中可循环利用的物质有_______ (填化学式)
Ⅱ.某牙膏摩擦剂的成分为CaCO3,为测定其中CaCO3的含量的操作如下(设该牙膏中的其他成分不与 盐酸或者氢氧化钠反应) :
①配制0. 10mol.L-1稀盐酸和0. 10mol.L-1NaOH 溶液;
②称取 0.60g 该牙膏,溶于水并稀释至20.00 mL;
③加入 25.00mL0.10mol . L-1稀盐酸;
④用0.10mol .L-1NaOH 溶液中和过量的稀盐酸, 记录所消耗氢氧化钠溶液的体积;
(4)该测定实验共进行了 4 次。实验室现有 50mL 、100mL 、250mL 、500mL4 种规格的容量瓶, 则配制盐酸应选用的容量瓶规格为_______
(5)某同学 4 次测定所消耗 NaOH 溶液的体积如表。
则该牙膏中碳酸钙的质量分数约为_______ (保留三位有效数字) %
I.按要求回答下列问题
(1)表中列出了牙膏中常见的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
| 摩擦剂成分 | 氢氧化镁 | 碳酸钙 | 二氧化硅 |
| 物质类别 | ① | ② | ③ |
(3)牙膏中的摩擦剂氢氧化镁可以用菱镁矿(主要成分为MgCO3、CaCO3、FeCO3、SiO2)来制备,按要求回答下列问题。

①该方案中属于电解质的物质是

A.菱镁矿 B .CO2 C . NH4 Cl D .H2 O E.硫酸钙 F.氨
②方案中可循环利用的物质有
Ⅱ.某牙膏摩擦剂的成分为CaCO3,为测定其中CaCO3的含量的操作如下(设该牙膏中的其他成分不与 盐酸或者氢氧化钠反应) :
①配制0. 10mol.L-1稀盐酸和0. 10mol.L-1NaOH 溶液;
②称取 0.60g 该牙膏,溶于水并稀释至20.00 mL;
③加入 25.00mL0.10mol . L-1稀盐酸;
④用0.10mol .L-1NaOH 溶液中和过量的稀盐酸, 记录所消耗氢氧化钠溶液的体积;
(4)该测定实验共进行了 4 次。实验室现有 50mL 、100mL 、250mL 、500mL4 种规格的容量瓶, 则配制盐酸应选用的容量瓶规格为
(5)某同学 4 次测定所消耗 NaOH 溶液的体积如表。
| 实验标号 | 1 | 2 | 3 | 4 |
| V (NaOH) /mL | 10.10 | 9.90 | 10.20 | 9.80 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】有以下物质;①石墨②铁③蔗糖④一氧化碳⑤氯化铁固体⑥碳酸氢钠固体⑦氢氧化钡溶液⑧纯醋酸⑨熔融氯化钠⑩液态氯化氢
(1)其中能导电的是___________ ;属于非电解质的是___________ ;属于弱电解质的是___________ 。
(2)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:___________ 。
(3)写出用⑤的饱和溶液制备 胶体的离子方程式:
胶体的离子方程式:___________ 。
(4)磷酸( )、亚磷酸(
)、亚磷酸( )来次磷酸(
)来次磷酸( )都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则
)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则 、
、 、
、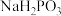 中属于正盐的是
中属于正盐的是___________ (填化学式)。
(1)其中能导电的是
(2)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:
(3)写出用⑤的饱和溶液制备
 胶体的离子方程式:
胶体的离子方程式:(4)磷酸(
 )、亚磷酸(
)、亚磷酸( )来次磷酸(
)来次磷酸( )都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则
)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则 、
、 、
、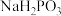 中属于正盐的是
中属于正盐的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】无机化合物可根据其组成和性质进行分类,
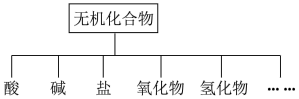
(1)如图所示的物质分类方法名称是___ 。
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②、④、⑥、⑧、⑩后面。
(3)SO2和CO2都属于酸性氧化物,在化学性质上有很多相似的地方,请写出少量的⑦与③反应的化学反应方程式为:___ 。
(4)磷的一种化合物叫亚磷酸(H3PO3),从交叉分类的角度看,它属于二元弱酸,则Na2HPO3属于___ 盐(填正盐、酸式盐或碱式盐)。
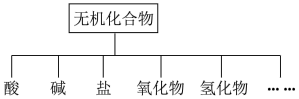
(1)如图所示的物质分类方法名称是
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②、④、⑥、⑧、⑩后面。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ② | ③NaOH ④ | ⑤Na2SO4 ⑥ | ⑦SO2 ⑧ | ⑨NH3 ⑩ |
(4)磷的一种化合物叫亚磷酸(H3PO3),从交叉分类的角度看,它属于二元弱酸,则Na2HPO3属于
您最近一年使用:0次

 ,
, ,
, ,
, ,
, ,浑浊的河水,
,浑浊的河水, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,
, ,空气,
,空气, ,
, ,
, ,
, ,
, 。
。

